Clear Sky Science · nl
KDM5B werkt samen met het CRL4B-complex om de tumorvorming van ER+ borstkanker te bevorderen via regulatie van cholestermetabolisme
Waarom dit onderzoek belangrijk is voor de dagelijkse gezondheid
Borstkanker is de meest voorkomende kanker bij vrouwen, en veel tumoren groeien als reactie op het hormoon oestrogeen. Deze kankers doen meer dan snel delen — ze herprogrammeren ook hoe ze vetten zoals cholesterol gebruiken. Deze studie onthult hoe een gen-regulerend eiwit genaamd KDM5B samenwerkt met een ander eiwitcomplex, CRL4B, om het cholesterol in oestrogeenreceptor–positieve (ER+) borstkankercellen te verhogen. Door dit verborgen partnerschap te begrijpen, hopen wetenschappers nieuwe manieren te vinden om tumorgroei te vertragen en bestaande behandelingen te verbeteren, zoals hormoontherapie en cholesterolverlagende medicijnen.
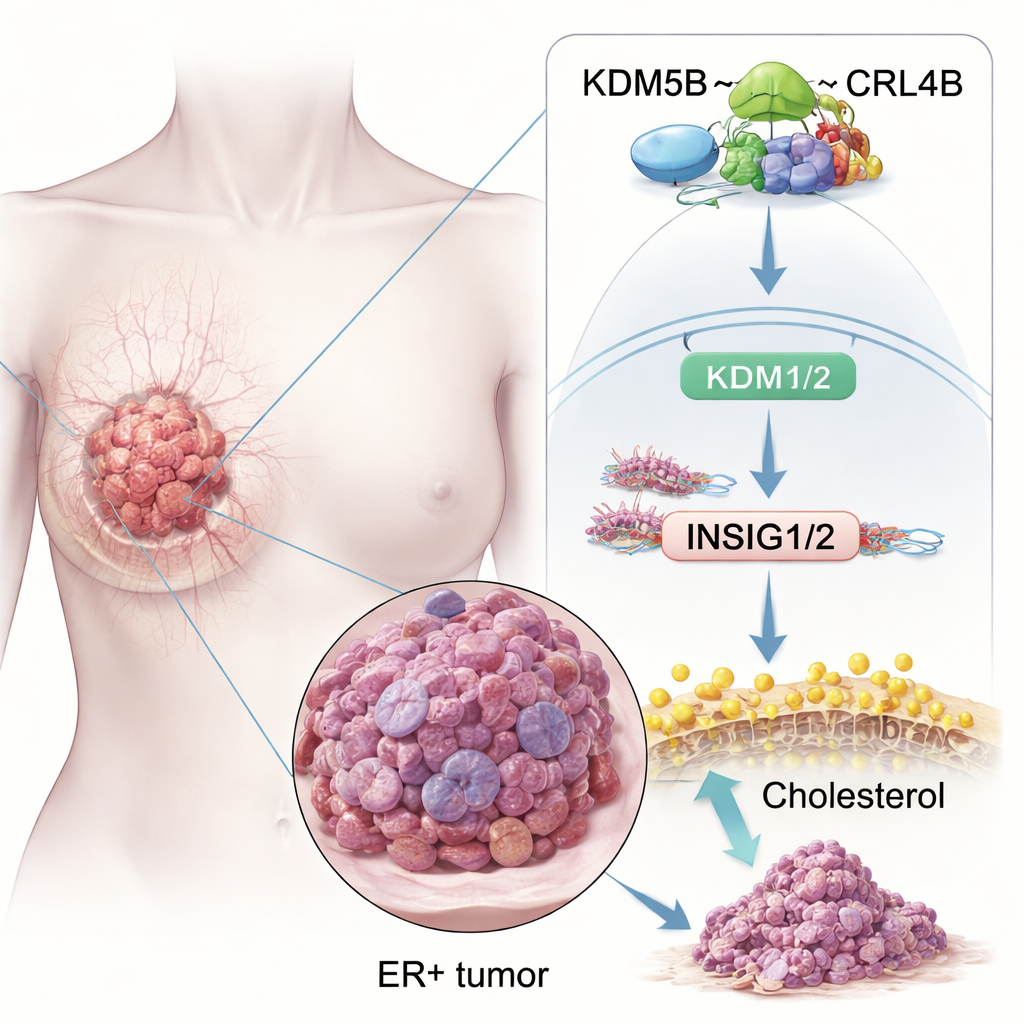
Een eiwit dat het evenwicht richting kanker doet kantelen
De onderzoekers stelden eerst de vraag of KDM5B louter aanwezig is in ER+ borstkankers of daadwerkelijk bijdraagt aan hun ontwikkeling. Door grote kankerdatabanken en weefselmonsters te analyseren, vonden ze dat KDM5B-niveaus hoger zijn in borsttumoren dan in normaal borstweefsel, en vooral hoog in ER+ tumoren. Patiënten waarvan de kanker meer KDM5B produceert, hebben doorgaans een slechtere overleving, zelfs wanneer ze standaard chemotherapie of hormoontherapie krijgen. In kweekexperimenten zorgde het opdrijven van KDM5B ervoor dat ER+ borstkankercellen sneller groeiden, gemakkelijker weefsel binnendrongen en meer stamcelachtige klonten vormden, waarvan men denkt dat ze nieuwe tumoren kunnen starten. Het onderdrukken van KDM5B had het tegengestelde effect en verkleinde kolonies in kweek en tumoren in muismodellen.
Een krachtige samenwerking binnen kankercellen
Om te zien hoe KDM5B deze effecten veroorzaakt, zocht het team naar zijn eiwitpartners. Ze ontdekten dat KDM5B fysiek bindt aan onderdelen van een moleculair apparaat genaamd het CRL4B-complex, een enzymatisch systeem dat eiwitten labelt en ook de verpakking van DNA verandert. Gedetailleerde biochemische tests toonden aan dat KDM5B rechtstreeks interageert met twee CRL4B-componenten, CUL4B en DDB1, via specifieke regio’s van elk eiwit. In ER+ borstkankercellen werkt dit KDM5B–CRL4B-complex op veel genen bij hun aan/uit-schakelaars. Met genoomwijde mapping vonden de auteurs dat KDM5B en CUL4B vaak samen op promoters van genen zitten, waar ze chemische tags op histon-eiwitten aanpassen — de spoelen waar DNA omheen gewikkeld is — om genen uit te schakelen.
De rem loslaten op cholesterol
Onder de veelal beïnvloede routes viel het cholesterolverkeer op. Kankercellen hebben extra cholesterol nodig om membranen op te bouwen en stress te weerstaan, en ER+ tumoren gebruiken ook cholesterol-afgeleide moleculen om oestrogeen na te bootsen. De studie toont aan dat het KDM5B–CRL4B-complex rechtstreeks bindt aan de controleregions van twee belangrijke “rem”-genen, INSIG1 en INSIG2. Deze genen helpen normaal gesproken een hoofdregulator van cholesterol, SREBP2, onder controle te houden. KDM5B–CRL4B voegt een repressief merkteken (H2AK119ub1) toe en verwijdert een activerend merkteken (H3K4me3) op histonen bij de INSIG1/2-promoters, waardoor deze genen naar beneden worden bijgesteld. Met minder INSIG1/2-eiwitten wordt SREBP2 vrij om cholesterolverhogende genen aan te zetten, wat het cholesterolgehalte in ER+ borstkankercellen verhoogt en hun invasief gedrag versterkt. Wanneer de onderzoekers KDM5B of CRL4B verstoorden, stegen INSIG1/2, daalde SREBP2-activiteit en nam het totale cholesterol in cellen af.
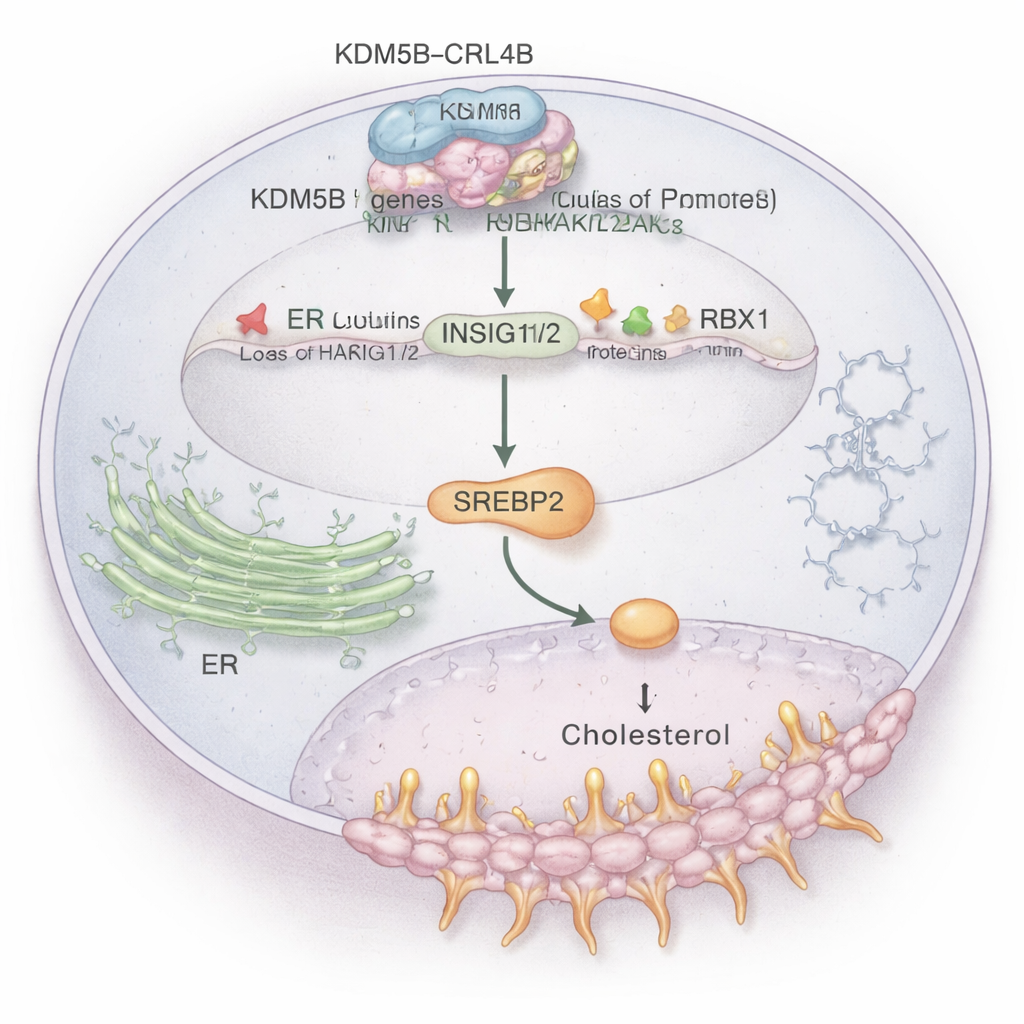
Cholesterolverlagende middelen en kankersignalen kruisen elkaar
Het werk koppelt deze route ook aan een cholesterol‑afgeleid signaal genaamd 27‑hydroxycholesterol (27‑HC), een molecuul dat al bekend staat om het bevorderen van ER+ borstkanker. Behandeling van ER+ cellen met 27‑HC verhoogde KDM5B-niveaus en onderdrukte verder INSIG1/2, waardoor cellen meer neigden naar groei en invasie. Belangrijk is dat het blokkeren van KDM5B of CRL4B deze agressieve effecten temperde, wat suggereert dat 27‑HC deels werkt via de KDM5B–CRL4B-as. Daarnaast toonden de onderzoekers aan dat simvastatine, een veelgebruikte cholesterolverlagende statine, de groei van borstkankercellen vertraagde, en dat in combinatie met een KDM5B-remmer het anti‑tumoreffect sterker was. Dit wijst erop dat het combineren van middelen die de cholesterolproductie remmen met middelen die KDM5B’s genregulerende activiteit blokkeren een veelbelovende therapeutische strategie kan zijn.
Wat dit betekent voor patiënten en toekomstige behandelingen
Deze studie onthult een nieuwe keten van gebeurtenissen binnen ER+ borstkankercellen: een cholesterolgerelateerd signaal (27‑HC) verhoogt KDM5B; KDM5B werkt samen met het CRL4B-complex om INSIG1 en INSIG2 uit te schakelen; dit maakt SREBP2 los, verhoogt de cholesterolproductie en helpt tumoren groeien, invasief te worden en stamcelachtige eigenschappen te behouden. Omdat KDM5B ook verhoogd is en gekoppeld aan slechte overleving in verschillende andere kankers, kan het blokkeren van dit eiwit — of het herstel van de INSIG1/2-remmen — nieuwe manieren bieden om tumorgroei te beheersen. Hoewel meer onderzoek nodig is voordat dit in de klinische praktijk kan worden toegepast, benadrukken de bevindingen hoe nauw het kankergedrag verbonden is met alledaagse moleculen zoals cholesterol, en hoe bestaande medicijnen zoals statines op termijn mogelijk gecombineerd kunnen worden met epigenetische therapieën om de uitkomsten te verbeteren.
Bronvermelding: Yang, Y., Gao, T., Yuan, B. et al. KDM5B cooperates with CRL4B complex to promote the tumorigenesis of ER+ breast cancer via regulating cholesterol metabolism. Cell Death Dis 17, 207 (2026). https://doi.org/10.1038/s41419-026-08438-1
Trefwoorden: ER-positieve borstkanker, cholestermetabolisme, KDM5B, INSIG1/INSIG2, epigenetische therapie