Clear Sky Science · nl
Herstel van apoptose in fotoreceptorcellen: een rol voor mitofagie
Wanneer stervende oogcellen een tweede kans krijgen
Veel blindmakende aandoeningen beginnen op dezelfde manier: lichtgevoelige cellen in het oog, fotoreceptoren genoemd, beginnen te sterven en komen niet terug. Deze studie onthult een verrassende wending in dat verhaal. Onder de juiste omstandigheden kunnen fotoreceptoren die op het punt lijken te staan van geprogrammeerde celdood zich terugtrekken van de rand, cruciale onderdelen repareren en overleven. Begrijpen hoe deze “tweede kans” werkt, kan nieuwe wegen openen om het gezichtsvermogen te behouden bij aandoeningen zoals retinale loslating en leeftijdsgebonden maculadegeneratie.
Oogcellen in gevaar bij veelvoorkomende blindheid
Fotoreceptoren bevinden zich achter in het oog en zetten licht om in elektrische signalen die de hersenen kunnen begrijpen. Zodra deze cellen volgroeid zijn, delen ze zich niet meer, dus wanneer ze sterven, is het gezichtsvermogen permanent aangetast. Bij retinale loslating en andere netvliesaandoeningen sterven fotoreceptoren vaak via apoptose, een nette zelfvernietigingsroutine die lange tijd werd beschouwd als onomkeerbaar zodra ze volledig op gang is gekomen. Toch suggereert klinische ervaring dat snelle heraanhechting van een losgelaten netvlies nuttig zicht kan herstellen, wat impliceert dat ten minste sommige fotoreceptoren gered kunnen worden, zelfs nadat ze aan deze doodsmarche zijn begonnen.
Van doodsspiraal naar herstel
De onderzoekers gebruikten een muizencone-fotoreceptorcellenlijn om te onderzoeken of deze cellen konden herstellen na ernstige stress. Ze brachten de cellen in contact met twee krachtige triggers van apoptose: een medicijn dat interne doodsmechanismen activeert en langdurige lage zuurstofcondities die nabootsen wat gebeurt tijdens retinale loslating. Onder beide stressoren vertoonden de cellen klassieke tekenen van apoptose: ze werden bol, vormden membraanblaasjes, activeerden sleutelenzymen die eiwitten afbreken en toonden noodsignalen op hun oppervlak. Toen de stress echter werd opgeheven, herwonnen veel cellen geleidelijk hun oorspronkelijke uitgerekte vorm en schakelden ze de doodsmachinerie binnen ongeveer 24 uur uit, wat aantoont dat zelfs laatstadiumveranderingen niet altijd eenrichtingsverkeer zijn.
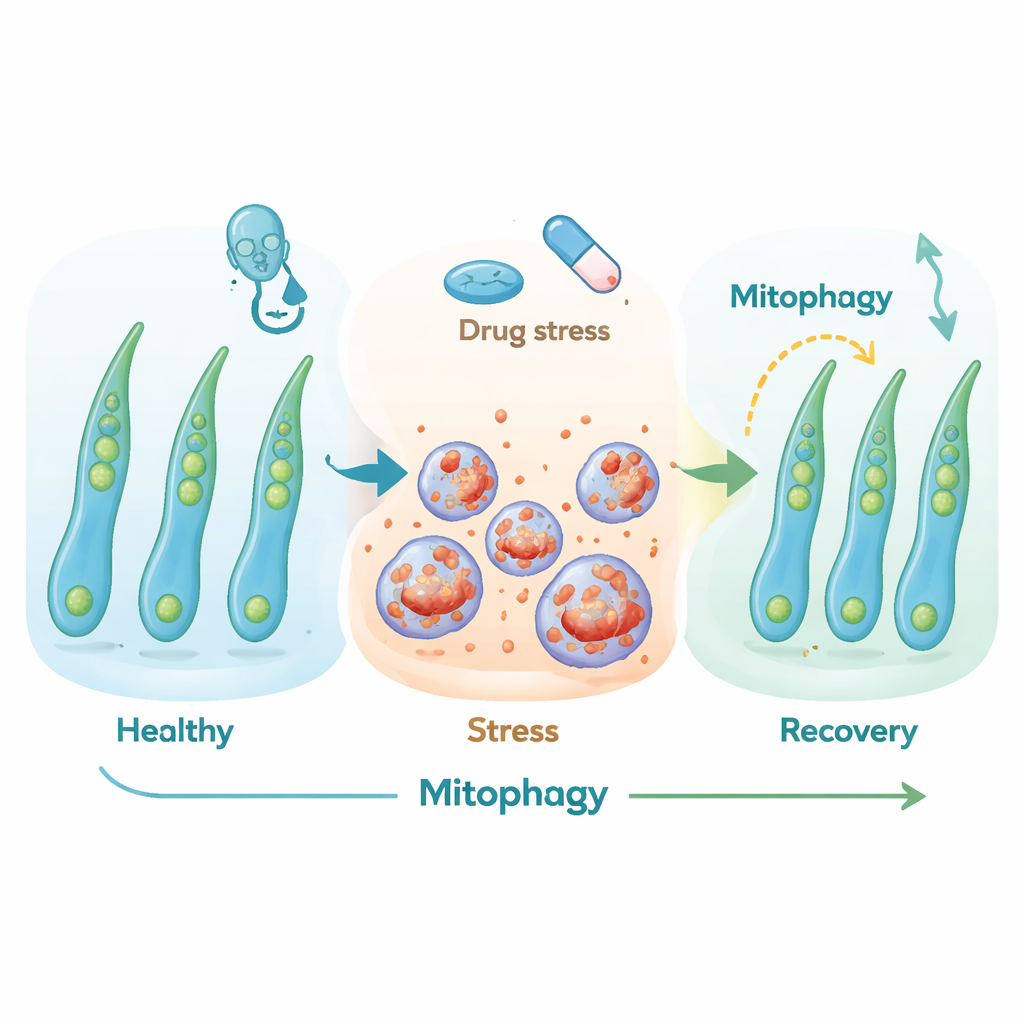
Krachtcentrales in onderhoud
Om te begrijpen hoe deze cellen erin slaagden te herstellen, richtte het team zich op de mitochondriën — de kleine krachtcentrales die cellulaire energie leveren en helpen beslissen of een cel leeft of sterft. Tijdens stress raakte de mitochondriale functie verstoord: energieniveaus daalden in geneesmiddelbehandelde cellen en schadelijke zuurstofbijproducten stegen in beide stressmodellen. Nadat de stress was opgeheven, herstelden overlevende cellen hun energieniveaus, verminderden ze schadelijke reactieve zuurstofsoorten en toonden ze signalen van vernieuwde mitochondriale aanmaak. De balans tussen mitochondriale splitsing en fusie verschoof ook op manieren die de opruiming van beschadigde componenten en het herbouwen van een gezonder netwerk ondersteunen.
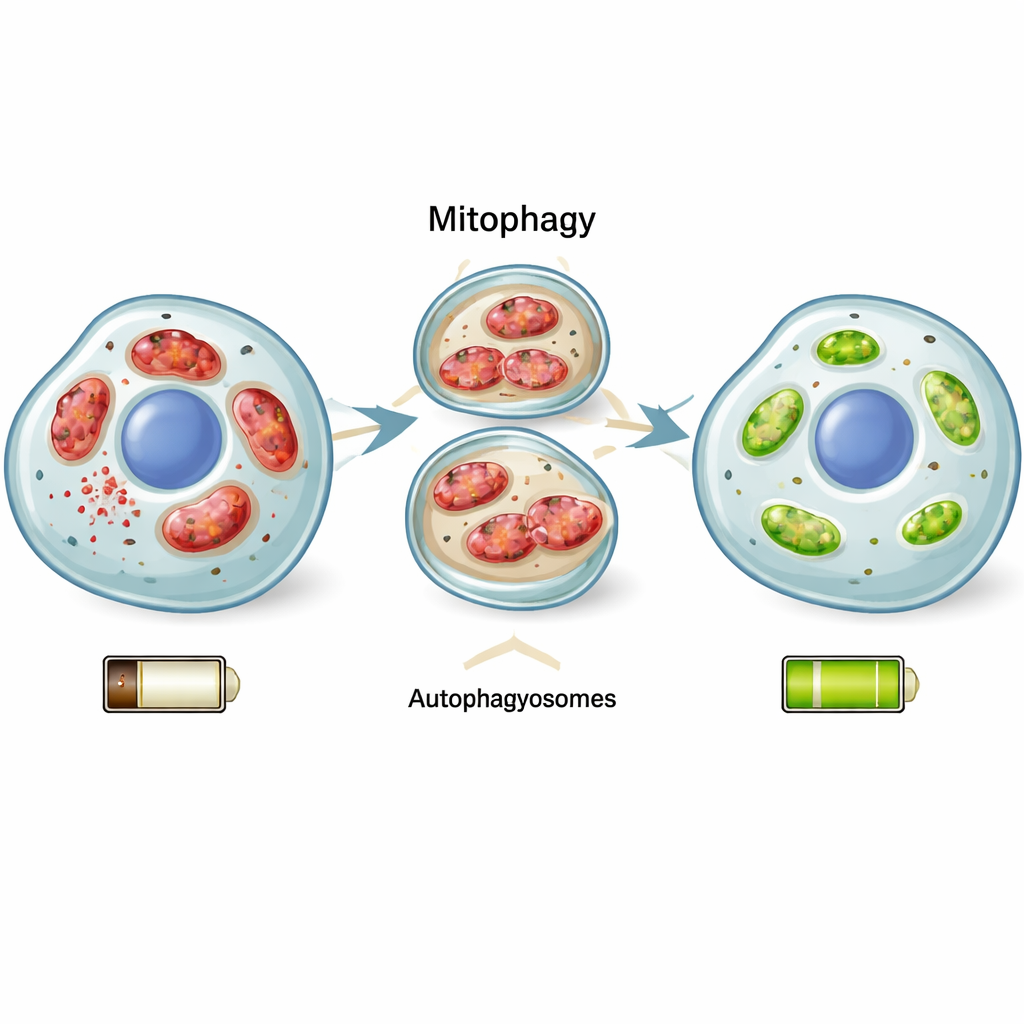
Mitofagie: gerichte opruiming die cellen redt
Een centrale speler in deze ommekeer was mitofagie, een kwaliteitscontroleproces dat selectief defecte mitochondriën verwijdert voordat ze de rest van de cel kunnen vergiftigen. De onderzoekers vonden dat toen fotoreceptoren herstelden van stress, ze genen en eiwitten opschroefden die mitofagie en algemene cellulair recycling aansturen. Wanneer ze mitofagie versterkten met een middel dat deze opruimroute bevordert, stierven minder cellen. Wanneer ze mitofagie blokkeerden, stokte het herstel praktisch en gingen meer cellen ten onder. Dit wees op mitofagie niet slechts als toeschouwer, maar als een sleutelstrategie voor overleven.
Bewijs in een levend oog
Celcultuurexperimenten hebben hun beperkingen, dus ontwikkelde het team een muismodel waarbij een deel van het netvlies losraakt en binnen enkele dagen vanzelf weer aanhecht. In deze dieren toonden fotoreceptoren in de heraangehechte gebieden veel minder merkers van celdood en een beter behouden structuur dan in ogen waar de loslating blijvend was gemaakt. Dit levende systeem komt nauw overeen met wat gebeurt bij patiënten wier netvliezen chirurgisch worden heraangehecht en ondersteunt het idee dat echte fotoreceptoren in het oog kunnen herstellen van ernstige stress als de beschadiging tijdig wordt weggenomen.
Wat dit kan betekenen voor het behoud van zicht
Kort gezegd laat de studie zien dat fotoreceptoren soms een ver gevorderd zelfvernietigingsprogramma kunnen stoppen en omkeren, mits hun mitochondriale “motoren” worden gerepareerd via mitofagie. Dit daagt het oude idee uit dat zodra deze lichtgevoelige cellen apoptose ingaan, ze verloren zijn. Als toekomstige behandelingen mitofagie en andere mitochondriale herstelroutes op het juiste moment — bijvoorbeeld rond de tijd van retinale reattachering — veilig kunnen versterken, zouden artsen mogelijk meer fotoreceptoren kunnen behouden en zo meer gezichtsvermogen voor patiënten in gevaar voor blindheid kunnen sparen.
Bronvermelding: Kaur, B., Miglioranza Scavuzzi, B., Yao, J. et al. Recovery from apoptosis in photoreceptor cells: A role for mitophagy. Cell Death Dis 17, 167 (2026). https://doi.org/10.1038/s41419-026-08436-3
Trefwoorden: fotoreceptoren, retinale loslating, apoptose, mitofagie, mitochondriën