Clear Sky Science · nl
TGFβ-signaal bevordert celdeling en weerstand tegen de CDK4/6-remmer palbociclib via SOX4-transcriptionele modulatie in borstkankercellen
Wanneer kankercellen een behulpzaam signaal kapen
Ons lichaam is afhankelijk van talloze chemische signalen om cellen te laten delen wanneer dat nodig is en te stoppen wanneer dat wenselijk is. Een van deze signalen, transformerende groeifactor bèta (TGFβ), helpt normaal gesproken bij het voorkomen van tumoren. Deze studie laat zien hoe hetzelfde TGFβ-signaal bij bepaalde vormen van borstkanker kan worden verdraaid zodat het tumorcellen juist helpt te groeien en weerstand te bieden tegen een belangrijk geneesmiddel, palbociclib. Inzicht in deze omschakeling kan leiden tot betere behandelcombinaties voor patiënten wier tumoren niet langer op therapie reageren.
Van groeiremming naar een tweesnijdend signaal
In gezond weefsel werkt TGFβ gewoonlijk als een rem: het vertraagt celdeling en beperkt ontsteking, wat helpt vroege tumorvorming te voorkomen. Maar in gevestigde kankers, met name in mammatumoren die al kankerbevorderende mutaties hebben verworven, kan TGFβ het tegenovergestelde doen—het stimuleert cellen om te migreren, binnen te dringen en uit te zaaien. Om dit dubbelgedrag te onderzoeken gebruikten de onderzoekers 3D “mini-tumoren” gekweekt uit humane borstcellen. Ze vergeleken normaal-achtige cellen met anderszins identieke cellen die een oncogene HRAS-mutatie dragen, die hen richting kanker duwt. Deze gecontroleerde opzet stelde hen in staat te vragen hoe hetzelfde TGFβ-signaal uitpakt in een voor-kanker versus een kankergelijke omgeving. 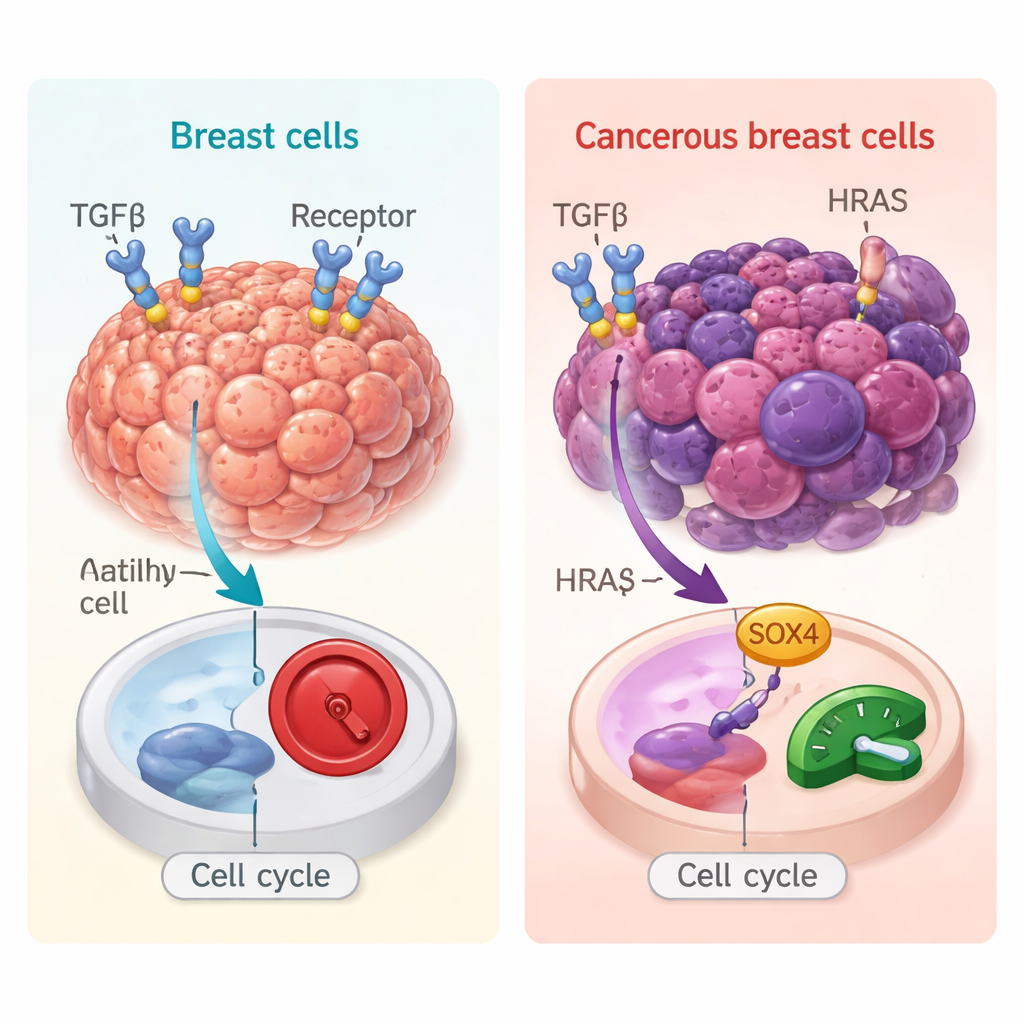
Het herschakelen van de genoomaan/uit-schakelaars
Het team keek naar chromatine, het DNA-en-eiwitpakket dat bepaalt welke genen toegankelijk zijn en aan gezet kunnen worden. Na behandeling van de 3D-celclusters met TGFβ zagen ze wijdverspreide openingen in chromatine bij genstarters en bij verre enhancerregio’s in zowel normaal-achtige als HRAS-mutante cellen. De patronen van nieuw-toegankelijke plekken verschilden echter sterk tussen de twee. In de kankergelijke cellen waren bindingsplaatsen voor een transcriptiefactor genaamd SOX4 uitzonderlijk verrijkt. Tegelijkertijd toonde genexpressieprofilering dat TGFβ niet langer alleen bekende programma’s zoals epitheel–mesenchymale transitie (geassocieerd met invasie) en metabolische verschuivingen activeerde; in de HRAS-mutante cellen versterkte het ook genen die betrokken zijn bij DNA-replicatie, DNA-reparatie en het doorgaan door belangrijke celcycluscontrolepunten.
SOX4 als moleculair tussenstation
Dieper graven liet zien dat SOX4 in het hart van deze omschakeling staat. Single-cell RNA-sequencinggegevens van primaire borsttumoren toonden aan dat SOX4 wordt mede-geëxprimeerd met celcyclusdrijvers zoals CDK4, CDK6 en cycline D1 (CCND1), vooral in actief delende kankercellen. In hun 3D-modellen verhoogde TGFβ de SOX4-niveaus, en SOX4 werd aangetroffen gebonden nabij de regelregio’s van deze celcyclusgenen, met name CDK4. Wanneer SOX4 met genetische middelen werd verminderd, kon TGFβ veel van zijn doelgenen niet langer effectief aanzetten, inclusief die gekoppeld aan celdeling en weefselhervorming, en werden de kankergelijke sferen minder invasief en stabieler. Biochemische experimenten toonden verder aan dat SOX4 samenwerkt met SMAD3, een centrale TGFβ-signaaldrager, en een coöperatief module in de celkern vormt die genactivatie versterkt.
Ondergraven van een eerstelijns geneesmiddel bij borstkanker
Palbociclib is een veelgebruikt geneesmiddel dat CDK4 en CDK6 blokkeert, eiwitten die cellen van een rusttoestand naar actieve deling sturen. Veel patiënten ontwikkelen uiteindelijk resistentie tegen deze behandeling. De auteurs combineerden grote datasets van geneesmiddelresponsen met labexperimenten in meerdere borstkankercellijnen en 3D-culturen. Ze vonden dat sterkere TGFβ-activiteit, samen met SOX4 en verwante genhandtekeningen, geassocieerd is met hogere noodzaak aan palbociclib-doseringen om groei te remmen. In het laboratorium maakte het toevoegen van TGFβ kankercellen minder gevoelig voor palbociclib, terwijl het blokkeren van TGFβ-signaal of het neerhalen van SOX4 de gevoeligheid herstelde. Langdurige blootstelling aan palbociclib leidde tot resistente cellijnen die verhoogde TGFβ-signalisatie, meer SOX4, en sterkere kenmerken van actief chromatine bij het SOX4-gen zelf vertoonden. In zebravismodellen verminderde remming van TGFβ de groei van tumoren afkomstig van palbociclib-resistente cellen aanzienlijk. 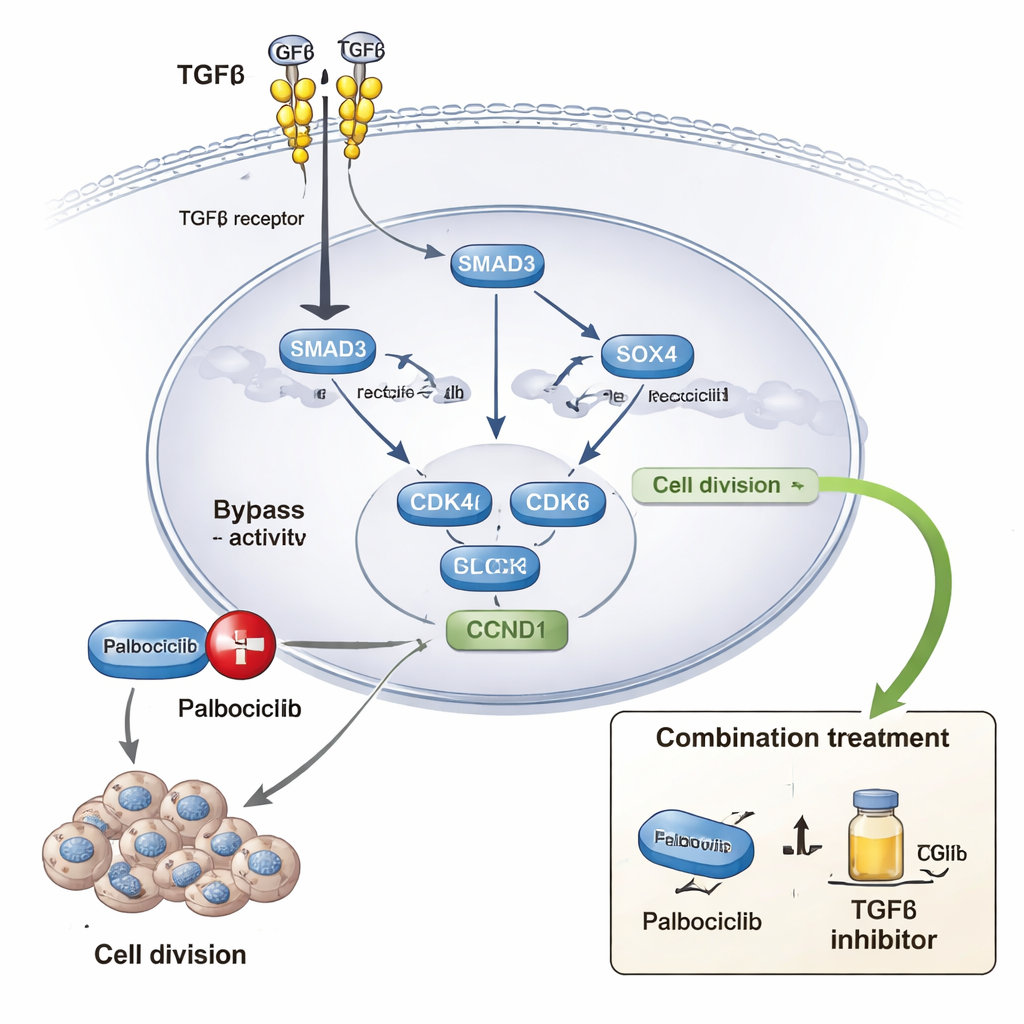
Wat dit betekent voor patiënten en toekomstige therapieën
Voor niet-specialisten is de kernboodschap dat een signaal bedoeld om ons tegen kanker te beschermen, in de verkeerde context kan worden gekaapt om tumoren te helpen overleven en geneesmiddelen te slim af te zijn. Hier werkt TGFβ samen met SOX4 om cruciale regio’s van het genoom te openen, celcyclusmotoren zoals CDK4 en CDK6 aan te zetten en het effect van palbociclib te verzwakken. De bevindingen suggereren dat, voor sommige vormen van borstkanker, het combineren van CDK4/6-remmers met middelen die TGFβ-signalisatie blokkeren—of die SOX4-gedreven programma’s targeten—resistentie zou kunnen uitstellen of overwinnen. Hoewel meer klinisch onderzoek nodig is, brengt deze studie een gedetailleerde moleculaire ontsnappingsroute van kankercellen in kaart en wijst ze op nieuwe manieren om die af te snijden.
Bronvermelding: Ali, M.M., Itoh, Y., Badji, A.M.P. et al. TGFβ signaling promotes cell cycle progression and resistance to the CDK4/6 inhibitor palbociclib through SOX4 transcriptional modulation in breast cancer cells. Cell Death Dis 17, 209 (2026). https://doi.org/10.1038/s41419-026-08435-4
Trefwoorden: borstkanker, TGF-beta signaal, SOX4, palbociclib-resistentie, celcyclus