Clear Sky Science · nl
BCL-xL als therapeutisch doelwit bij cetuximab-refractaire colorectale kanker
Waarom dit belangrijk is voor mensen met darmkanker
Colorectale (dikke darm en endeldarm) kanker is een van de meest voorkomende vormen van kanker wereldwijd, en veel patiënten met gevorderde ziekte krijgen een gerichte antilichaamtherapie genaamd cetuximab. Dit middel kan aanvankelijk tumoren verkleinen, maar bij de meeste patiënten vindt de kanker binnen enkele maanden manieren om te ontsnappen, waardoor artsen weinig goede opties overhouden. Deze studie stelt een prangende vraag: als darmtumoren niet langer op cetuximab reageren, is er dan een ander zwak punt dat nieuwe geneesmiddelen kunnen benutten om de kankercellen te doen sterven?
Wanneer een gerichte therapie ophoudt te werken
Cetuximab werkt door een oppervlakte-antenne op kankercellen te blokkeren, de epidermale groeifactorreceptor (EGFR), die hun groei aanstuurt. Het team maakte een laboratoriummodel van resistentie door een gevoelige colorectale kankercellijn (LIM1215) gedurende zes maanden bloot te stellen aan geleidelijk toenemende doses cetuximab. Er ontstonden twee onafhankelijk ontwikkelde resistente celpopulaties die bleven groeien zelfs bij hoge medicijnconcentraties, maar er — wanneer het middel werd verwijderd — net zo gezond en snelgroeiend uitzagen als de oorspronkelijke cellen. Belangrijk is dat de resistente cellen het doelwit van het middel nog steeds op hun oppervlak droegen en cetuximab er nog steeds aan kon binden, wat suggereert dat de kanker de receptor niet simpelweg ‘verborgen’ of veranderd had.
Resistente cellen leiden groeisignalen om
Om te begrijpen hoe de cellen cetuximab omzeilden, onderzochten de onderzoekers cruciale groeipaden binnen de cel. Bij de oudercellen dempte cetuximab normaal gesproken het MAPK-pad, een belangrijke motor van celdeling. Bij de resistente cellen bleef de MAPK-activiteit hoog, zelfs wanneer EGFR werd geblokkeerd, wat aantoont dat het groeisignaal losgekoppeld was van de oorspronkelijke receptor. Sequencing van cel-RNA onthulde nieuwe activerende mutaties in een ander RAS-gen, HRAS, in subpopulaties van de resistente cellen, maar niet in de gebruikelijkere verdachten zoals KRAS, NRAS of BRAF. Pogingen om deze omgeleide signalering uit te schakelen met een MEK-remmer (die stroomafwaarts van RAS werkt) verminderden de groei slechts beperkt. Dit onderstreepte dat het, in plaats van elke nieuwe mutatie na te jagen, effectiever kan zijn om het levens- of doodsmechanisme van de cel aan te vallen dat bij verschillende resistente klonen gemeenschappelijk is. 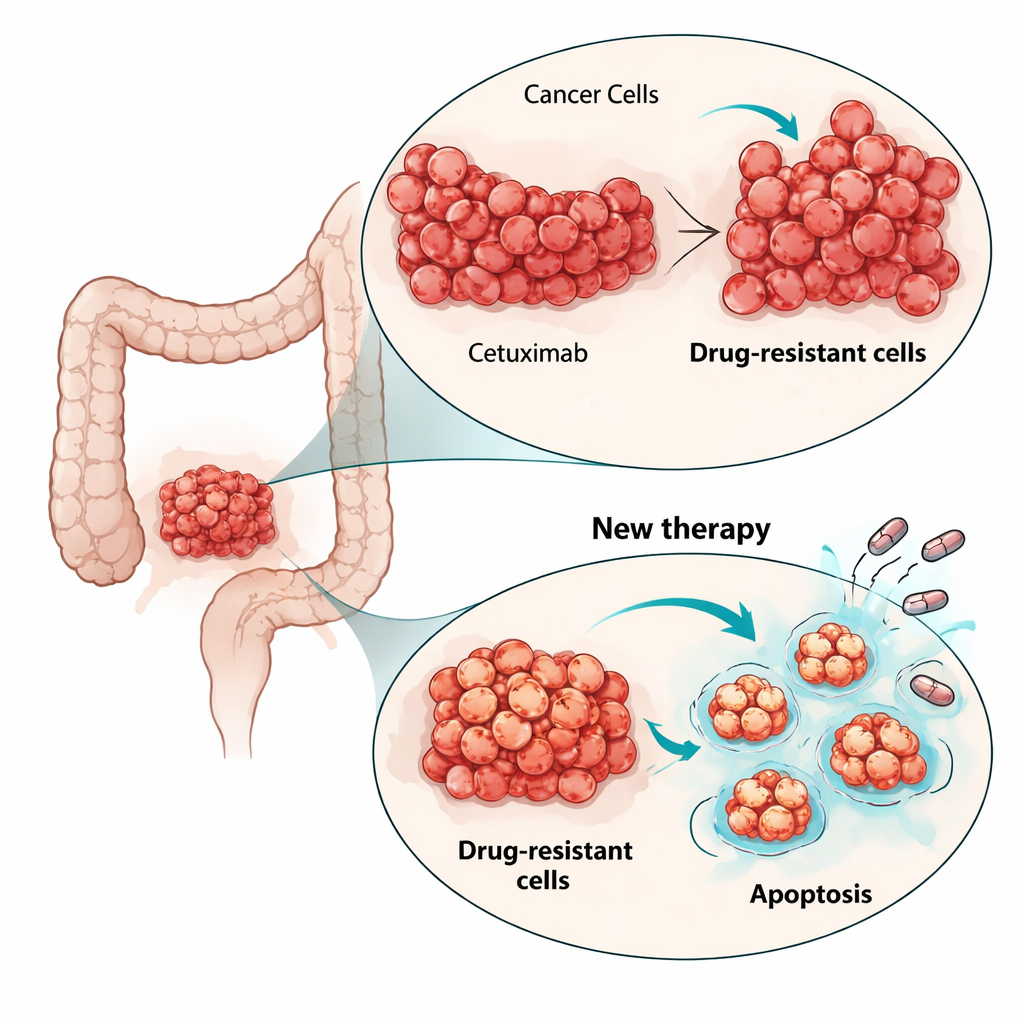
Kanker raken in zijn ademhalingssysteem
De wetenschappers richtten hun aandacht op apoptose, het ingebouwde celsuïcidale programma dat kankers vaak onderdrukken. Genexpressieanalyse toonde aan dat apoptose-gerelateerde paden veranderd waren in de resistente cellen. In het bijzonder was het anti-dood-eiwit BCL-xL verhoogd in één resistente populatie en licht verhoogd in de andere, terwijl een ander overlevingsproteïne, MCL-1, ook aanwezig was. Het team testte kleine molecuulmiddelen genaamd BH3-mimetica die ontworpen zijn om deze overlevingsproteïnen te blokkeren en zo het doodsmechanisme vrij te maken. In tweedimensionale celkweken waren alle drie celijnen — ouderlijk en resistent — gevoelig voor middelen die BCL-xL of MCL-1 blokkeren, maar opvallend was dat lagere doses de cetuximab-resistente cellen effectiever doodden. Het toevoegen van een lage dosis van de proteasoomremmer bortezomib, die helpt pro-doodsignalen te accumuleren, versterkte de celdood verder, vooral in combinatie met de MCL-1-remmer.
Van platte schaaltjes naar 3D-mini-tumoren en patiëntweefsel
Aangezien vlakke cellagen tumoren in het lichaam niet volledig nabootsen, kweekte het team de cellen vervolgens als driedimensionale sferoïden ingebed in een gel, wat beter de architectuur en de uitdagingen van medicijndiffusie in echte tumoren weerspiegelt. Ook hier verminderde blokkade van BCL-xL of MCL-1 de levensvatbaarheid van sferoïden, en het combineren van deze middelen met bortezomib leidde tot dramatische dalingen in metabole activiteit en duidelijke tekenen van celdood. Om te testen of deze kwetsbaarheid ook in realistischer menselijk tumormateriaal bestaat, gebruikten ze dunne plakjes van cetuximab-resistente colorectale kankers gekweekt in muizen uit patiënttumoren (patient-derived xenografts). Deze modellen waren allemaal KRAS wild-type zoals de oorspronkelijke LIM1215-cellen, maar droegen diverse extra mutaties, onder andere in BRAF en TP53, wat de genetische variatie weerspiegelt die in de kliniek wordt gezien. 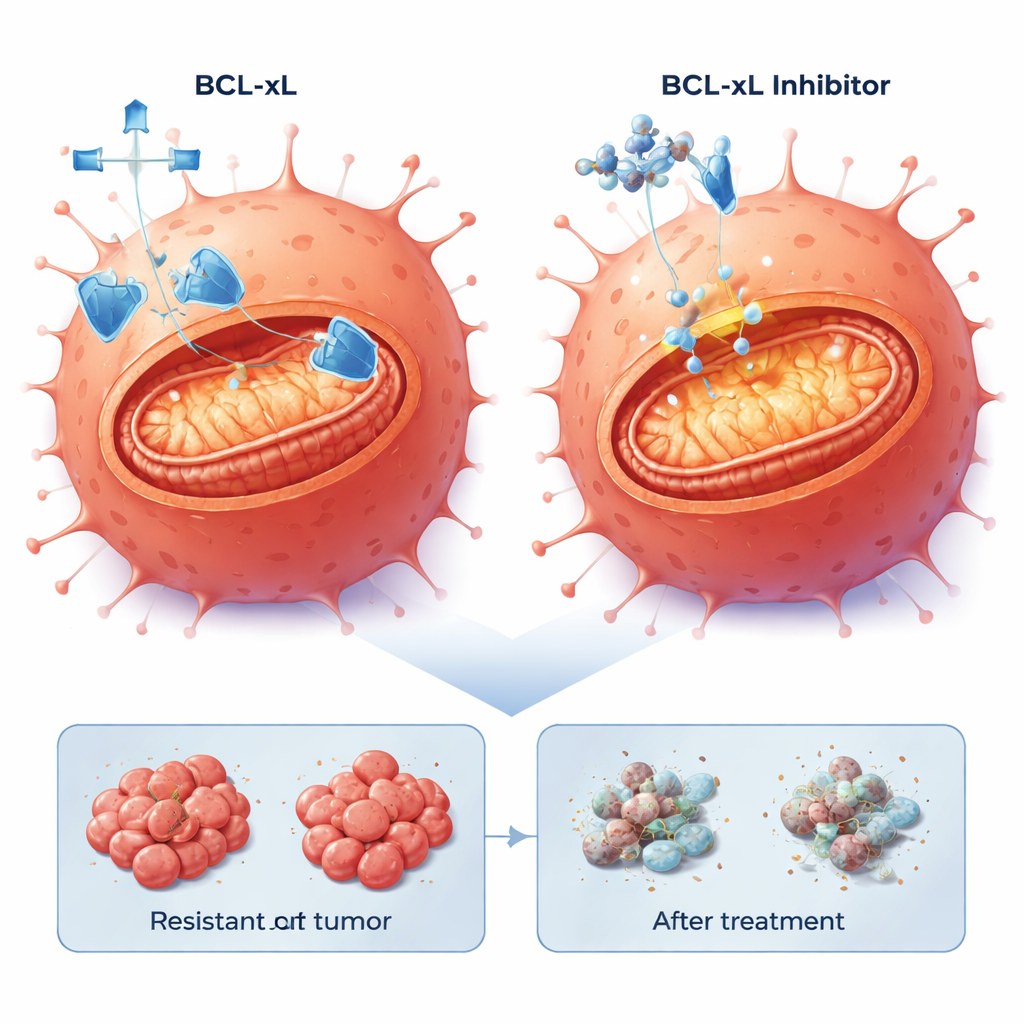
BCL-xL-richting werkt bij diverse resistente tumoren
In deze patiënt-afgeleide tumorglazuurplakjes veroorzaakte de combinatie van een BCL-xL-remmer met lage dosis bortezomib consequent robuuste celdood in 20–40% van de tumorcellen over vier verschillende modellen, waaronder modellen met agressieve BRAF-mutaties. Ter vergelijking: blokkade van MCL-1 met bortezomib gaf sterke effecten alleen in een subset van tumoren. Belangrijk is dat het vermogen van resistente cellen om apoptose te ondergaan behouden bleef: zodra het BCL-xL-veiligheidsnet was verwijderd, kon het interne doodsprogramma nog steeds worden geactiveerd, ongeacht de specifieke genetische route die de tumor had genomen om cetuximab te ontwijken.
Wat dit betekent voor patiënten
Voor mensen van wie de colorectale kanker niet meer op cetuximab reageert, biedt deze studie voorzichtige optimisme. Het suggereert dat zelfs nadat tumoren resistent zijn geworden tegen EGFR-gerichte therapie, veel kankercellen nog steeds klaarstaan om te sterven als een sleutelfactor voor overleving, BCL-xL, wordt geblokkeerd. Hoewel BCL-xL-remmers bijwerkingen kunnen hebben, met name op bloedplaatjes, wijst dit werk op combinaties en dosisoptimalisatie-strategieën die toxiciteit kunnen beperken terwijl ze een gemeenschappelijke achillespees van moeilijk behandelbare tumoren benutten. In de toekomst zouden geneesmiddelen die BCL-xL uitschakelen de ruggengraat kunnen vormen van nieuwe tweedelijnsbehandelingen voor cetuximab-refractaire colorectale kanker, minder afhankelijk van het voortdurend verschuivende mutatiebeeld van de tumor.
Bronvermelding: Asmanidou, S., Thiel, J., Ekstrom, T.L. et al. BCL-xL as a therapeutic target in cetuximab-refractory colorectal cancer. Cell Death Dis 17, 187 (2026). https://doi.org/10.1038/s41419-026-08434-5
Trefwoorden: colorectale kanker, drugresistentie, cetuximab, BCL-xL-remming, apoptose