Clear Sky Science · nl
LAP2α stimuleert borsttumorvorming door replicatiestress te verminderen
Waarom dit belangrijk is voor borstkanker
Borsttumoren groeien deels omdat kankercellen manieren vinden om constant aanwezige stress tijdens het kopiëren van hun DNA te overleven. Deze studie onthult hoe een minder bekend eiwit, LAP2α genoemd, borstkankercellen helpt hun DNA tijdens replicatie te beschermen, waardoor tumorgroei wordt bevorderd en kankers moeilijker te behandelen zijn. Inzicht in dit verborgen ondersteuningssysteem suggereert nieuwe manieren om tumoren te verzwakken en de werking van bestaande medicijnen te verbeteren.
Een verborgen helper in de kernen van tumorcellen
Elke keer dat een cel deelt, moet het zijn DNA nauwkeurig kopiëren. Bij kankercellen staat dat proces onder bijzondere druk: groeisignalen staan continu aan en het replicatiemechanisme wordt tot het uiterste gedreven. Deze druk, bekend als replicatiestress, laat gedeelten enkelstrengs DNA achter die snel moeten worden omhuld en gestabiliseerd door een eiwitcomplex genaamd RPA. De auteurs ontdekten eerder dat LAP2α, een eiwit verbonden aan het interne skelet van de kern, RPA kan binden en helpt om RPA naar beschadigd DNA te brengen. In het huidige werk onderzochten ze of deze LAP2α–RPA-partnerschap daadwerkelijk de ontwikkeling van borstkanker aanjaagt en de reactie van tumoren op behandeling beïnvloedt.
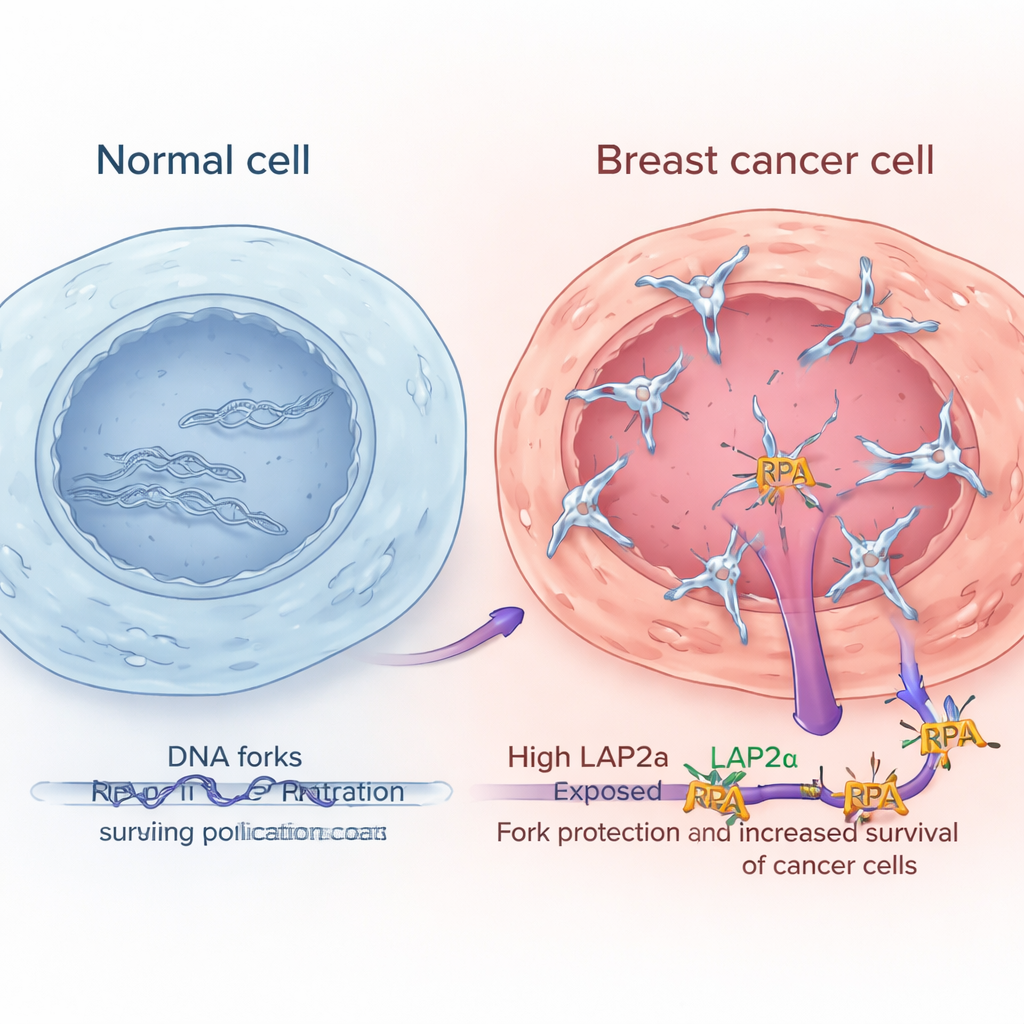
Hoge LAP2α-waarden duiden op agressievere borsttumoren
Door grote, openbare genexpressie-datasets te analyseren en tumormonsters onder de microscoop te bekijken, lieten de onderzoekers zien dat LAP2α consequent hoger is in borstkankerpatiënten dan in omliggend normaal borstweefsel. De concentratie neemt toe met tumorgraad: meer afwijkende en agressieve kankers hebben doorgaans meer LAP2α. Dit patroon trad op bij meerdere belangrijke borstkankersubtypes, waaronder hormoonreceptor-positieve, HER2-rijke en triple-negatieve tumoren. Belangrijk voor patiënten was dat degenen met tumoren met hoge LAP2α-scores geneigd waren slechter te overleven. De kerncomponenten van RPA zelf toonden daarentegen geen vergelijkbare veranderingen of duidelijke verbanden met uitkomst, wat suggereert dat het de versterkte functie van LAP2α is — en niet simpelweg meer RPA — die kankercellen beter helpt omgaan met replicatiestress.
Uitschakelen van LAP2α vertraagt tumoren en legt kwetsbaarheden bloot
Om verder te gaan dan correlaties gebruikte het team muismodellen van borstkanker waarin LAP2α selectief kon worden verwijderd. Nadat mammatumoren zich hadden gevormd, leidde het genetisch uitschakelen van LAP2α tot vertraagde tumorgroei en verlengde het de overleving van de dieren. Tumorcellen zonder LAP2α deelden minder en vertoonden meer tekenen van DNA-schade, zoals verhoogde kleuring voor DNA-breukmarkers en verminderde RPA-bedekking van DNA. Toen deze LAP2α-deficiënte tumorcellen in nieuwe muizen werden getransplanteerd, vormden ze opnieuw kleinere tumoren en waren ze gevoeliger voor DNA-beschadigende chemotherapie, waaronder het platinummiddel cisplatine en een PARP-remmer. Vergelijkbare experimenten in menselijke borstkankercellijnen bevestigden dat vermindering van LAP2α cellen gevoeliger maakte voor meerdere genotoxische geneesmiddelen, terwijl het herstellen van normaal LAP2α — maar niet een mutante vorm die RPA niet kan binden — zowel DNA-bescherming als medicijnresistentie deed terugkeren.
Hoe LAP2α helpt kwetsbare DNA-strengen te beschermen
Om het mechanisme te ontrafelen, reconstrueerden de onderzoekers de DNA-bindingsstappen in proefbuisassays. Ze mengden gezuiverd RPA, enkelstrengs DNA en ofwel normaal LAP2α of een variant die niet met RPA kan interageren. Ze ontdekten dat LAP2α direct de efficiëntie verhoogde waarmee RPA enkelstrengs DNA bedekte en hielp RPA deze kwetsbare regio’s uit te rekken en te stabiliseren, werkend als een laad- of chaperonneerhulp. Wanneer DNA aanwezig was, liet RPA vaak LAP2α los en bond volledig met de enkelstreng, wat aangeeft dat LAP2α geen deel uitmaakt van het uiteindelijke beschermende omhulsel maar RPA aan DNA overhandigt. Zonder een functionele LAP2α–RPA-interactie stortten meer replicatievorken in, hoopten DNA-breuken zich op en stierven kankercellen vaker, vooral wanneer extra schade werd geïnduceerd door chemotherapie.
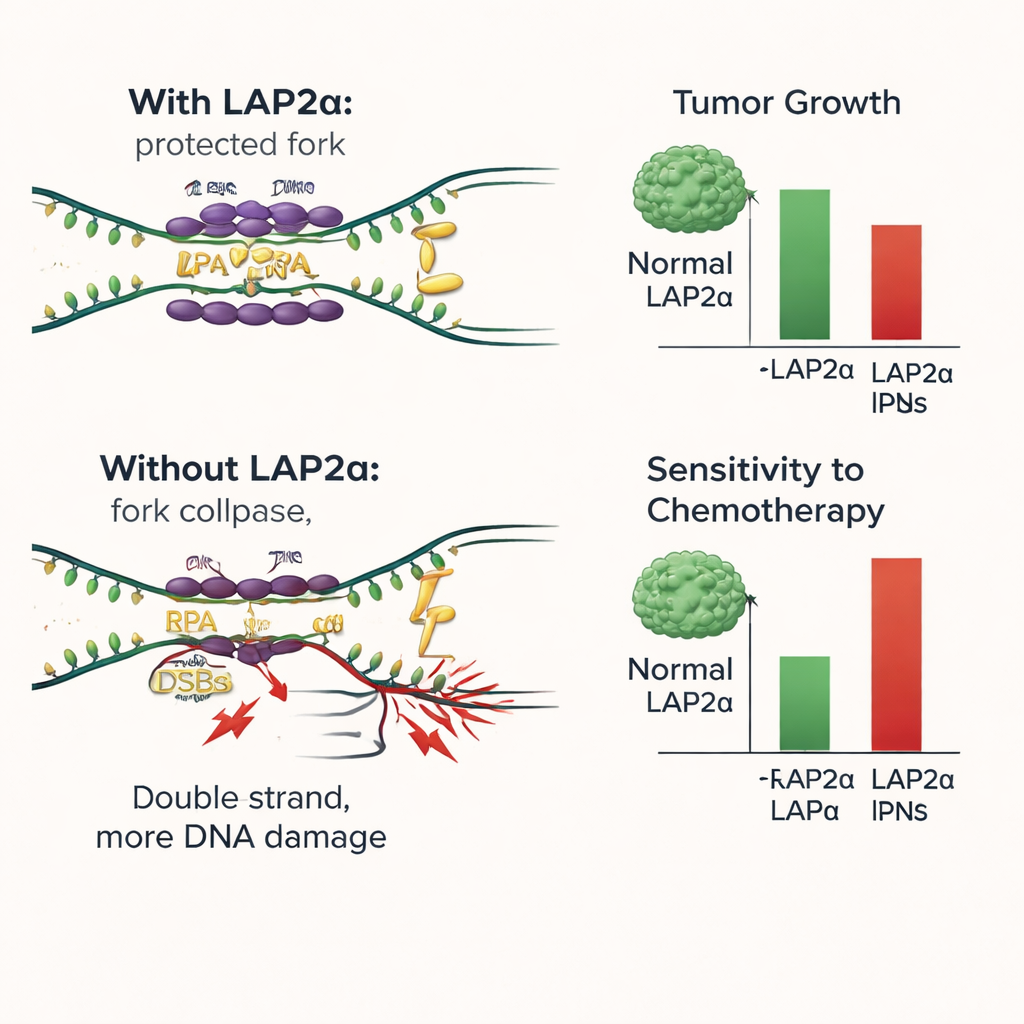
Wat dit betekent voor toekomstige borstkankerbehandeling
Kort gezegd toont deze studie aan dat LAP2α fungeert als een achter-de-schermen assistent die borstkankercellen helpt de spanning van DNA-replicatie te doorstaan. Door RPA efficiënt op kwetsbaar DNA te laden, vermindert LAP2α schade en ondersteunt het aanhoudende tumorgroei. Het verwijderen of uitschakelen van LAP2α kantelt de schaal: DNA-schade stapelt zich op, cellen stoppen met delen en conventionele middelen die DNA aanvallen worden effectiever. Deze bevindingen suggereren dat LAP2α als een merker van slechtere prognose kan dienen en als een nieuw therapeutisch doelwit. Middelen die LAP2α blokkeren of de binding met RPA verstoren, zouden bestaande behandelingen zoals platinummiddelen en PARP-remmers kunnen versterken, vooral in tumoren die sterk steunen op dit stress-bufferende systeem.
Bronvermelding: Ma, Y., Qin, Y., Bao, P. et al. LAP2α drives breast tumorigenesis by mitigating replication stress. Cell Death Dis 17, 201 (2026). https://doi.org/10.1038/s41419-026-08433-6
Trefwoorden: borstkanker, DNA-replicatiestress, LAP2 alfa, replicatie-eiwit A, gevoeligheid voor chemotherapie