Clear Sky Science · nl
Gerichte remming van glycerofosfolipidesynthese overwint chemoresistentie veroorzaakt door verlies van SLFN11 bij Ewing-sarcoom
Waarom dit onderzoek belangrijk is voor kinderkanker
Ewing-sarcoom is een zeldzame maar agressieve kanker die vooral kinderen en tieners treft. Veel patiënten reageren aanvankelijk goed op chemotherapie, maar voor wie de kanker terugkomt, schieten de huidige behandelingen vaak tekort. Deze studie stelt een urgente vraag: wanneer Ewing-sarcoomcellen resistent worden tegen chemotherapie, welke veranderingen in de cellen helpen hen te overleven — en kunnen die veranderingen worden omgezet in nieuwe kwetsbaarheden die artsen kunnen benutten?
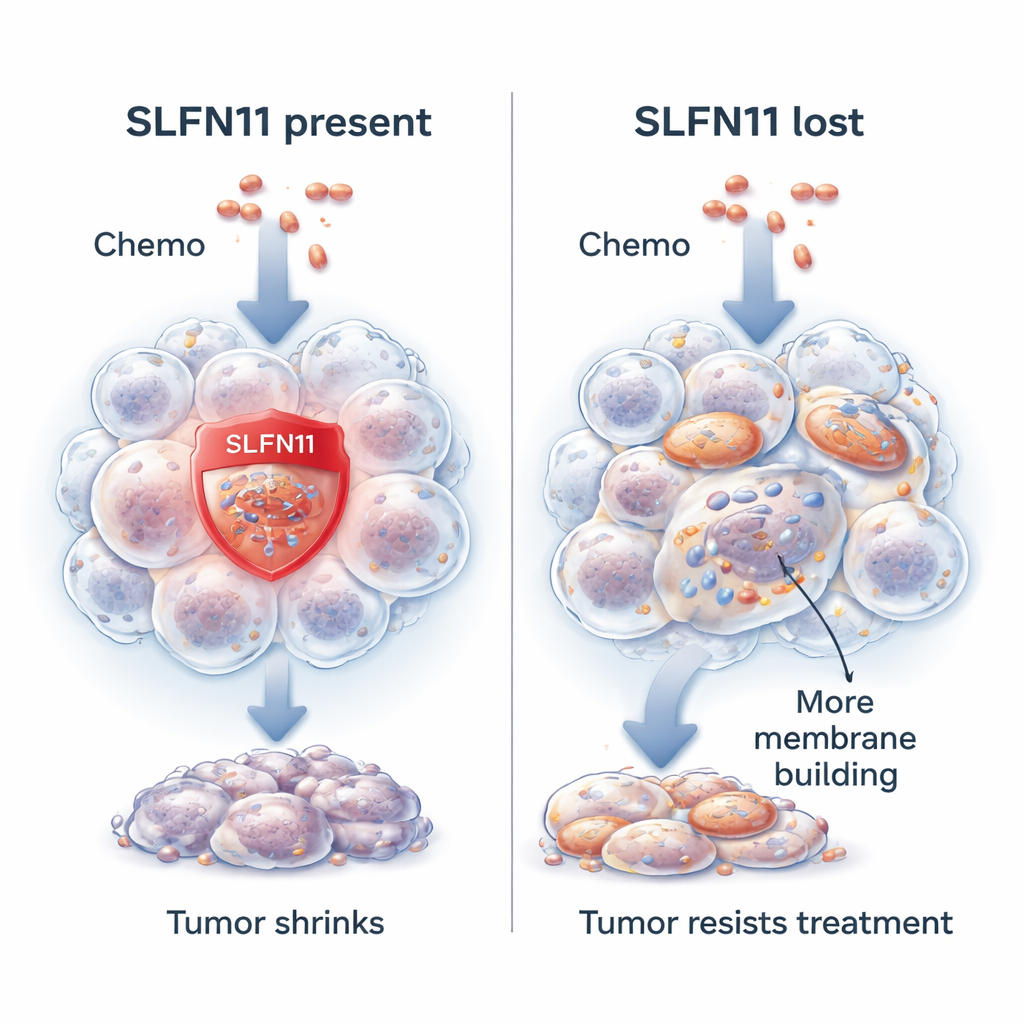
Een gen dat kankercellen makkelijker te doden maakt
De onderzoekers richten zich op een gen genaamd SLFN11. In veel Ewing-tumoren is SLFN11 sterk actief en maakt het de kankercellen veel gevoeliger voor middelen die DNA beschadigen, het genetische bestand van de cel. Wanneer deze medicijnen worden toegediend, helpt SLFN11 de DNA-herstelprocessen stil te leggen en duwt het de kankercel richting celdood. Patiënten waarvan de tumoren hogere SLFN11-niveaus hebben, blijken doorgaans langer te overleven en beter op behandeling te reageren. Ongeveer één op de tien tumoren heeft echter van meet af aan weinig of geen SLFN11 of verliest het gen tijdens de behandeling. In dat geval is dezelfde chemotherapie veel minder effectief, terwijl de kankercellen nog steeds in staat zijn te groeien.
Hoe kankercellen hun brandstof- en vetgebruik herschakelen
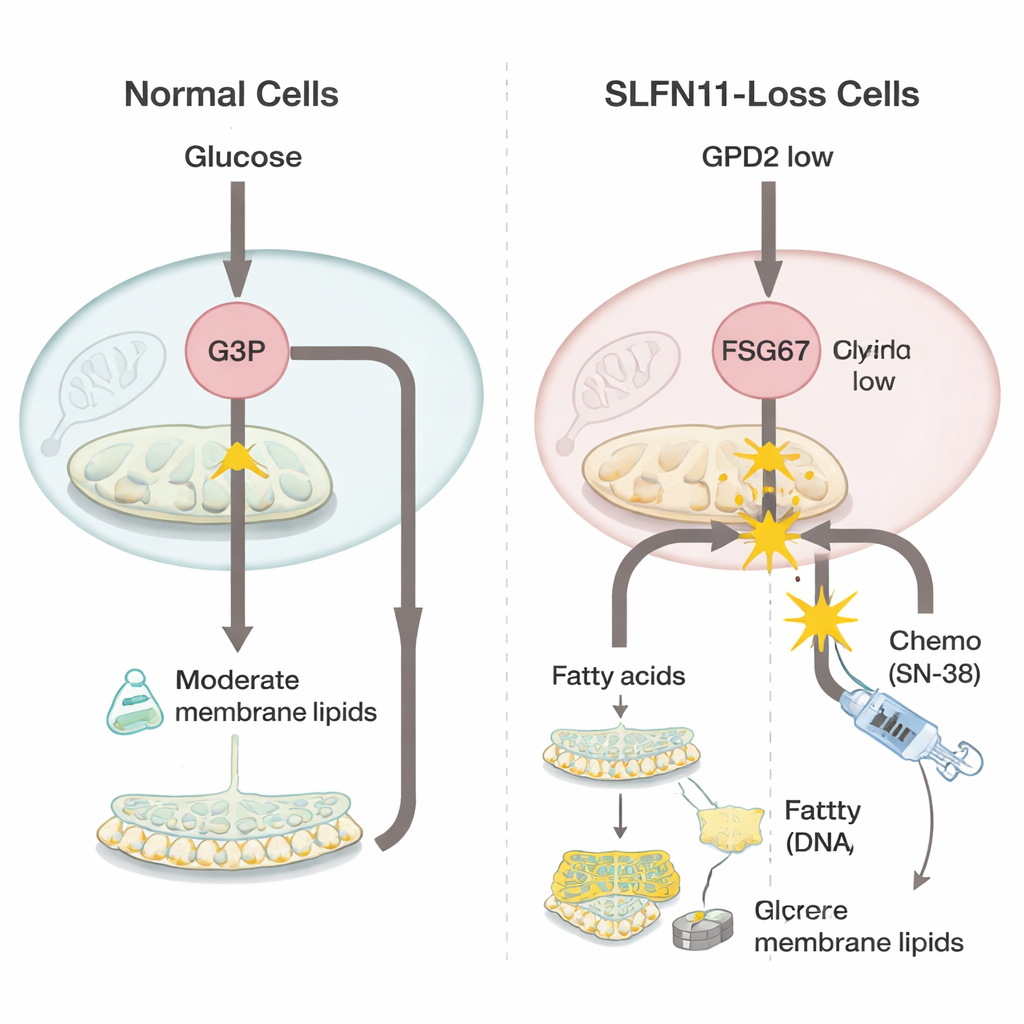
Om te begrijpen wat er verandert bij verlies van SLFN11, vergeleek het team Ewing-sarcoomcellen met en zonder dit gen met behulp van krachtige ‘omics’-methoden die duizenden genen en kleine moleculen tegelijk meten. Ze ontdekten dat cellen zonder SLFN11 een enzym in hun mitochondriën naar beneden bijstellen dat GPD2 heet, dat normaal glycerol-3-fosfaat helpt verbranden als onderdeel van de energieproductie. Wanneer GPD2 wordt verminderd, hoopt glycerol-3-fosfaat zich op. In plaats van verloren te gaan, wordt dit extra bouwsteenmateriaal omgeleid naar de productie van meer vetachtige moleculen die celmembranen vormen, een groep die bekendstaat als glycerofosfolipiden. De cellen vertoonden ook aanwijzingen voor de productie van meer flexibele, onverzadigde vetten, wat snelgroeiende tumoren kan helpen zich aan stress aan te passen.
Een overlevingstruc veranderen in een zwakke plek
Aangezien deze SLFN11-deficiënte cellen sterker afhankelijk leken van membraanopbouw, testten de wetenschappers of het blokkeren van dit proces de gevoeligheid voor chemotherapie kon herstellen. Ze gebruikten een verbinding genaamd FSG67, die een sleutelstap in de productie van glycerofosfolipiden remt. Op zichzelf was het standaard DNA-schadigende middel SN-38 veel minder krachtig geworden in SLFN11-deficiënte cellen, wat het klinische probleem van resistentie weerspiegelt. Maar wanneer SN-38 werd gecombineerd met FSG67, werden de eerder resistente cellen veel harder geraakt en werkten de twee middelen samen beter dan op grond van hun individuele effecten verwacht zou worden. Daarentegen bood toevoeging van FSG67 aan cellen die nog SLFN11 hadden en al zeer gevoelig waren voor SN-38 weinig extra voordeel en kon het zelfs licht contraproductief zijn. Dit patroon suggereert dat de nieuw ontstane afhankelijkheid van vet- en membraanproductie specifiek is voor de resistente, SLFN11-lage toestand.
Een potentiële niet-invasieve indicator van moeilijk behandelbare tumoren
Vervolgens vroegen de onderzoekers of deze metabole herschakeling in echte tumoren kon worden gedetecteerd, niet alleen in cellen op een kweekplaat. Ze lieten Ewing-sarcoomtumoren groeien in muizen, met of zonder SLFN11, en gebruikten nucleaire magnetische resonantie (NMR) om de chemische samenstelling van de tumorextracten te onderzoeken. Tumoren zonder SLFN11 vertoonden een hogere verhouding van twee choline-bevattende moleculen die samenhangen met membraanomzetting: phosphocholine en glycerophosphocholine. Een hoge phosphocholine/glycerophosphocholine-verhouding is bij andere kankers in verband gebracht met agressiever gedrag en slechtere behandelrespons. Omdat cholinesignalen met geavanceerde beeldvormingstechnieken kunnen worden gemeten, zou dit soort verschuiving mogelijk ooit kunnen dienen als een niet-invasieve marker om Ewing-sarcoomtumoren te signaleren die deze resistente, membraanopbouwende modus hebben aangenomen.
Wat dit kan betekenen voor toekomstige behandelingen
Al met al laat de studie zien dat wanneer Ewing-sarcoomcellen SLFN11 verliezen en minder gevoelig worden voor DNA-schadigende chemotherapie, ze dat compenseren door hun stofwisseling om te schakelen naar de productie van meer membraanvetten. Deze verschuiving helpt de cellen niet alleen te overleven; ze creëert ook een nieuwe achilleshiel. Het blokkeren van glycerofosfolipidesynthese met een middel zoals FSG67 kan de dodelijke werking van chemotherapie bij deze resistente cellen gedeeltelijk herstellen. Hoewel FSG67 zelf nog geen klinisch geneesmiddel is, wijst dit werk op een strategie waarbij artsen mogelijk tumoren van patiënten op basis van SLFN11-status en metabole kenmerken kunnen typeren en DNA-schadigende therapieën kunnen combineren met gerichte remmers van vet- en membraansynthese om resistentie te overwinnen.
Bronvermelding: Chakraborty, K., Burman, R., Satheesh, S. et al. Targeting glycerophospholipid biosynthesis overcomes chemoresistance driven by SLFN11 loss in Ewing sarcoma. Cell Death Dis 17, 190 (2026). https://doi.org/10.1038/s41419-026-08432-7
Trefwoorden: Ewing-sarcoom, chemoresistentie, SLFN11, kankerstofwisseling, lipsynthese