Clear Sky Science · nl
Het richten op hypoxische exosomale IGFBP2 doorbreekt CD47-gemedieerde immuunontwijking bij glioblastoom
Waarom het uithongeren van tumoren van zuurstof averechts kan werken
Artsen weten al lang dat glioblastoom, een dodelijke hersenkanker, vaak groeit in gebieden waar weinig zuurstof beschikbaar is. Deze hypoxische zones maken de tumor moeilijker te behandelen. Deze studie laat zien hoe lage zuurstofniveaus kankercellen helpen zich te verbergen voor het immuunsysteem en suggereert een nieuwe combinatietherapie die ze makkelijker voor het lichaam te bestrijden zou kunnen maken.
Een dodelijke hersentumor die onze verdediging omzeilt
Glioblastoom is de meest agressieve veelvoorkomende hersentumor bij volwassenen, met een mediane overleving van slechts enkele maanden. Hoewel immuuncellen deze tumoren binnendringen, ontsnappen kankercellen vaak aan vernietiging. Een belangrijke ontsnappingsroute is een oppervlakte-eiwit genaamd CD47, soms het "eet-me-niet"-signaal genoemd, dat nabijgelegen immuuncellen zoals macrofagen vertelt de kankercel niet te verwijderen. Middelen die CD47 blokkeren worden al getest, maar de resultaten bij solide tumoren zoals glioblastoom zijn wisselend, wat suggereert dat andere factoren in de tumoromgeving deze therapieën ondermijnen.
Hypoxische zones en kleine kankerpakketjes
Met behulp van single-cell RNA-sequencing brachten de onderzoekers duizenden cellen uit verschillende regio’s van glioblastoommonsters in kaart en vergeleken ze de zuurstofarme kern van de tumor met de buitenrand. Ze vonden een bijzonder agressief celtype in de hypoxische kern, genoemd mesenchymaal-achtige GBM-cellen, dat sterk CD47 en een eiwit genaamd IGFBP2 tot expressie bracht. Tegelijk ontdekten ze dat deze kernen grote aantallen nanoschaalblaasjes, exosomen genoemd, vrijgaven die IGFBP2 op hun oppervlak droegen. Omdat exosomen door de hersenen en zelfs in de bloedbaan kunnen reizen, kunnen ze signalen ver verspreiden voorbij hun plek van herkomst. 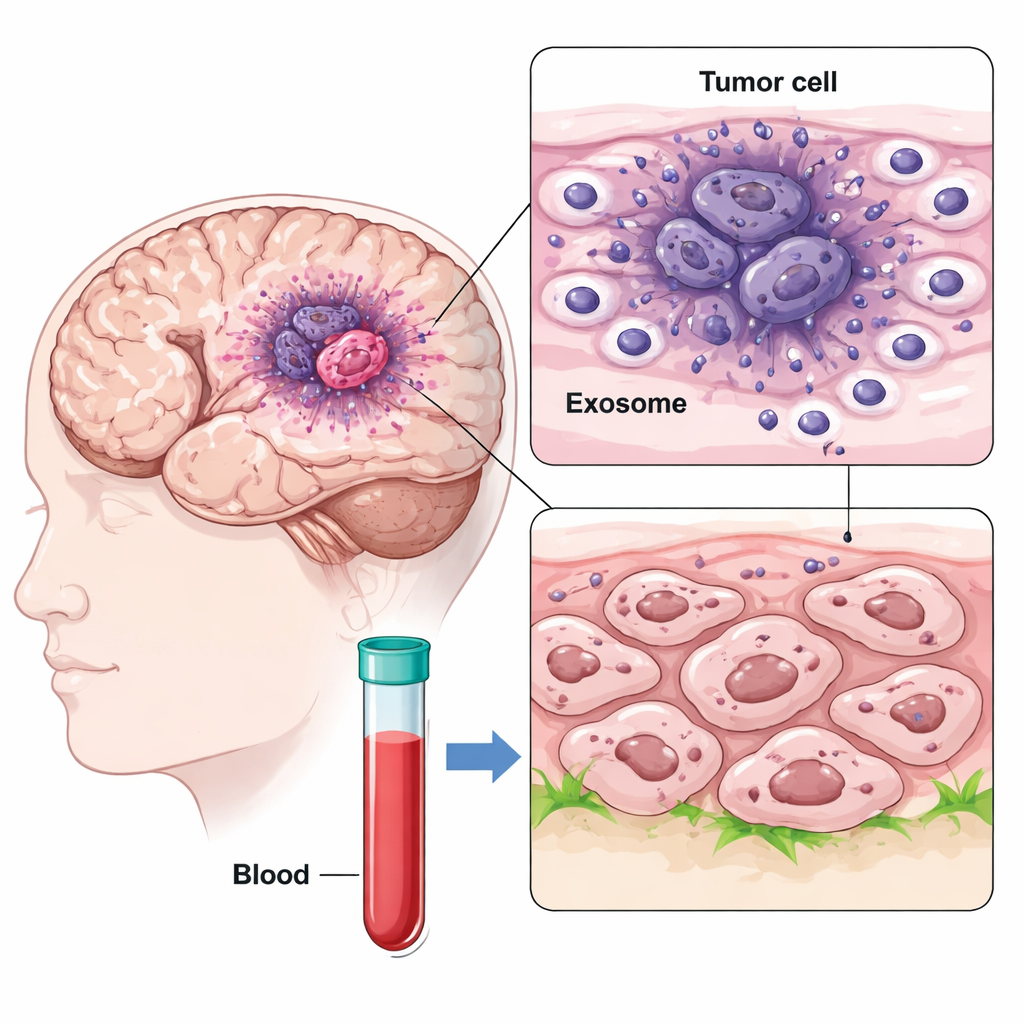
Hoe een partner-eiwit het "eet-me-niet"-signaal versterkt
Het team onderzocht vervolgens wat IGFBP2 precies doet. Ze toonden aan dat onder lage zuurstof een hypoxiesensor-eiwit genaamd HIF-2α het IGFBP2-gen in tumorcellen activeert. IGFBP2 bindt vervolgens aan specifieke receptoren, integrines genoemd, op het oppervlak van exosomen en bekleedt hun buitenmembraan. Wanneer deze met IGFBP2 gecoate exosomen fuseren met andere tumorcellen, activeren ze een signaleringsketen binnen de cel die eiwitten als FAK en STAT3 omvat. Deze cascade verhoogt uiteindelijk de hoeveelheid CD47 op het tumorceloppervlak, waardoor het "eet-me-niet"-signaal naar macrofagen wordt versterkt en kankercellen nog beter beschermd worden tegen immuunaanvallen. 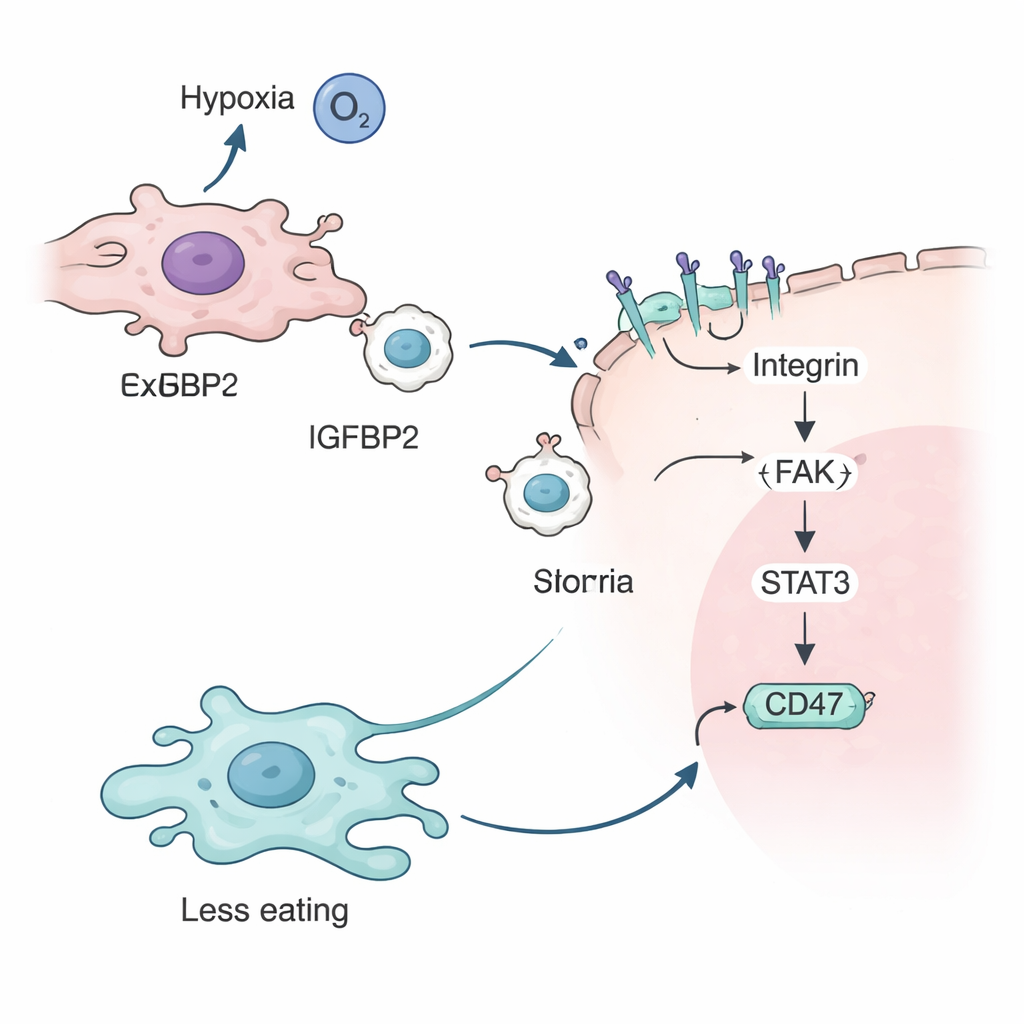
Bewijs uit patiëntmonsters en diermodellen
Om deze laboratoriumbevindingen aan de klinische realiteit te koppelen, onderzochten de onderzoekers tumorweefsel en bloed van mensen met glioom. Ze vonden dat IGFBP2-niveaus hoger waren in zowel tumoren als bloedexosomen van patiënten met een gevorderdere ziekte, wat suggereert dat IGFBP2-positieve exosomen als bloedgerichte marker voor tumorgraad kunnen dienen. In muismodellen maakte het verlagen van IGFBP2 in glioblastoomcellen ze vatbaarder voor fagocytose door macrofagen, vertraagde het tumorprogressie en verlengde het de overleving. Omgekeerd verhoogde het toedienen van extra IGFBP2-rijke exosomen CD47-niveaus, verminderde het immuunceleten en versnelde het de tumorontwikkeling.
Een veelbelovende combinatiestrategie voor therapie
Ten slotte testte het team of het blokkeren van IGFBP2 CD47-gerichte therapie effectiever kon maken. Bij muizen met hersentumoren leidde behandeling met antilichamen tegen zowel IGFBP2 als CD47 tot sterkere macrofaagactiviteit, kleinere tumoren en langere overleving dan elke behandeling op zichzelf. Door het hypoxie-gestuurde IGFBP2-signaal af te knijpen en tegelijk het CD47 "eet-me-niet"-signaal direct te blokkeren, viel deze gecombineerde therapie de immuuncamouflage van de tumor van twee kanten aan. Voor patiënten suggereren deze bevindingen dat het meten van IGFBP2 in bloedexosomen kan helpen degenen te identificeren die het meest waarschijnlijk van CD47-gebaseerde immunotherapie profiteren, en dat het combineren van IGFBP2- en CD47-remmers een krachtigere strategie tegen glioblastoom kan zijn dan elk middel afzonderlijk.
Bronvermelding: Qi, Y., Zhao, R., Zhang, X. et al. Targeting hypoxic exosomal IGFBP2 overcomes CD47-mediated immune evasion in glioblastoma. Cell Death Dis 17, 192 (2026). https://doi.org/10.1038/s41419-026-08430-9
Trefwoorden: glioblastoom, exosomen, immuunontwijking, CD47, hypoxie