Clear Sky Science · nl
HSPA5 bevordert de stabiliteit van YAP/TAZ onafhankelijk van het Hippo-pad en induceert een proneurale‑naar‑mesenchymale transitie in glioblastoom
Waarom deze studie over hersenkanker ertoe doet
Glioblastoom is een van de dodelijkste vormen van hersenkanker, mede omdat veel tumoren in de loop van de tijd overgaan naar een hardere, meer therapieresistente toestand. Deze studie laat zien hoe een veelvoorkomend stress‑respons‑eiwit, HSPA5, dat proces aanstuurt en tumorbevorderende moleculen langer in leven houdt dan normaal. Inzicht in dit "overlevingstrucje" wijst op nieuwe manieren om glioblastoom minder agressief en gevoeliger voor bestaande therapieën te maken.
Een tumor die van karakter verandert
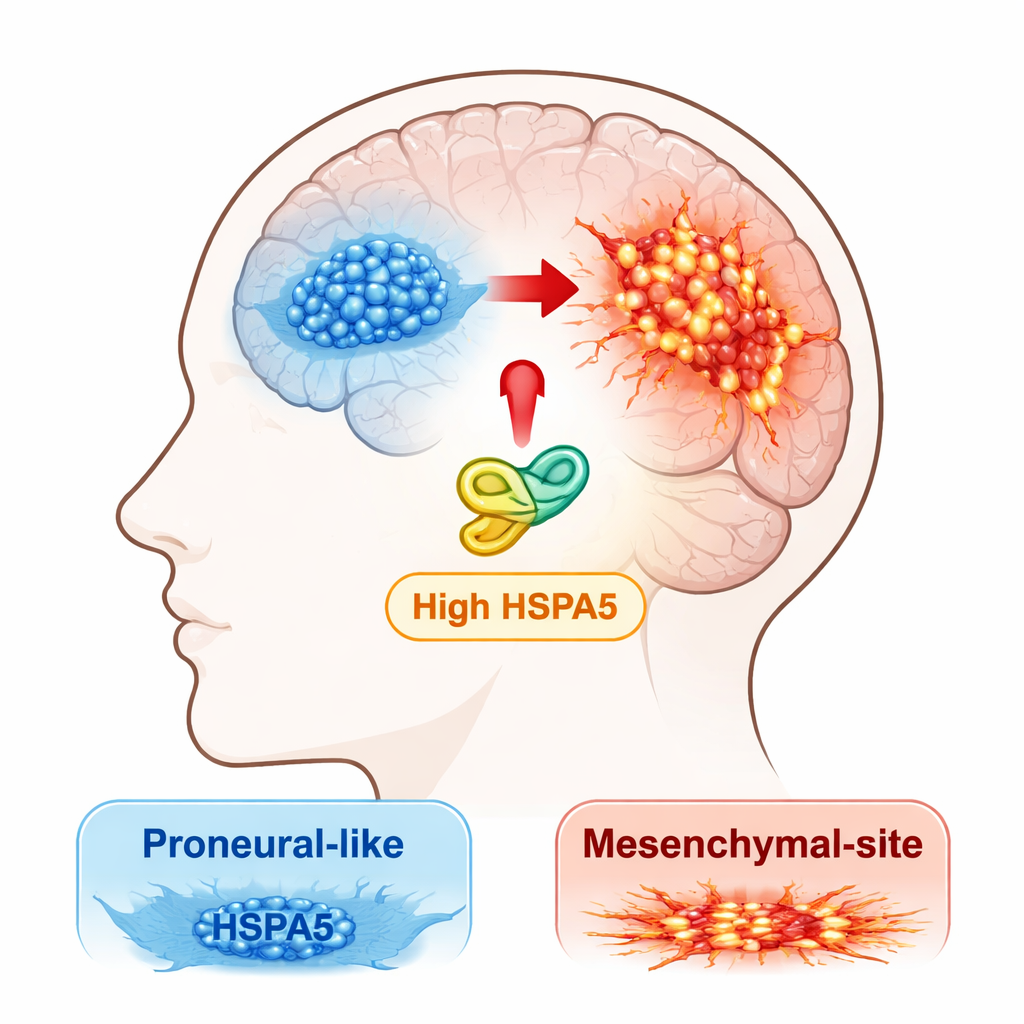
Artsen en onderzoekers erkennen nu dat glioblastoom geen eenduidige ziekte is, maar een mengeling van moleculaire subtypes. Twee belangrijke varianten zijn een “proneurale” vorm, die doorgaans iets minder agressief is, en een “mesenchymale” vorm, die invasiever is, resistenter tegen behandeling en geassocieerd met vroegere terugkeer. Tumoren kunnen evolueren van de proneurale naar de mesenchymale toestand, een proces dat de auteurs proneuraal‑naar‑mesenchymaal transitie (PMT) noemen. Het team ging op zoek naar welke stress‑respons‑eiwitten tumoren mogelijk in deze gevaarlijke richting duwen.
Een stress‑hulpje onder de loep
De onderzoekers begonnen met het doorzoeken van grote openbare kankerdatasets en hun eigen patiëntmonsters op leden van de HSP70‑familie, een groep “chaperonne”‑eiwitten die andere eiwitten helpen vouwen en overleven onder stress. Eén chaperonne, HSPA5, stak er met kop en schouders bovenuit. De activiteit ervan was het hoogst in het mesenchymale subtype van glioblastoom en duidelijk hoger in tumoren dan in normaal hersenweefsel. Patiënten met tumoren die meer HSPA5 bevatten hadden doorgaans een slechtere overleving, wat HSPA5 aanduidt als mogelijke aanjager van agressieve ziekte in plaats van een passieve bijstander.
Cellen dwingen om agressiever te worden
Om te onderzoeken wat HSPA5 daadwerkelijk binnen tumorcellen doet, kweekte het team primaire glioblastoomcellen direct afkomstig van patiënten en splitste ze in proneuraal‑achtige en mesenchymaal‑achtige groepen. Toen ze proneurale cellen dwongen extra HSPA5 te maken, begonnen die cellen zich meer als mesenchymaal te gedragen: ze deelden sneller, migreerden en invadeerden gemakkelijker, en schakelden kenmerkende mesenchymale markers zoals CD44 en c‑MET aan, terwijl proneurale markers zoals SOX2 en OLIG2 werden geremd. Het omgekeerde was ook waar — het verminderen van HSPA5 in mesenchymale cellen dempte hun groei en invasiviteit en duwde ze deels terug naar een minder agressief profiel.
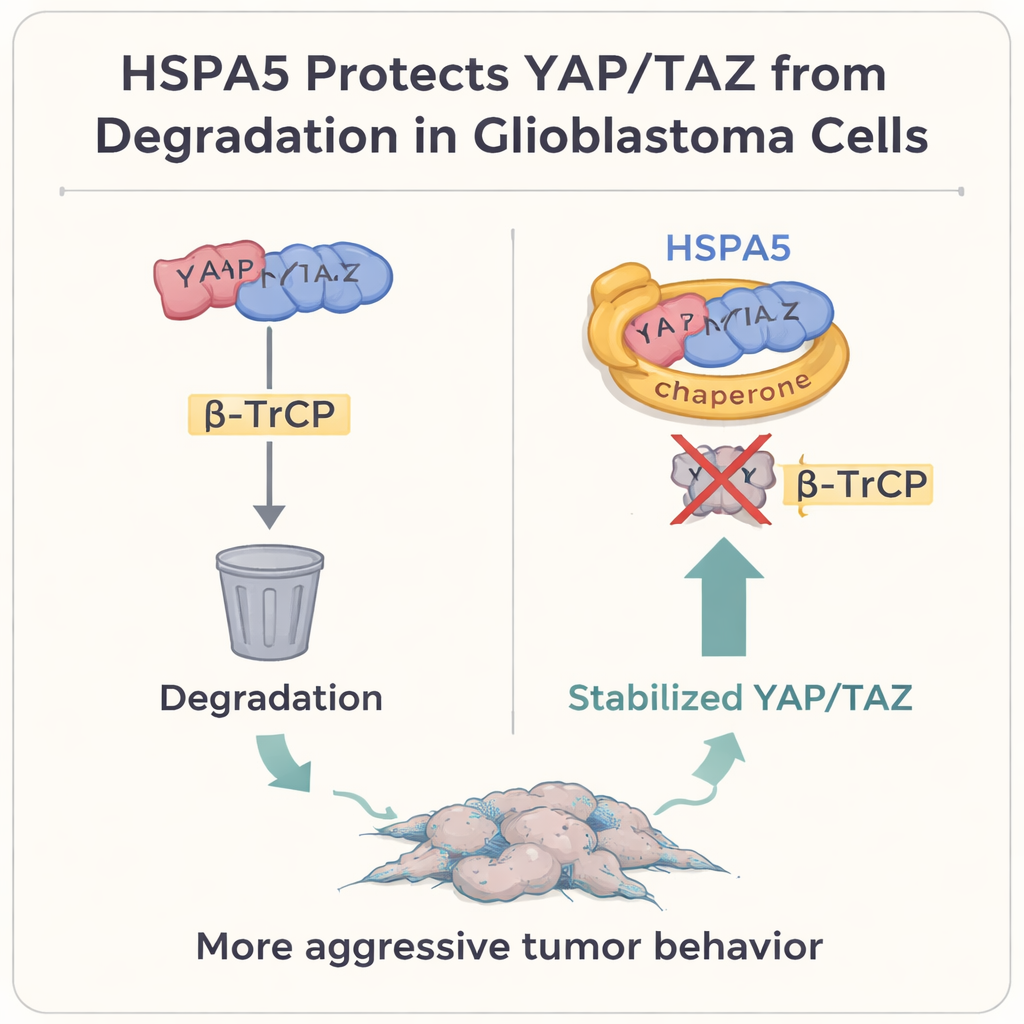
Sleutelgroeischakelaars beschermen tegen de cellulaire vuilnisbak
Dieper gravend richtten de auteurs zich op twee krachtige groeiregulatoren, YAP en TAZ, die centraal staan in het Hippo‑signaalpad. In veel solide tumoren, waaronder glioblastoom, fungeren deze eiwitten als hoofdschakelaars die celgroei, plasticiteit en de mesenchymale toestand bevorderen. Normaal gesproken, wanneer cellen dit programma willen beteugelen, labelen ze YAP en TAZ voor afbraak via een eiwit genaamd β‑TrCP, dat hen naar de ‘‘vuilnisbak’’ van de cel, het proteasoom, begeleidt. De studie laat zien dat HSPA5 fysiek bindt aan YAP en TAZ en daarbij zijn substraatbindende domein als een beschermende handschoen gebruikt. Daardoor blokkeert het de binding van β‑TrCP, voorkomt het ubiquitinering en afbraak van YAP/TAZ, en laat het deze factoren opstapelen in de kern waar ze mesenchymale genen aanzetten, waaronder CD44 en c‑MET zelf.
Van kweekschalen en muizen tot patiënttumoren
Het team bevestigde dit mechanisme op verschillende manieren. Het blokkeren van HSPA5 liet YAP‑ en TAZ‑eiwitten sneller verdwijnen, tenzij het proteasoom chemisch werd geïnactiveerd, en verhoogde de "vuilnislabel"‑signalen op deze eiwitten. Het heractiveren van YAP en TAZ herstelde het verlies aan groei en invasie dat optrad bij HSPA5‑verlaging, terwijl het stilleggen van YAP/TAZ de pro‑tumoreffecten van HSPA5‑overexpressie uitschakelde. In muismodellen waarin menselijke glioblastoomcellen in de hersenen werden geïmplanteerd, groeiden tumoren met veel HSPA5 sneller en doodden ze de dieren eerder; het verlagen van HSPA5, of het onderbreken van zijn ondersteuning van YAP/TAZ, vertraagde de groei en verlengde de overleving. Tot slot lieten overeenkomstige menselijke monsters van dezelfde patiënten, genomen vóór en na recidief, zien dat terugkerende, meer mesenchymale tumoren hogere niveaus van HSPA5, YAP, TAZ en mesenchymale markers hadden dan de oorspronkelijke proneuraal‑achtige tumoren.
Wat dit betekent voor toekomstige behandelingen van hersenkanker
In eenvoudige bewoordingen suggereert dit werk dat glioblastoomcellen een stress‑respons‑helper, HSPA5, exploiteren om cruciale groeischakelaars (YAP en TAZ) te beschermen tegen afbraak. Die bescherming helpt tumoren om over te schakelen naar en vast te houden aan een agressievere, therapieresistente identiteit. Omdat er al kleine‑molecuulremmers van HSPA5 bestaan en tumorcellen mogelijk meer afhankelijk zijn van deze chaperonne dan normale cellen, biedt de HSPA5–YAP/TAZ‑as een aantrekkelijk nieuw doelwit. Therapieën die dit beschermende schild verzwakken, zouden glioblastoomcellen minder adaptief, minder invasief en kwetsbaarder voor standaardbehandelingen zoals chemotherapie en radiotherapie kunnen maken.
Bronvermelding: Gui, S., Yu, W., Song, Z. et al. HSPA5 promotes YAP/TAZ stability independently of the Hippo pathway and induces proneural-to-mesenchymal transition in glioblastoma. Cell Death Dis 17, 208 (2026). https://doi.org/10.1038/s41419-026-08428-3
Trefwoorden: glioblastoom, HSPA5, YAP/TAZ, tumorplasticiteit, mesenchymale transitie