Clear Sky Science · nl
p16-gemedieerde G0/G1-celcyclusarrest leidt tot SASP en fibrose bij Fuchs endotheliale corneale dystrofie
Waarom deze oogaandoening van belang is
Naarmate mensen ouder worden, is een van de minder bekende bedreigingen voor het gezichtsvermogen een aandoening genaamd Fuchs endotheliale corneale dystrofie (FECD), die geleidelijk het normaal heldere voorraam van het oog troebel maakt. Dit artikel onderzoekt waarom bepaalde cellen aan het binnenoppervlak van de cornea na verloop van tijd verslijten en littekenweefsel vormen, en waarom vrouwen vaker worden getroffen. Inzicht in deze verborgen veranderingen kan de weg openen naar medicijnen die de noodzaak van corneatransplantaties vertragen of zelfs voorkomen.
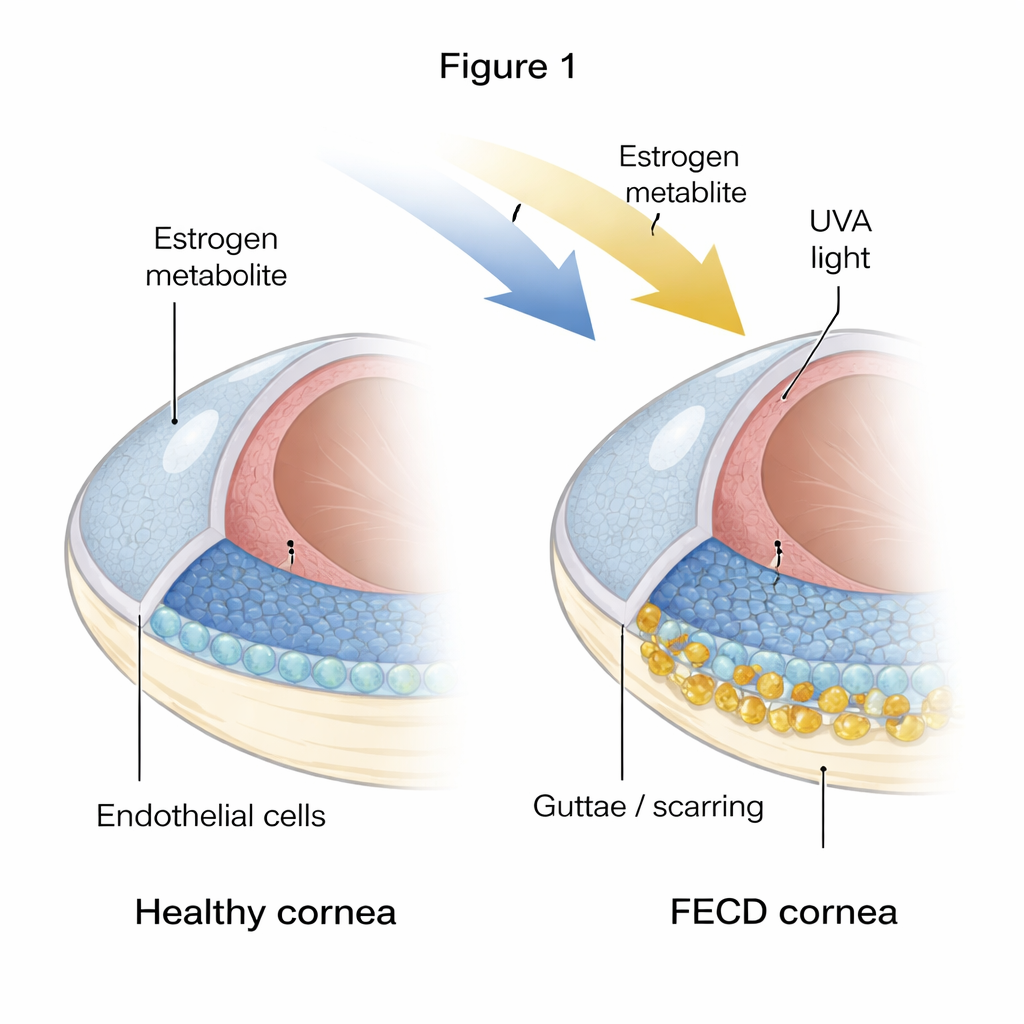
De kwetsbare binnenbekleding van de cornea
De cornea moet precies gedehydrateerd blijven om transparant te blijven; die taak wordt uitgevoerd door een enkele laag zeshoekige cellen, de cornea-endotheelcellen. Bij FECD gaan veel van deze cellen verloren en wordt de laag ongelijkmatig en plaatselijk beschadigd. Tegelijkertijd bouwen zich harde bobbels en verdikt materiaal op het binnenoppervlak op, bekend als guttae en overtollig extracellulair matrix. De auteurs vergeleken gezonde donorcornea's met cornea's van FECD-patiënten en vonden sterke aanwijzingen dat het zieke weefsel zowel ’verouderd’ als fibrotisch is: cellen vertoonden merkers van senescentie (een permanente stilstand) en van fibrose (cellen die zich meer als littekenvormende cellen gedragen en extra matrix afzetten).
Chronische licht- en hormoonstress duwt cellen in een doodlopende weg
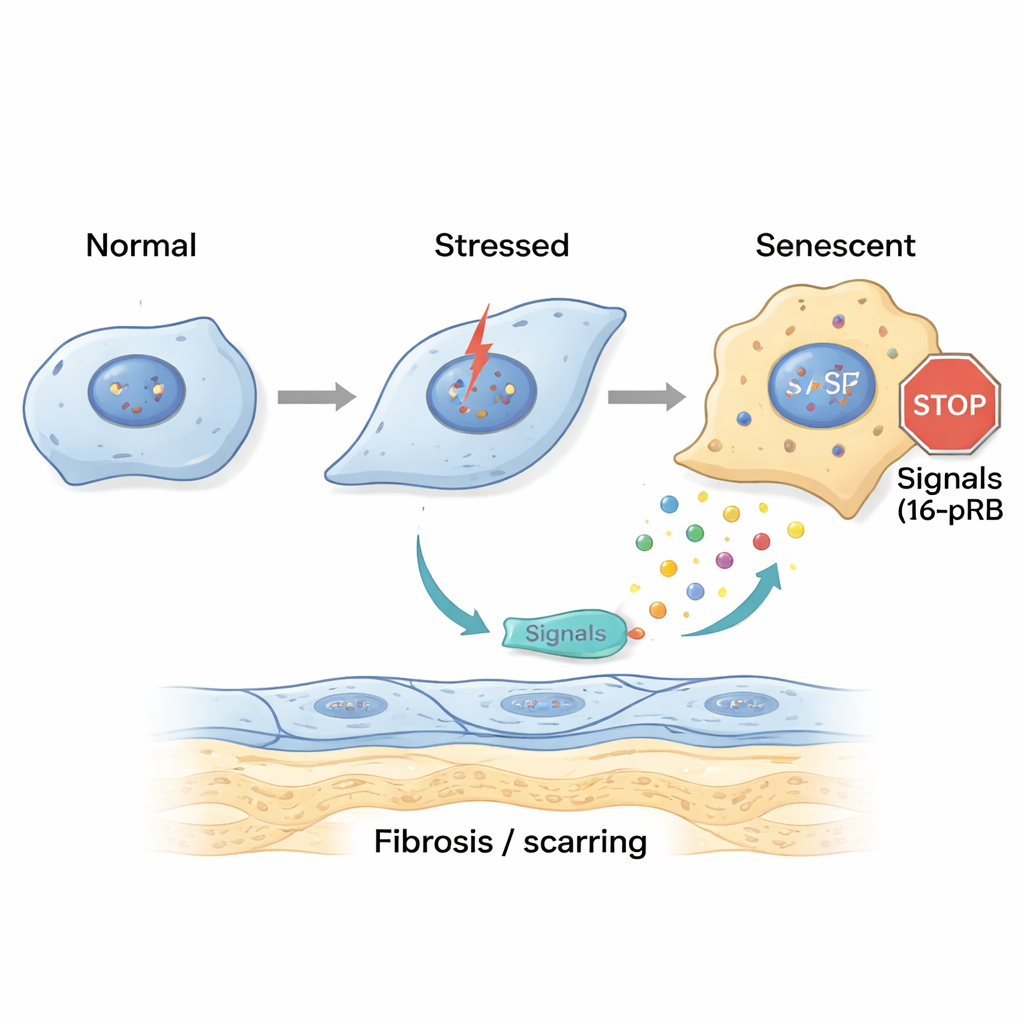
Om te onderzoeken hoe deze schade begint, simuleerden de onderzoekers FECD-achtige stress in het laboratorium. Ze brachten gezonde cornea-endotheelcellen bloot aan ultraviolette A (UVA)-straling en aan 4-hydroxyestradiol, een geïoniseerd oestrogeenbijproduct dat geassocieerd wordt met DNA-schade. Eén korte blootstelling maakte cellen tijdelijk stopgezet in een latere fase van de celcyclus en zette een vroege overgang naar een meer fibroblast-achtig stadium in gang, maar er bleef enige herstelcapaciteit bestaan. Door herhaalde, chronische blootstelling verdwenen die mogelijkheden echter: cellen stapelden zich op in een vroege celcyclusfase genaamd G0/G1 en schakelden een gen genaamd p16 aan, dat de celcyclus vergrendelt via zijn partnerproteïne pRB. Deze cellen werden groot, plat en onmiskenbaar senescent, en brachten daarnaast sterke expressie van fibrose-markers en eiwitten voort die bijdragen aan de verdikte guttae bij FECD.
Senescente cellen geven schadelijke signalen af en verspreiden littekenvorming
Senescente cellen zitten niet stil; ze scheiden een mix van signaalmoleculen uit die bekendstaat als het senescence-associated secretory phenotype (SASP). Het team verzamelde vocht van gestreste corneacellen en bracht dit aan op verse cellen en op gezonde donorcornea's. De ‘acute’ SASP veroorzaakte vroege tekenen van celvormverandering, terwijl de ‘chronische’ SASP veel cellen naar senescentie dreef en genen verhoogde die samenhangen met fibrose en extra matrixafzetting. Gedetailleerde analyses toonden aan dat chronische SASP rijk was aan ontstekingsboodschappers zoals IL-8 en IL-17, die bekendstaan om het bevorderen van veroudering van cellen, fibrotische littekenvorming en rekrutering van immuuncellen. Wanneer de onderzoekers het IL-17-pad of de IL-8-receptor CXCR2 blokkeerden, vertoonden cellen die aan chronische SASP waren blootgesteld minder senescentiemerkers en minder fibrose, wat suggereert dat deze signalen belangrijke drijfveren van de ziekte zijn.
Versleten cellen verwijderen ter bescherming van het gezichtsvermogen
Aangezien p16-positieve senescente cellen zo nauw verbonden waren met littekenvorming, testten de auteurs of het elimineren ervan de cornea kon beschermen. In een muismodel waarin UVA-licht FECD-achtige veranderingen veroorzaakt, behandelden ze de dieren met een senolytische geneescombinatie, Dasatinib plus Quercetine, die selectief senescente cellen doodt. Vergeleken met onbehandelde muizen behielden de met senolytica behandelde muizen een regelmatiger endotheelcelmozaïek, behielden ze meer cellen in totaal en vertoonden ze minder merkers van senescentie, fibrose en overtollige matrix. Met andere woorden, het opruimen van de meest beschadigde cellen verminderde de last van schadelijke afscheidingen en hielp een gezonder cornea-oppervlak te behouden.
Wat dit betekent voor mensen met FECD
Voor patiënten leidt FECD momenteel vaak tot corneatransplantatie wanneer het zicht te troebel wordt. Deze studie suggereert een ander pad: de ziekte kan worden aangedreven door een langzame ophoping van gestreste, niet-delende cellen die zowel hun functie niet meer vervullen als hun buren actief vergiftigen met ontstekings- en fibrotische signalen. Het richten op die signalen met geneesmiddelen tegen IL-17- of IL-8-paden, of het gebruik van senolytische therapieën om selectief de ergst aangetaste cellen te verwijderen, zou op termijn littekenvorming kunnen vertragen, meer van het natuurlijke weefsel van het oog kunnen behouden en de noodzaak van chirurgie kunnen uitstellen of verminderen.
Bronvermelding: Parekh, M., Adhikari, Y., Deshpande, N. et al. p16-mediated G0/G1 cell cycle arrest leads to SASP and fibrosis in Fuchs endothelial corneal dystrophy. Cell Death Dis 17, 197 (2026). https://doi.org/10.1038/s41419-026-08425-6
Trefwoorden: Fuchs-dystrofie, cornea-endotheel, cellulaire senescentie, fibrose, senolytische therapie