Clear Sky Science · nl
Mitochondriaal DNA activeert de NLRP3-IL-1β-as in microglia door te binden aan NLRP3, wat leidt tot neurodegeneratie in Parkinson-modellen
Waarom dit belangrijk is voor de ziekte van Parkinson
De ziekte van Parkinson staat vooral bekend om tremoren en vertraagde beweging, maar onder deze symptomen speelt zich een complexe strijd in de hersenen af. Deze studie onthult hoe kleine fragmenten genetisch materiaal uit beschadigde mitochondriën in immuuncellen van de hersenen ontsteking kunnen aanwakkeren die geleidelijk de dopamine-producerende neuronen doodt die nodig zijn voor vloeiende bewegingen. Inzicht in deze keten van gebeurtenissen opent nieuwe, zeer specifieke doelwitten voor geneesmiddelen die mogelijk de schade zoals bij Parkinson kunnen vertragen of voorkomen.
Hersenimmuuncellen en energiecentrales onder stress
De hersenen bevatten niet alleen neuronen, maar ook microglia, de residentiële immuuncellen. Bij de ziekte van Parkinson worden deze microglia vaak overactief en geven ze giftige moleculen en ontstekingssignalen af die nabijgelegen neuronen beschadigen. De auteurs concentreerden zich op mitochondriën, de “energiecentrales” van cellen, die hun eigen DNA dragen. Wanneer mitochondriën beschadigen—door toxines, veroudering of andere stressoren—kan hun DNA geoxideerd raken, een vorm van chemische schade veroorzaakt door reactieve zuurstofsoorten. Omdat mitochondriaal DNA lijkt op bacterieel DNA, kunnen deze beschadigde fragmenten binnen de hersenen fungeren als alarmsignalen, het immuunsysteem waarschuwen en mogelijk chronische ontsteking aandrijven.
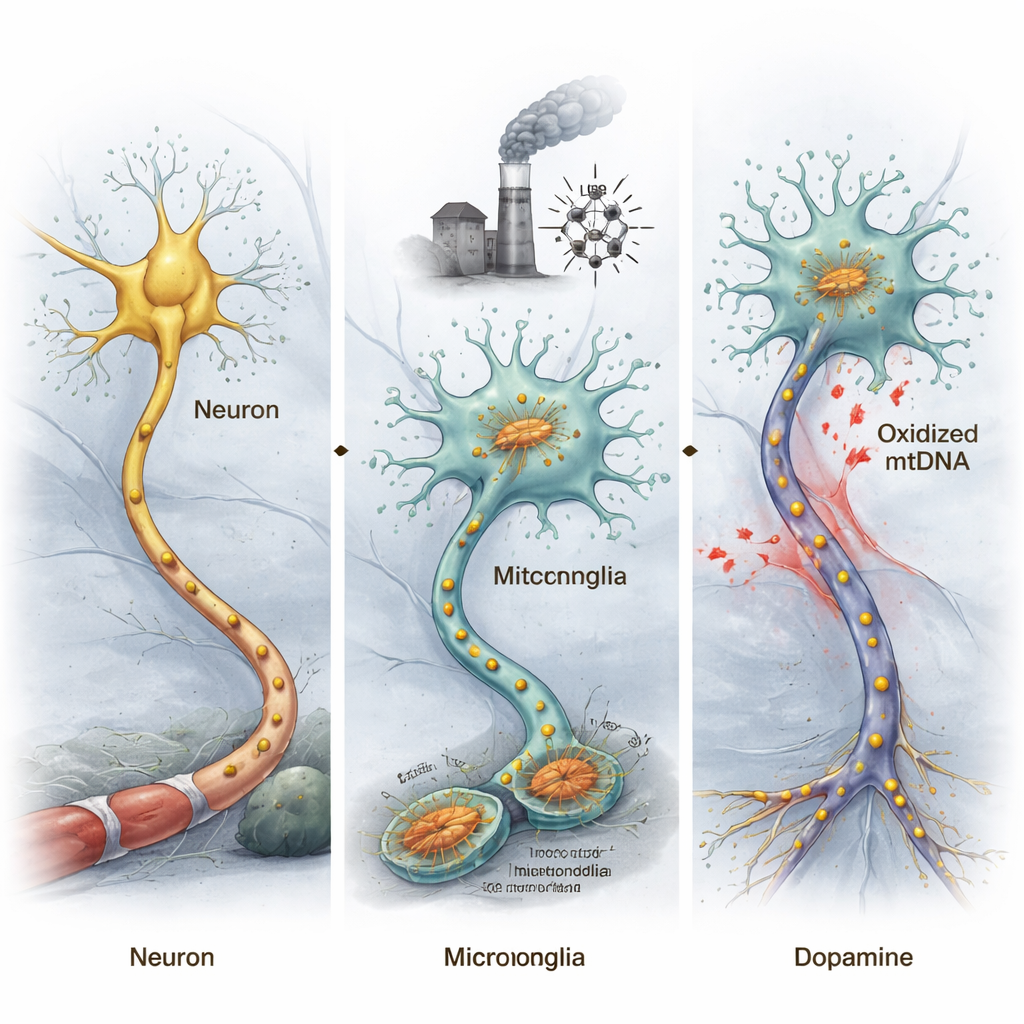
Beschadigd mitochondriaal DNA kan muizen naar Parkinson-achtige ziekte duwen
Om te testen of geoxideerd mitochondriaal DNA (ox-mtDNA) daadwerkelijk Parkinson-achtige veranderingen kan veroorzaken, haalden de onderzoekers ox-mtDNA uit gestresste microgliale cellen en injecteerden dit rechtstreeks in een hersenregio die normaal dopamine-producerende neuronen bevat die belangrijk zijn voor beweging. Muizen die aan dit ox-mtDNA werden blootgesteld, toonden verminderde beweging in gedragstests en een verlies van deze dopaminerge neuronen, wat overeenkomt met kernkenmerken van de ziekte van Parkinson. Door neuronen en microglia uit het middenbrein te sorteren en hun genactiviteit te analyseren, vond het team dat genen die aan Parkinson verbonden zijn meer afwijkend werden in neuronen, terwijl ontstekingsgerelateerde genen sterk geactiveerd waren in microglia.
Een molekeur alarm binnen microglia
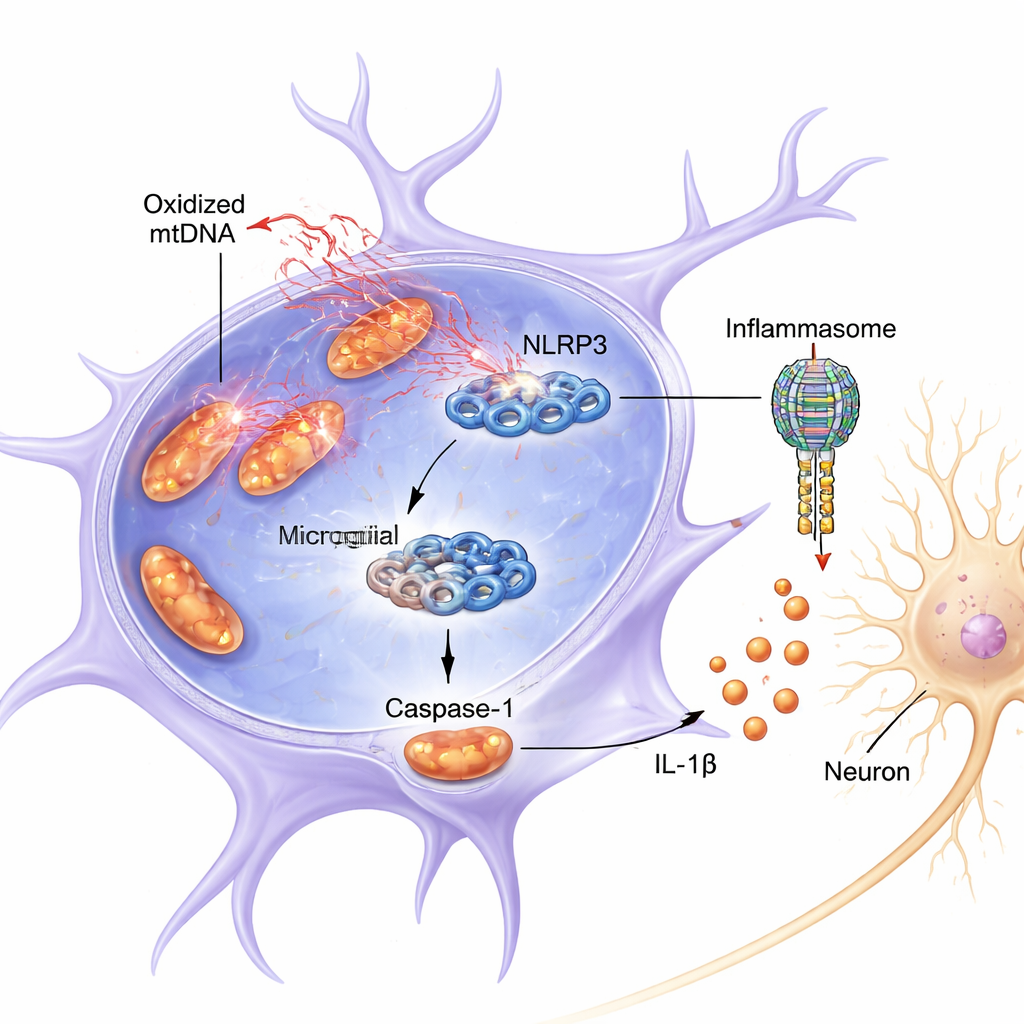
De studie richtte zich op een eiwitcomplex in microglia genaamd NLRP3, onderdeel van een groter geheel dat het inflammasoom wordt genoemd. Wanneer het wordt geactiveerd, helpt NLRP3 bij het aanzetten van caspase-1, een enzym dat het ontstekingsmolecuul IL-1β in zijn actieve, schadelijke vorm knipt. Zowel in muizen als in gekweekte cellen veroorzaakte de combinatie van een inflammatoire primingsignaal (LPS, een bacterieel bestanddeel) en het pesticide-achtige toxine rotenon dat mitochondriën in microglia geoxideerd mtDNA vrijgaven in het celvocht. Deze vrijgave viel samen met sterkere activatie van NLRP3, meer gekloven (actieve) caspase-1 en hogere IL-1β-niveaus. Medium afkomstig van deze overactieve microglia was direct toxisch voor dopamine-achtige neuronen die in een kweek werden gekweekt, met verminderde overleving en lagere niveaus van hun belangrijkste marker, tyrosinehydroxylase.
Directe binding: hoe geoxideerd DNA de NLRP3-schakelaar omzet
Verder dan louter correlatie toonden de auteurs aan dat ox-mtDNA niet alleen aanwezig is tijdens ontsteking—het lijkt fysiek te binden aan NLRP3 en het te activeren. Wanneer ze de vrijgave van mitochondriaal DNA blokkeerden met een geneesmiddel, namen de activatie van caspase-1 en IL-1β af. Omgekeerd versterkte het rechtstreeks afleveren van geoxideerd mtDNA in microglia de NLRP3-signaalgeving sterk, meer dan niet-geoxideerd mtDNA. Met behulp van biochemische pull-downexperimenten detecteerden ze mtDNA, rijk aan markers van oxidatieve schade, gekoppeld aan NLRP3. Computer-modellering en eiwitchemie onthulden dat ox-mtDNA bindt aan een positief geladen, flexibele segment van NLRP3 (een “intrinsiek gedesordeerd gebied” dat aminozuren 180–187 omvat). Wanneer dit cruciale stukje uit NLRP3 werd verwijderd, nam het vermogen om ox-mtDNA te binden en caspase-1 te activeren sterk af.
Het uitschakelen van het inflammasoom spaart neuronen
De onderzoekers vroegen zich vervolgens af of het blokkeren van NLRP3 neuronen kon beschermen. In gekweekte microglia verminderde het genetisch verlagen van NLRP3 sterk de activatie van caspase-1 en IL-1β na behandeling met LPS en rotenon, en het geconditioneerde medium van deze cellen was veel minder toxisch voor dopamine-achtige neuronen. Bij muizen verminderde een selectieve NLRP3-remmer (MCC950) de activatie van microglia, behield dopaminerge neuronen en verlaagde inflammasoom-gerelateerde eiwitten in modellen die werden aangedreven door ofwel LPS plus rotenon of door geïnjecteerd mtDNA. Samen tonen deze experimenten aan dat de ox-mtDNA–NLRP3–IL-1β-keten niet slechts geassocieerd is met schade; ze is vereist voor een groot deel van het waargenomen neuronverlies.
Wat dit betekent voor toekomstige therapieën tegen Parkinson
Voor niet-specialisten is de kernboodschap dat beschadigd mitochondriaal DNA dat uit immuuncellen in de hersenen lekt, rechtstreeks kan vasthechten aan een interne “alarmschakelaar” (NLRP3), wat een golf van ontsteking veroorzaakt die dopamine-neuronen beschadigt en in modellen Parkinson-achtige ziekte aandrijft. Omdat deze interactie afhangt van een korte, gedefinieerde segment van het NLRP3-eiwit en van de geoxideerde aard van het mitochondriaal DNA, biedt ze precieze nieuwe geneesmiddeldoelen. Therapieën die voorkomen dat mitochondriaal DNA beschadigt of ontsnapt, die de binding ervan aan NLRP3 blokkeren, of die NLRP3 zelf remmen, zouden in principe deze ontstekingscascade kunnen afkoelen en de progressie van de ziekte van Parkinson kunnen vertragen.
Bronvermelding: Gan, Q., Fu, X., Zhou, T. et al. Mitochondrial DNA drives NLRP3-IL-1β axis activation in microglia by binding to NLRP3, leading to neurodegeneration in Parkinson’s disease models. Cell Death Dis 17, 213 (2026). https://doi.org/10.1038/s41419-026-08424-7
Trefwoorden: Ziekte van Parkinson, microglia, mitochondriaal DNA, NLRP3-inflammasoom, neuroinflammatie