Clear Sky Science · nl
Lactylatie van SLC26A3 in het zure tumormicro-omgeving bevordert de kwaadaardige progressie van colorectale carcinomen
Waarom tumorzuurtegraad ertoe doet
Colorectale kanker blijft een van de dodelijkste kankers wereldwijd, deels omdat tumoren vaak terugkeren, uitzaaien of ophouden te reageren op behandelingen. Deze studie onderzoekt een ondergewaardeerde oorzaak van dat gedrag: de zure, melkzuurrijke omgeving binnen tumoren. Door te laten zien hoe deze vijandige omgeving een beschermend membraaneiwit genaamd SLC26A3 destabiliseert, onthullen de auteurs een nieuwe keten van gebeurtenissen die kankercellen helpt meer stamcelachtig, invasief en geneesmiddelresistent te worden — wat nieuwe behandelideeën biedt.
Een vijandige buurt rond kankercellen
Snelgroeiende tumoren verbruiken veel suiker en zuurstof en scheiden melkzuur en waterstofionen uit, waardoor hun omgeving verzureert. Met behulp van grote patiëntendatasets en weefselmonsters tonen de onderzoekers aan dat deze zure toestand, gemarkeerd door een eiwitmarker genaamd CA9, samenhangt met agressieve colorectale tumoren. Bij geavanceerdere kankers zijn de CA9-waarden hoog, terwijl SLC26A3-waarden consequent laag zijn. SLC26A3 bevindt zich normaal op het oppervlak van darmcellen en helpt bij het balanceren van zout en bicarbonaat, wat op zijn beurt de zuurtegraad reguleert. In tumorstalen, kankercellijnen en enkelceldata vindt het team dat wanneer de zuurtegraad stijgt, SLC26A3 afneemt — vooral in kwaadaardige, stamcelachtige kankercellen. 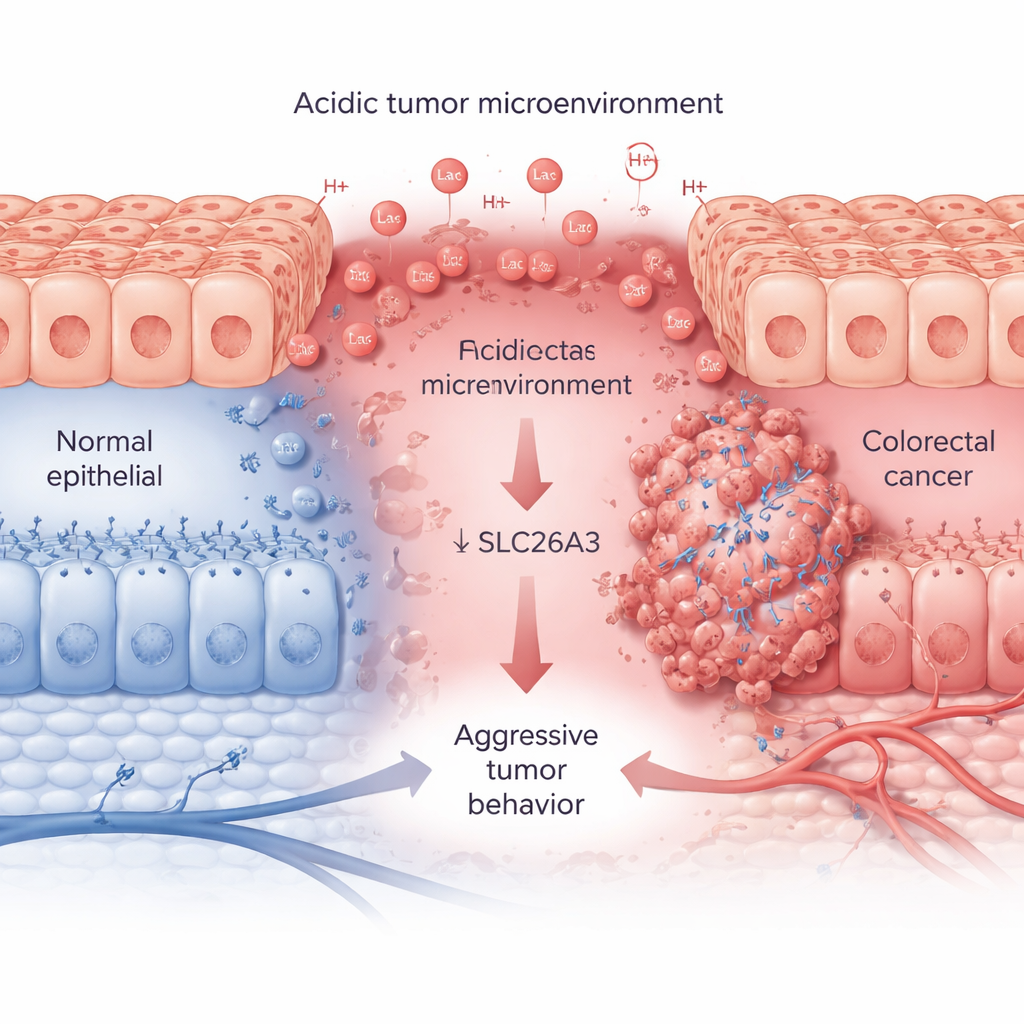
Hoe melkzuur een doelwit markeert voor vernietiging
De auteurs vragen zich vervolgens af waarom SLC26A3 afneemt in zure tumoren. Ze richten zich op lactylatie, een recent ontdekt chemisch merkje dat ontstaat uit melkzuur en aan eiwitten kan worden toegevoegd. Wanneer colorectale kankercellen worden blootgesteld aan melkzuur of in zure omstandigheden worden gekweekt, raakt SLC26A3 sterk gelactyleerd. Gedetailleerde proteïne-analyse wijst één sleutelplaats aan, een aminozuur genaamd K536, waar dit merkteken wordt geplaatst. Lactylatie op K536 maakt SLC26A3 minder stabiel: het eiwit wordt sneller gemerkt met ubiquitine, een cellair "gooi-dit-weg"-signaal, en naar het afbreeksysteem van de cel gestuurd. Het blokkeren van het enzym p300, dat bijdraagt aan het plaatsen van lactylatie-markeringen, beschermt SLC26A3 gedeeltelijk tegen afbraak. Hierdoor zetten zuurtegraad en lactaat een schadelijke feedbacklus op — meer lactaat leidt tot meer lactylatie, wat SLC26A3 vermindert, de pH-balans verder verstoort en een nog zuurdere micro-omgeving bevordert.
Het uitschakelen van een rem op kankerstamgedrag en verspreiding
Met SLC26A3 uitgeput, gedragen kankercellen zich agressiever. In kweek vertonen colorectale stamcelachtige kankercellen van nature minder SLC26A3 dan hun niet-stamcelachtige tegenhangers. Wanneer onderzoekers opzettelijk SLC26A3 verlagen, vormen tumorcellen meer sferen (een kenmerk van stamcellen), vernieuwen zich efficiënter, dringen door kunstmatige membranen en migreren sneller over kraswonden. Ze worden ook minder gevoelig voor gangbare chemotherapiemiddelen zoals oxaliplatine en 5‑fluorouracil. Omgekeerd vermindert versterking van SLC26A3 stamcelmarkers en vertraagt invasie en migratie — maar dit voordeel neemt af wanneer extra lactaat wordt toegevoegd, wat benadrukt hoe zuurtegraad het beschermende effect kan overrulen.
Een verborgen link naar genregulatie
Naast het helpen reguleren van zuurtegraad fungeert SLC26A3 ook als een scaffold die twee RNA-bindende eiwitten bindt: HuR en CUGBP1. Deze eiwitten regelen de levensduur van veel boodschapper-RNA's die kankergeneeslijke eiwitten coderen. Wanneer SLC26A3 ruim aanwezig is, sequestreert het een deel van HuR en CUGBP1, waardoor hun vermogen om bepaalde kankergerelateerde boodschappen te stabiliseren of te destabiliseren beperkt wordt. Wanneer SLC26A3 verloren gaat door lactylatie en afbraak, zijn HuR en CUGBP1 vrijer om oncogene mRNA's te binden die stamgedrag, epitheliale-mesenchymale transitie (EMT), invasie en overleving bevorderen. Experimenten tonen aan dat HuR mRNA's voor stamcelmarkers en cel-junctie-eiwitten helpt stabiliseren, terwijl CUGBP1 sommige doelen kan tegenwerken, de junction-integriteit vermindert en EMT aanmoedigt — beide bevorderen tumorspreiding.
Het herbalanceren van de omgeving om kanker te bestrijden
Om te testen of deze inzichten in behandelingsstrategieën kunnen worden omgezet, gebruiken de onderzoekers muismodellen van colorectale kanker. Het neutraliseren van tumorzuurtegraad met natriumbicarbonaat, het blokkeren van lactaattransport met een MCT1-remmer, of het overexpressen van SLC26A3 vertraagt allemaal de tumorgroei. Het combineren van SLC26A3‑herstel met chemotherapie verkleint tumoren nog verder. In patiëntgegevens correleert een hogere SLC26A3-uitdrukking met betere overleving, minder recidief, minder metastasen en betere reacties op chemotherapie, wat suggereert dat dit eiwit zowel als biomarker als therapeutisch doel kan dienen. 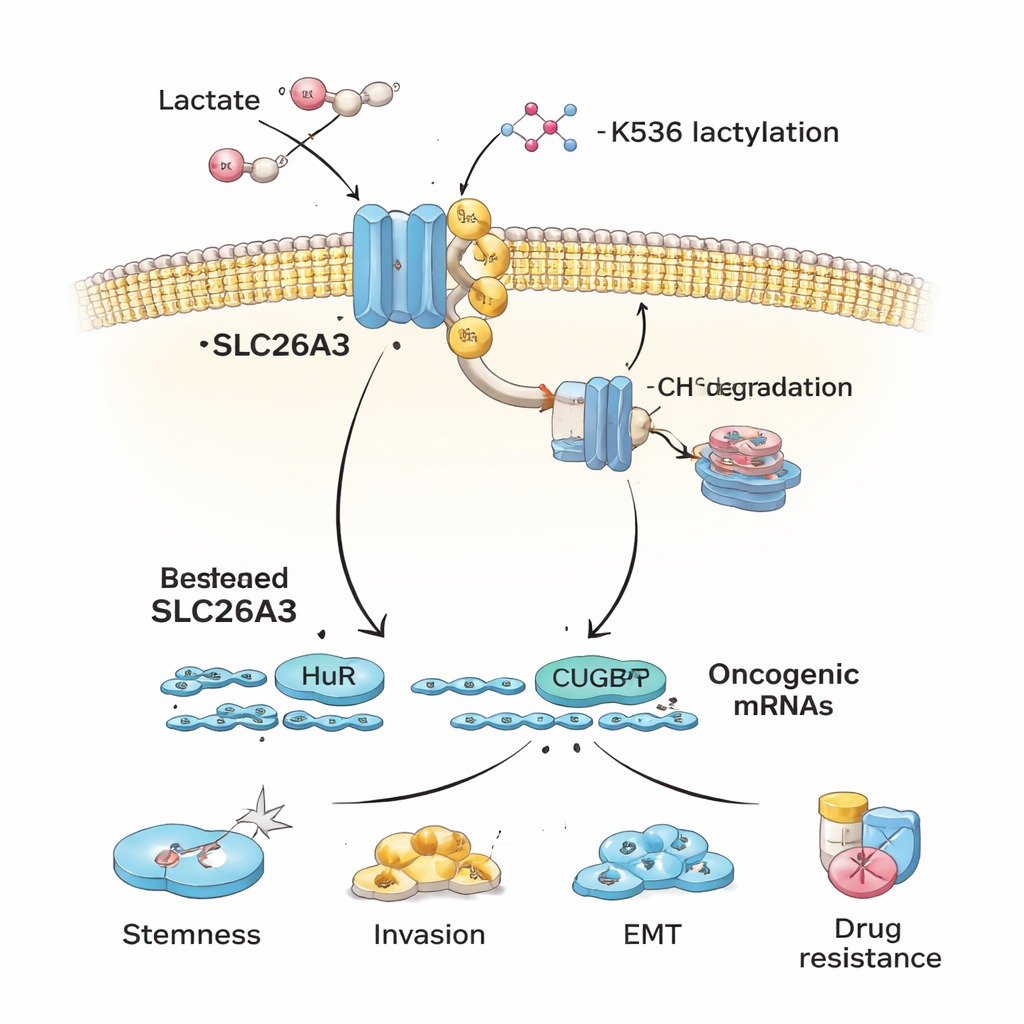
Wat dit betekent voor patiënten
In gewone bewoordingen laat deze studie zien dat colorectale tumoren floreren in een zure, melkzuurrijke omgeving die een beschermende poortwachter, SLC26A3, chemisch "merkt" en vernietigt. Zodra deze poortwachter wegvalt, nemen kankercellen gemakkelijker stamcelachtige eigenschappen aan, verspreiden ze zich en worden ze behandelingsresistenter, geholpen door krachtige RNA-regulatoren in de cel. Door tumorzuurtegraad te bufferen, lactaatverwerking te blokkeren of SLC26A3 te herstellen, kan die kwaadaardige feedbacklus mogelijk worden verzwakt en standaardtherapieën effectiever worden gemaakt. Hoewel dergelijke benaderingen nog rigoureus klinisch getest moeten worden, bieden ze een veelbelovende nieuwe invalshoek voor hoe het beheersen van de chemische omgeving van tumoren kan helpen bij het bestrijden van colorectale kanker.
Bronvermelding: Chen, C., Cai, D., Liu, X. et al. Lactylation of SLC26A3 in the acidic tumor microenvironment promotes malignant progression of colorectal carcinoma. Cell Death Dis 17, 164 (2026). https://doi.org/10.1038/s41419-026-08422-9
Trefwoorden: colorectale kanker, tumormicro-omgeving, lactylatie, kankerstamcellen, chemotherapie-resistentie