Clear Sky Science · nl
Gericht op GNG4 remt tumorprogressie en herstelt gevoeligheid voor enzalutamide bij prostaatkanker door autophagie te onderdrukken
Waarom dit onderzoek ertoe doet
Voor veel mannen met gevorderde prostaatkanker werken krachtige hormoonblokkers zoals enzalutamide aanvankelijk goed, maar verliezen ze na verloop van tijd hun effect. Deze studie onthult een verborgen overlevingsmechanisme dat tumorcellen gebruiken en wijst op een specifiek eiwit, GNG4, dat kankers helpt doorgroeien en behandeling te weerstaan. Inzicht in dit mechanisme kan leiden tot combinatiebehandelingen die bestaande middelen effectiever en langduriger maken.
Een eiwitwisselaar die in het zicht verborgen is
Prostaatkankercellen worden sterk aangedreven door mannelijke hormonen, dus de standaardzorg voor gevorderde ziekte schakelt deze signalen uit. Toch worden de meeste tumoren uiteindelijk “castratie-resistent” en beginnen ze weer te groeien. De onderzoekers zochten naar genen die veel actiever waren in tumormateriaal dan in het naastgelegen normale prostaatweefsel van dezelfde patiënten. Onder meerdere kandidaten stak GNG4 eruit: wanneer ze het niveau van dit eiwit verlaagden in prostaatkankercellen, daalde de tumorgroei sterk. Analyses van honderden patiëntmonsters bevestigden dat GNG4 hoger is in primaire prostaatkankers dan in normaal weefsel en bijzonder verhoogd is in agressievere, hooggradige tumoren.
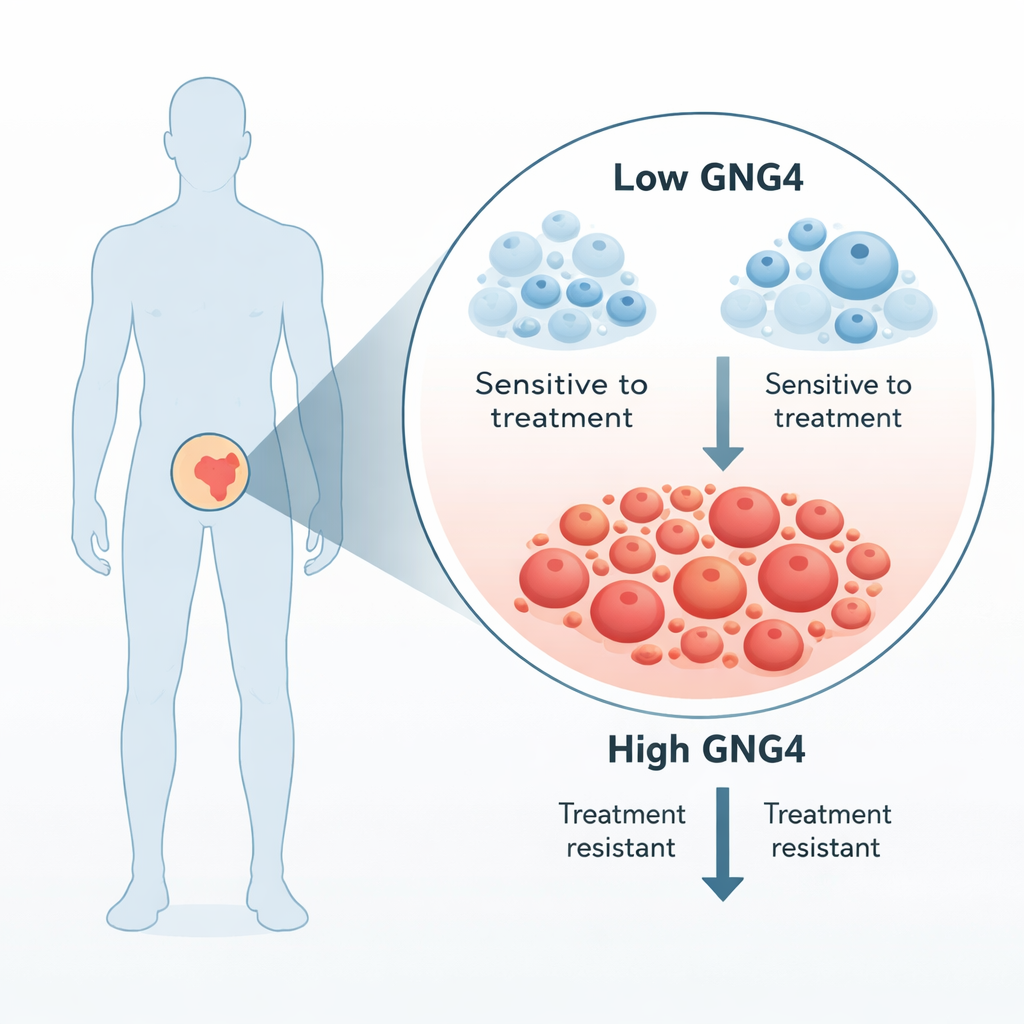
Hoe GNG4 tumoren helpt gedijen
GNG4 maakt deel uit van een grotere signaalfamilie, bekend als G-eiwitten, die aan het celmembraan zitten en signalen van buiten naar binnen doorgeven. Het team toonde aan dat het terugdraaien van GNG4 in prostaatkankercellijnen de celdeling vertraagde, cellen deed stoppen in een controlepunt van de celcyclus en geprogrammeerde celdood (apoptose) verhoogde. Deze veranderingen verminderden ook het vermogen van kankercellen om te migreren en wonden te sluiten in laboratoriumtests, en tumoren die uit GNG4-deficiënte cellen waren gevormd groeiden langzamer in muismodellen. Samen suggereren deze bevindingen dat GNG4 als het gaspedaal fungeert voor groei en verspreiding van prostaatkanker.
Autophagie: de noodvoorraadkast van de kankercel
De onderzoekers richtten zich vervolgens op een proces dat autophagie heet, waarbij cellen hun eigen componenten afbreken en recyclen om stress te overleven, zoals voedseltekort of medicijnbehandeling. In veel gevorderde kankers fungeert autophagie als een noodvoorraadkast die tumorcellen helpt omgaan met moeilijke omstandigheden. In deze studie vertoonden prostaatkankercellen met hoge GNG4-activiteit meer tekenen van actieve autophagie, terwijl cellen met gereduceerde GNG4 minder recyclestructuren en lagere niveaus van belangrijke autophagiemarkers hadden. Wanneer GNG4 werd overgeproduceerd, verdroegen cellen enzalutamide beter en ondergingen ze minder celdood. Het blokkeren van autophagie met een chemische remmer maakte een groot deel van deze bescherming ongedaan, wat aangeeft dat GNG4 tumoren voornamelijk helpt behandeling te doorstaan door dit recyclingsysteem op te voeren.
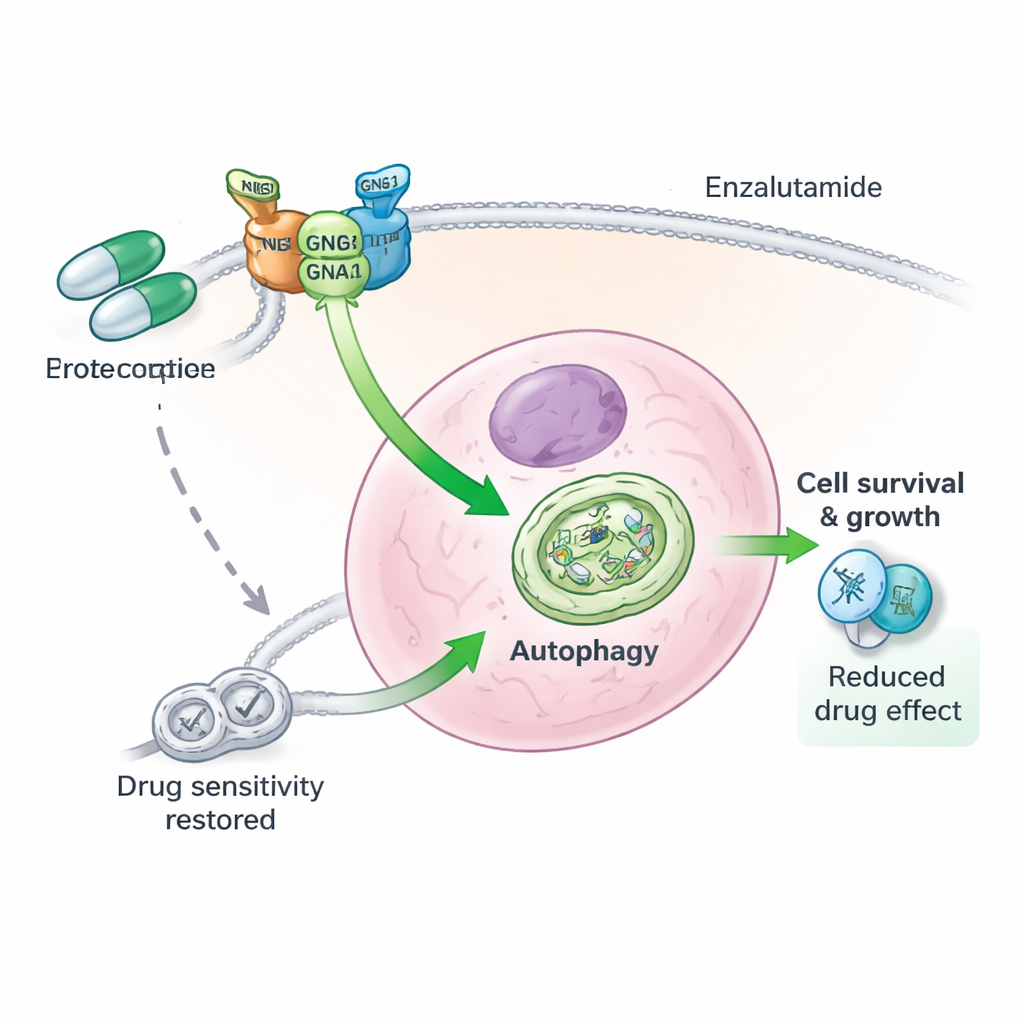
Een trio-eiwitteam achter medicijnresistentie
Dieper gravend ontdekten de auteurs dat GNG4 niet alleen werkt. Het bindt fysiek aan een ander G-eiwitcomponent, GNB1, om een derde eiwit, GNAI3, te stabiliseren. Samen vormen deze drie subeenheden een functioneel complex dat autophagie in prostaatkankercellen versterkt. Wanneer GNG4 werd verminderd, werd GNAI3 sneller gemerkt voor afbraak en afgebroken door het cellulair afvalverwerkingssysteem, waarmee het autophagiesignaal werd uitgeschakeld. Het verwijderen van GNAI3 zelf maakte de groeivoordelen en overlevingsvoordelen die door extra GNG4 werden verleend ongedaan, zowel in gecultiveerde cellen als in muizentumoren. Met andere woorden, GNG4 drijft maligniteit en stressbestendigheid grotendeels via deze GNG4–GNB1–GNAI3-as.
Bestaande geneesmiddelen harder laten werken
Tot slot onderzochten de onderzoekers wat er gebeurt wanneer gericht remmen van GNG4 wordt gecombineerd met enzalutamide, een toonaangevend middel voor gevorderde prostaatkanker. In het laboratorium maakte het terugbrengen van GNG4 kankercellen duidelijk gevoeliger voor enzalutamide en verminderde hun vermogen om na behandeling kolonies te vormen. In muizen krompen tumoren met verlaagd GNG4 sterker bij toediening van enzalutamide dan tumoren met normale GNG4-niveaus, zonder duidelijke extra toxiciteit. Directe blokkering van autophagie leverde vergelijkbare verbeteringen op. Deze resultaten suggereren dat het verstoren van GNG4-gedreven autophagie tumorcellen hun vitale copingmechanisme kan ontnemen, waardoor bestaande hormoonblokkerende therapieën een krachtigere en duurzamere slag kunnen toebrengen.
Wat dit betekent voor patiënten
Voor niet-specialisten is de kernboodschap dat sommige prostaatkankers behandeling overleven door een intern recyclingsysteem in te schakelen dat fungeert als een noodgenerator. Deze studie identificeert GNG4 als de hoofdschakelaar die dat systeem inschakelt, in samenwerking met partner-eiwitten om kankercellen tegen enzalutamide te beschermen. Door deze schakelaar uit te schakelen—ofwel door GNG4 direct te richten of door autophagie op een veilige manier te dempen—kunnen toekomstige therapieën mogelijk de tumorgroei vertragen en de gevoeligheid voor medicijnen herstellen bij mannen van wie de kankers moeilijk te behandelen zijn.
Bronvermelding: Chen, L., Zhang, J., Hu, Y. et al. Targeting GNG4 inhibits tumor progression and restores enzalutamide sensitivity in prostate cancer by suppressing autophagy. Cell Death Dis 17, 160 (2026). https://doi.org/10.1038/s41419-026-08421-w
Trefwoorden: prostaatkanker, medicijnresistentie, autophagie, G-eiwitten, enzalutamide