Clear Sky Science · nl
DNA-PKcs orkestreert CTLA-4‑depletie‑geïnduceerde senescentie in kankercellen
De groeiknop van kanker veranderen in een stopsein
Immunotherapieën tegen kanker richten zich vaak op een molecuul genaamd CTLA‑4, dat op immuuncellen wordt gevonden, om het lichaam te helpen tumoren aan te vallen. Deze studie onthult een verrassende wending: CTLA‑4 komt ook voor binnenin kankercellen en kan daar fungeren als een verborgen groeihulp. Wanneer wetenschappers deze intracellulaire CTLA‑4 doelbewust verwijderden uit melanoomcellen, stopten de kankercellen met delen en belandden ze in een langdurige “pensioen‑”toestand die bekendstaat als cellulaire senescentie. Het begrijpen van deze onverwachte rol opent nieuwe mogelijkheden om tumoren te vertragen of zelfs te laten krimpen door CTLA‑4 binnen kankercellen aan te pakken, en niet alleen op immuuncellen.
Wanneer cellen kiezen voor pensioen in plaats van ongecontroleerde groei
Cellen delen zich normaal, repareren zich en—wanneer ze onherstelbaar beschadigd zijn—sterven ze of raken ze in senescentie, een blijvende stop van hun groei. Senescentie‑cellen worden doorgaans groter, veranderen van vorm en produceren specifieke merkers die in het laboratorium kunnen worden gedetecteerd. De onderzoekers ontdekten dat wanneer ze CTLA‑4 in muis‑ en menselijke melanoomcellen verminderden, de cellen groter werden, hun groei sterk daalde en klassieke senescentiesignalen toenamen, waaronder enzymen die zichtbaar zijn met speciale kleuringen en eiwitten zoals p16 en p21 die de celcyclus blokkeren. Deze veranderingen traden op zowel bij tijdelijke stillegging van CTLA‑4 als bij permanente uitzetting met gen‑editing‑tools.
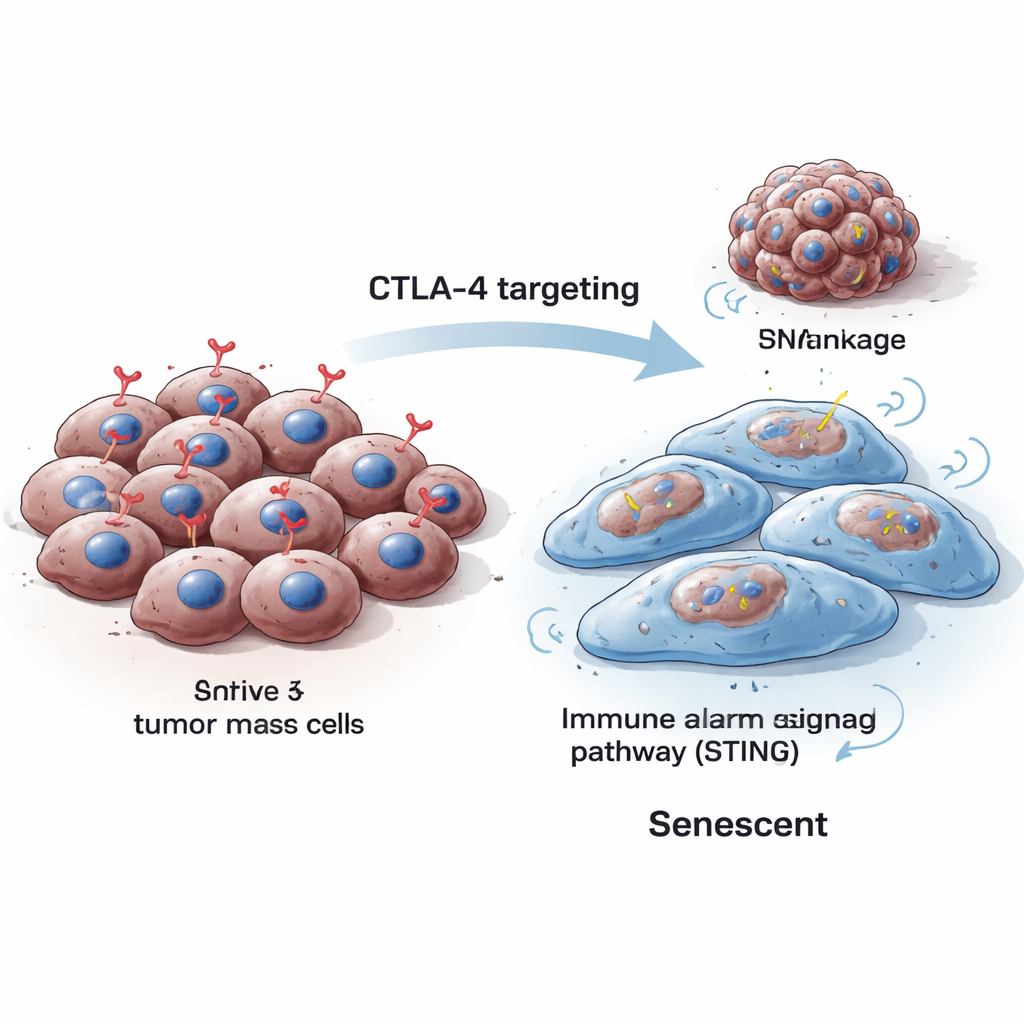
Scheurtjes in het genetische stappenplan leiden tot stilstand
Om te begrijpen waarom verlies van CTLA‑4 kankercellen in senescentie duwt, onderzochten de onderzoekers hoe deze cellen hun DNA behandelen tijdens deling. Ze ontdekten dat CTLA‑4‑depletie de niveaus van Aurora B verminderde, een eiwit dat helpt chromosomen schoon te scheiden tijdens celdeling. Wanneer Aurora B daalde, ontwikkelden de cellen genomische instabiliteit: kleine extra DNA‑bevattende lichaampjes, micronucleus genoemd, verschenen en markers voor DNA‑schade namen toe. Dit soort DNA‑stress staat bekend om cellen richting senescentie te duwen in plaats van naar ongecontroleerde groei. Belangrijk is dat het herstellen van Aurora B hielp deze micronuclei te verminderen, waarmee het verlies van CTLA‑4 rechtstreeks werd verbonden met foutief chromosoombeheer en DNA‑schade.
DNA‑schade activeert een intern alarmeringssysteem
Het gebroken en verkeerd geplaatste DNA in CTLA‑4‑gedepleteerde cellen bleef niet onopgemerkt. Het activeerde DNA‑PKcs, een sensor voor DNA‑schade, die op zijn beurt het STING‑pad activeerde, een ingebouwd alarm dat reageert op losgeraakt DNA in cellen. Zodra STING werd ingeschakeld, stuurde het signalen naar downstream moleculen, waaronder TBK1 en IRF3, en versterkte het ook een andere belangrijke groeicontroleroute, het AKT‑pad. In plaats van groei te bevorderen leidde deze gecombineerde signaalvoering uiteindelijk tot een toename van p21, een krachtige rem op de celcyclus, wat de senescente toestand versterkte. Wanneer de wetenschappers DNA‑PKcs blokkeerden, verminderden STING‑activatie en de kenmerken van senescentie sterk, wat aantoont dat DNA‑PKcs centraal staat in deze alarmlijn.
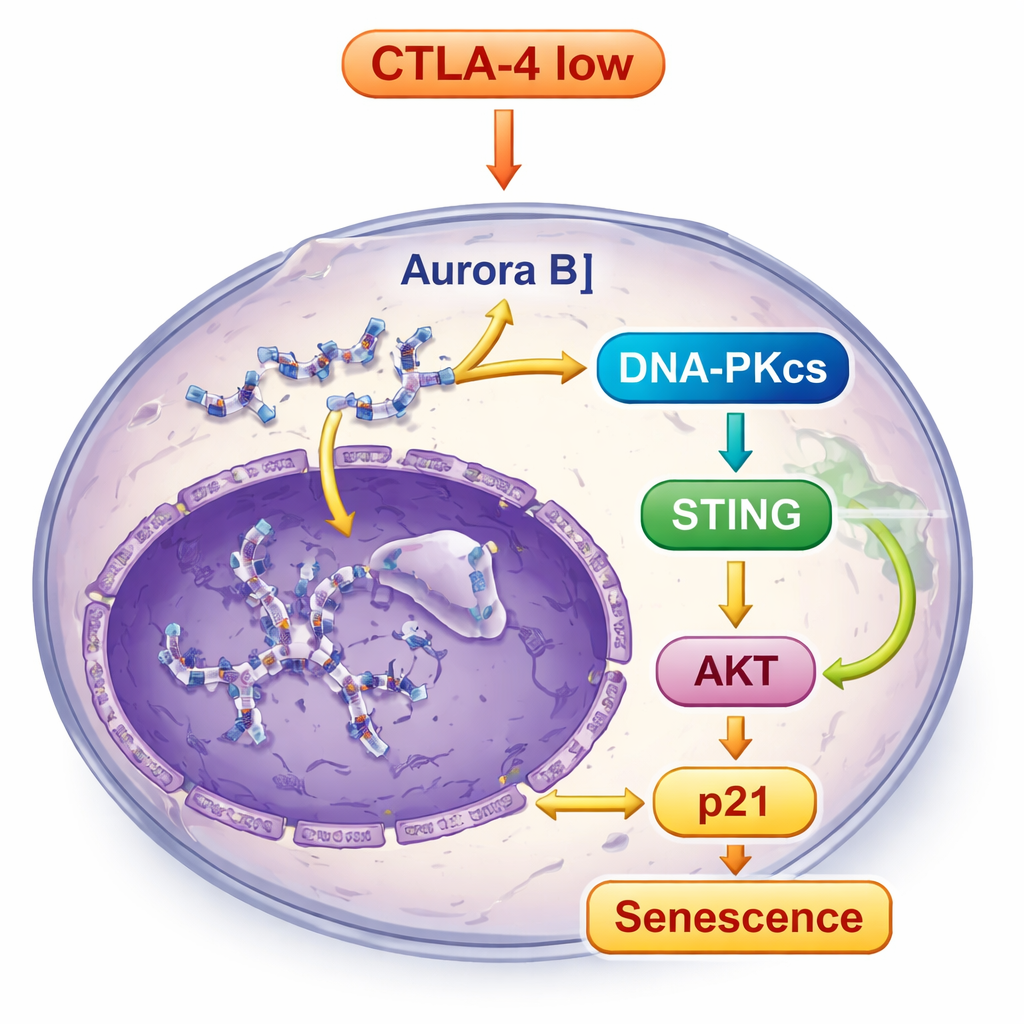
Van kweekschotel naar tumoren in levende dieren
Laboratoriumschotels vertellen maar een deel van het verhaal, dus testten de onderzoekers of verlies van CTLA‑4 echte tumoren in muizen zou beïnvloeden. Ze implanteren melanoomcellen met of zonder CTLA‑4 aan tegenovergestelde zijden van dezelfde dieren. Tumoren zonder CTLA‑4 groeiden langzamer, wogen minder en hadden een kleiner volume dan hun CTLA‑4‑bevatte tegenhangers. Deze CTLA‑4‑deficiënte tumoren lieten ook sterkere senescentiekleuring en hogere niveaus van DNA‑schade en STING‑padactivatie zien. Analyse van patiëntgegevens uit grote openbare databases ondersteunde de koppeling verder: over meerdere kankertypen bleek CTLA‑4‑expressie vaak omgekeerd gerelateerd aan DNA‑PKcs en andere DNA‑herstelcomponenten, wat de laboratoriumbevindingen in menselijke ziekte weerspiegelt.
Wat dit betekent voor toekomstige kankerbehandelingen
Samenvattend toont de studie aan dat CTLA‑4 binnen kankercellen hen helpt genetische stabiliteit te behouden en te blijven delen. Wanneer CTLA‑4 wordt verwijderd, raken chromosomen instabiel, hopen DNA‑breuken zich op en activeert een intern alarmpad—gecentreerd op DNA‑PKcs en STING—dat de cellen in permanente groeistop duwt. Voor leken betekent dit dat het uitschakelen van CTLA‑4 in tumorcellen kankers wegduwt van gevaarlijk snelle groei en richting een veiligere, “gepensioneerde” toestand. Deze inzichten suggereren dat toekomstige kankertherapieën niet alleen ontworpen kunnen worden om het immuunsysteem los te laten door CTLA‑4 op immuuncellen te blokkeren, maar ook om tumoren direct uit te schakelen door CTLA‑4 binnen kankercellen te richten en senescentie als een ingebouwde rem op kankergroei te benutten.
Bronvermelding: Lee, JJ., Rhee, W.J., Kim, S.Y. et al. DNA-PKcs orchestrates CTLA-4 depletion-induced senescence in cancer cells. Cell Death Dis 17, 204 (2026). https://doi.org/10.1038/s41419-026-08419-4
Trefwoorden: cellulaire senescentie, melanoom, CTLA-4, DNA‑schade, STING‑pad