Clear Sky Science · nl
Cytoplasma‑kern transport van TET2: een intrinsische rem op de progressie van colorectale kanker
Hoe kankercellen hun eigen rem dragen
Colorectale kanker is een van de meest voorkomende vormen van kanker wereldwijd en wordt vaak dodelijk zodra tumorcellen leren omliggend weefsel binnen te dringen en naar andere organen uit te zaaien. Deze studie laat zien dat veel van die kankercellen feitelijk een intern "remsysteem" dragen — een eiwit genaamd TET2 — dat hun voortgang kan vertragen wanneer het naar de kern van de cel verhuist. Begrijpen hoe deze ingebouwde rem aan- en uitgezet wordt, kan nieuwe manieren openen om tumorgroei te remmen in plaats van alleen te proberen kankercellen rechtstreeks te doden.
Een sleutelprotein in tumorcellen zien bewegen
De onderzoekers concentreerden zich op TET2, een eiwit dat helpt te bepalen welke genen aan of uit staan door bepaalde chemische markeringen op DNA te verwijderen. In weefselmonsters van honderden patiënten met colorectale kanker volgden ze waar TET2 zich in de tumorcellen bevindt. Ze vonden vier hoofdpatronen: voornamelijk in de kern, voornamelijk in het cytoplasma, of sterk gekanteld naar het een of het ander. Patiënten van wie de tumoren meer TET2 in de kern hadden, leefden doorgaans langer, terwijl degenen bij wie TET2 in het cytoplasma bleef, slechtere uitkomsten hadden. Naarmate kankers naar latere klinische stadia vorderden, werd kern‑TET2 zeldzamer, wat suggereert dat het verliezen van deze nucleaire bescherming deel uitmaakt van hoe tumoren agressiever worden.
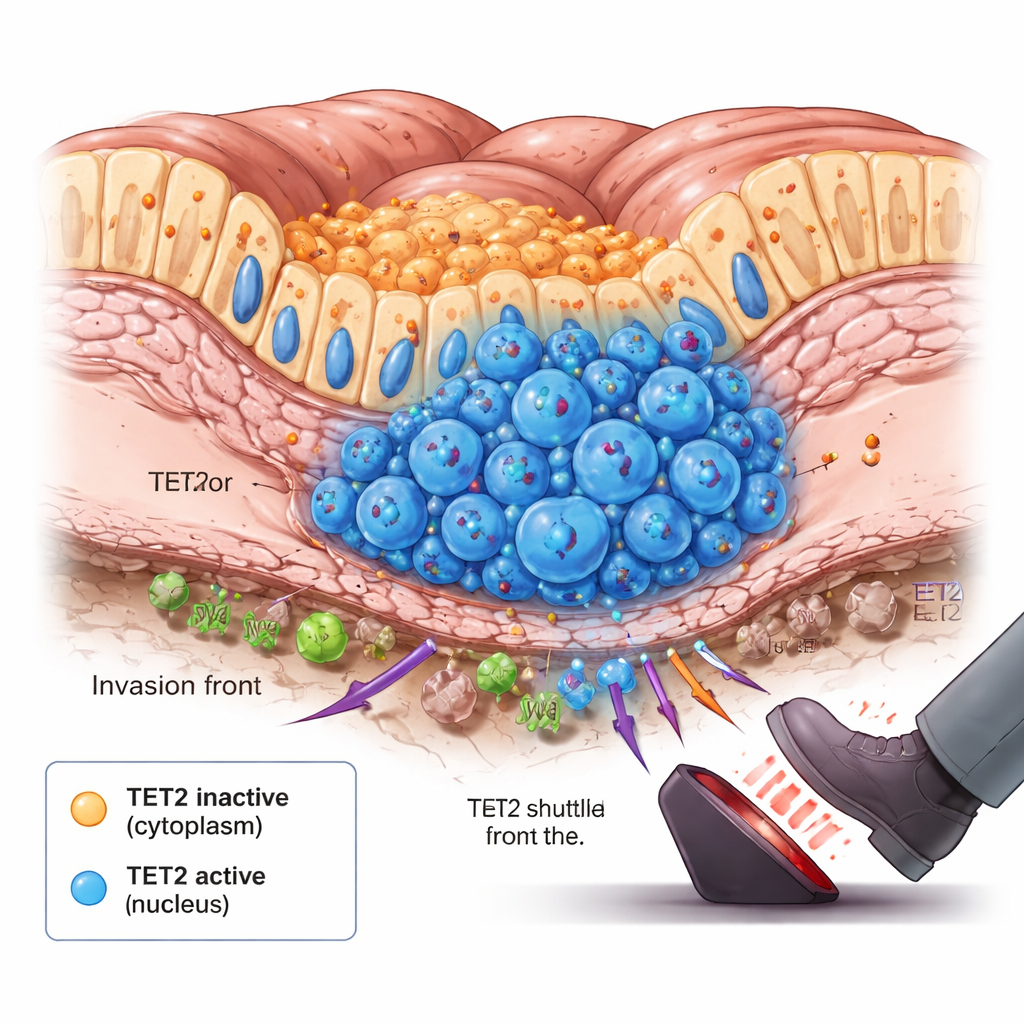
De frontlinie van de tumor en het moment van verandering
Dieper gravend merkte het team iets verrassends op: in tumoren die net begonnen te verspreiden, was er een lichte toename van cellen waarin TET2 naar de kern was verplaatst. Deze cellen groeperden zich aan de onderkant van de darmwand, de invasiegrens waar kankercellen eerst in dieper weefsel drukken. Dierproeven en langlopende kweekmodellen die tumorgroei nabootsen, toonden een vergelijkbaar patroon in de tijd. In het begin bleef TET2 in het cytoplasma en was grotendeels inactief. Toen tumoren groeiden en binnenste gebieden verarmden aan zuurstof en voedingsstoffen, activeerden intracellulaire signalen TET2 om in specifieke subpopulaties naar de kern te schuiven. Eenmaal daar verwijderde TET2 DNA‑methylatiemerken en vertraagde de tumorgroei, werkend als een noodrem wanneer de kanker een gevaarlijke drempel overschreed.
Wanneer "gas"‑signalen ook een rem triggeren
Colorectale tumoren vertrouwen vaak op twee krachtige "gas"‑programma’s: een vormveranderingsproces genaamd epitheliale–mesenchymale transitie (EMT), dat cellen mobieler en invasiever maakt, en de WNT‑signalering, die groei en overleving stimuleert. Deze paden worden gewoonlijk als puur schadelijk bij kanker gezien. Deze studie toont echter aan dat wanneer EMT en WNT sterk afgaan, ze ook helpen TET2 naar de kern te drijven. Met behulp van geneesmiddelen en genetische instrumenten in celculturen lieten de wetenschappers zien dat het aanzetten van EMT of WNT ervoor zorgde dat meer cellen TET2 naar hun kernen verplaatsten, terwijl het blokkeren van deze paden het tegengestelde effect had. Eenmaal in de kern zette actieve TET2 vervolgens EMT‑ en WNT‑gerelateerde genen terug, waardoor celmigratie afnam en proliferatie vertraagde. Met andere woorden, dezelfde signalen die tumoren helpen groeien, wekken ook een interne tegenkracht.
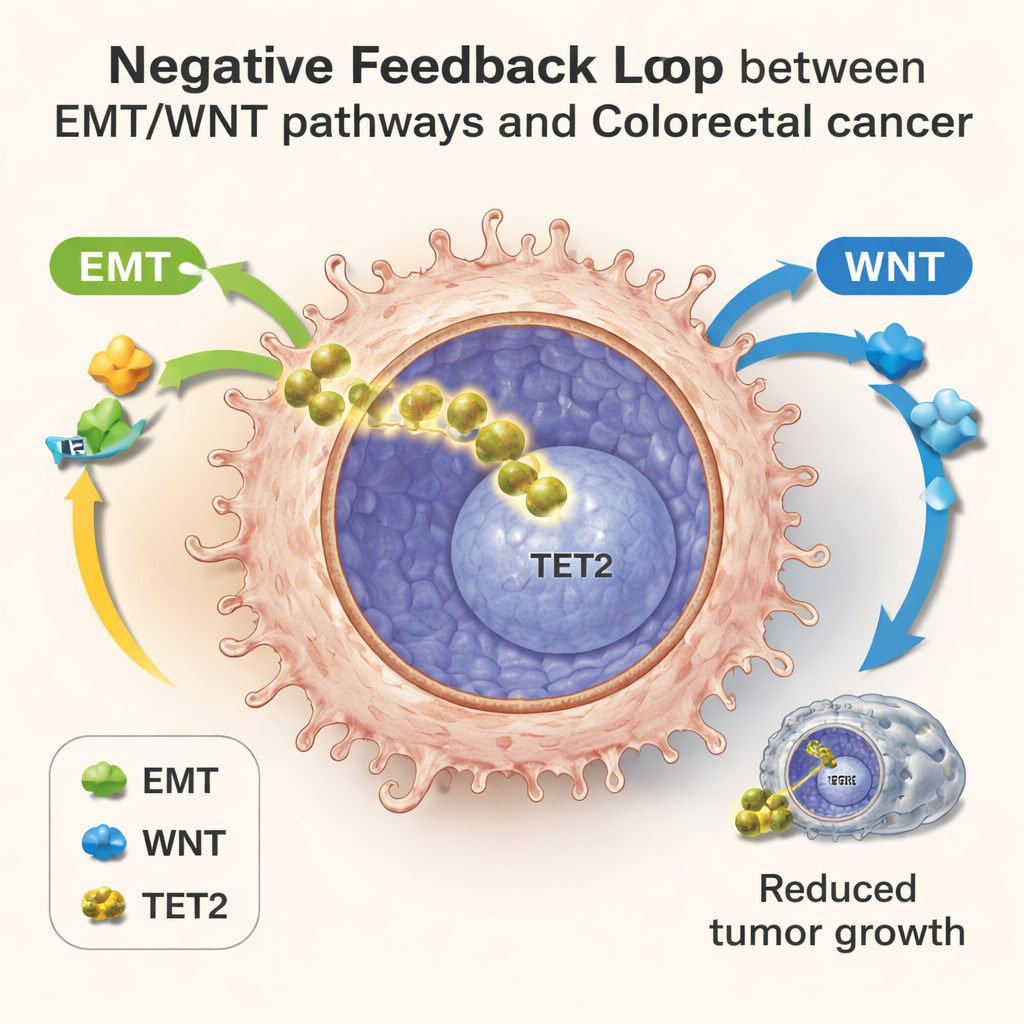
Enkele cellen onthullen een verborgen terugkoppelingslus
Om dit kat‑en‑muis‑spel gedetailleerd in kaart te brengen, gebruikte het team single‑cell RNA‑sequencing, een techniek die afleest welke genen actief zijn in duizenden individuele cellen tegelijk. In in het lab gekweekte kolonies, in muizentumoren en in monsters van patiënten met colorectale kanker zagen ze cellen verspreid langs een progressietijdlijn. Vroege cellen vertoonden normaal energiegebruik en zwakke EMT/WNT‑activiteit; latere cellen lieten metabole herprogrammering, sterke EMT/WNT‑signalen en vervolgens stijgende expressie van TET2‑doelgenen zien. In deze latere stappen hadden cellen met hogere TET2‑activiteit lagere niveaus van invasiegerelateerde genen en werden ze geassocieerd met betere patiëntuitkomsten, zelfs binnen tumoren die al begonnen waren te verspreiden. Dit patroon ondersteunt het idee van een negatieve terugkoppeling: metabole stress en EMT/WNT‑activering zetten TET2 aan om naar de kern te gaan, en nucleair TET2 remt op zijn beurt diezelfde agressieve programma’s af.
Wat dit betekent voor toekomstige kankerbehandelingen
Voor niet‑deskundigen is de kernboodschap dat de progressie van colorectale kanker geen eenvoudige "aan/uit"‑schakel is tussen goed en slecht gedrag. In plaats daarvan is er een ingebouwd, vertraagd veiligheidsmechanisme: naarmate tumorcellen invasiever worden, activeren ze ook TET2 in hun kernen, wat ze gedeeltelijk in toom houdt. In de loop van de tijd weten veel tumoren te ontkomen door nucleair TET2 te verliezen of zijn effecten te overweldigen. Door manieren te vinden om TET2 in de kern te houden of zijn activiteit te versterken — mogelijk in combinatie met middelen die EMT of WNT moduleren — zouden artsen deze natuurlijke rem kunnen versterken en de verspreiding van kanker kunnen vertragen. In plaats van kankercellen alleen van buitenaf aan te vallen, zouden toekomstige therapieën kunnen werken door dit interne controlesysteem te herstellen en te versterken.
Bronvermelding: Li, C., Meng, F., He, J. et al. Cytoplasm-nucleus shuttling of TET2: an intrinsic brake in colorectal cancer progression. Cell Death Dis 17, 163 (2026). https://doi.org/10.1038/s41419-026-08418-5
Trefwoorden: colorectale kanker, TET2, epigenetica, EMT WNT‑signalering, kankerprogressie