Clear Sky Science · nl
Aberrante handhaving van de ontwikkelings-transcriptiefactor PAX6 bevordert celdood van neuronen via JNK3-signaalering
Waarom dit onderzoek van belang is voor het zicht
Glaucoom is een belangrijke oorzaak van permanente blindheid, grotendeels omdat de zenuwcellen die visuele informatie van het oog naar de hersenen vervoeren langzaam afsterven. Veel behandelingen verlagen de oogdruk, maar mensen kunnen nog steeds ziensvermogen verliezen, zelfs wanneer de druk goed onder controle is. Deze studie stelt een dieperliggende vraag: wat doet deze retinale zenuwcellen besluiten te sterven wanneer ze onder stress staan, en kunnen we dat besluit uitzetten op het niveau van genregulatie in de celkern?
Een gestrest netvlies onder aanval
Centraal bij glaucoom en aanverwante oogaandoeningen staat het langzame verlies van retinale ganglioncellen (RGCs), de uitvoerende neuronen van het oog. Deze cellen zijn kwetsbaar voor veel soorten stress, waaronder giftige niveaus van de hersenboodschapper glutamaat, dat NMDA-receptoren overactiveert en schadelijke calciumoverbelasting opwekt. De onderzoekers gebruikten een goed gevestigde muismodel waarbij een kleine hoeveelheid NMDA in het oog wordt geïnjecteerd, waarbij RGCs selectief worden beschadigd terwijl andere retinale lagen grotendeels intact blijven. Ze bevestigden dat deze behandeling de oogdruk niet veranderde, maar wel typische tekenen van geprogrammeerde celdood in RGCs veroorzaakte, zoals het vrijkomen van cytochroom c uit mitochondriën en het verschijnen van TUNEL-positieve kernen.
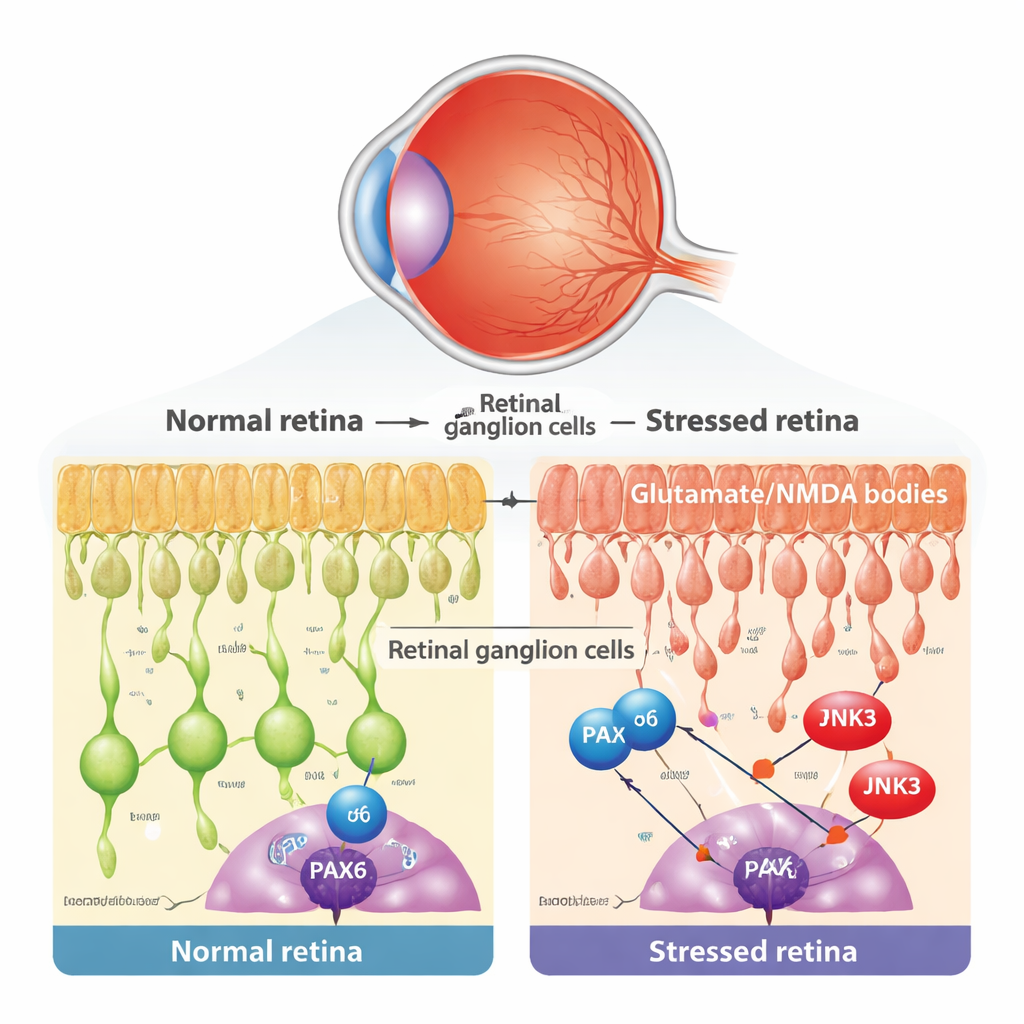
Een ontwikkelingsgen dat weigert met pensioen te gaan
Tijdens de vroege ontwikkeling fungeert een genregulator genaamd PAX6 als een meesterarchitect van het oog, die stuurt hoe verschillende retinale cellen ontstaan en worden bekabeld. De gangbare opvatting is dat zulke ontwikkelingsprogramma’s grotendeels uitgeschakeld zijn bij volwassenen. Door opnieuw single-cell RNA-sequencinggegevens van zowel muis- als menselijke netvliezen te analyseren, vonden de onderzoekers dat PAX6 in feite sterk en selectief wordt gehandhaafd in rijpe RGCs en bepaalde interneuronen. Met microscopische kleuring toonden ze aan dat in de laag waar RGCs zich bevinden, PAX6 grotendeels aanwezig is in ganglioncellen in plaats van in naburige amacriene cellen. Dit riep een intrigerende mogelijkheid op: in de volwassen ziekte zou een oud ontwikkelingsprogramma kunnen worden gekaapt en veranderd in een aanjager van degeneratie.
Van beschermer naar beul: PAX6 verandert van rol
Om te testen of PAX6 RGCs helpt overleven of sterven onder stress, gebruikten de wetenschappers een op gentherapie lijkende aanpak. Ze leverden een viraal vector die een klein RNA draagt dat specifiek PAX6 stillegt in het netvlies, en stelden vervolgens de ogen bloot aan NMDA. Vergeleken met controles toonden PAX6-gereduceerde netvliezen veel minder apoptotische RGCs en aanzienlijk minder mitochondriale schade, wat aangeeft dat PAX6 nodig is voor volledige celdood in dit model. Genoomwijde RNA-sequencing toonde aan dat veel pro-doodgenen, met name die betrokken bij mitochondriale schade en caspase-activatie, sterk werden geïnduceerd door NMDA in normale muizen maar afgezwakt waren wanneer PAX6 werd gedoofd. Met andere woorden: PAX6 helpt een netwerk van genen aan te zetten dat RGCs over de rand duwt.
De stresskinase die de PAX6-schakelaar omslaat
Hoe activeert stress PAX6 zonder zijn hoeveelheid te verhogen? Het team richtte zich op JNK3, een stress-responsief enzym dat voornamelijk in neuronen voorkomt. Onder NMDA-schade verhuisde JNK3 naar de kern van RGCs en ging fysiek een complex aan met PAX6. Biochemische proeve-op-glas-experimenten met gezuiverde eiwitten toonden aan dat JNK3 rechtstreeks fosfaatgroepen aan PAX6 kan toevoegen, en deze reactie werd geblokkeerd door een JNK-remmer. Bij muizen die het Jnk3-gen misten, produceerde NMDA niet langer hetzelfde patroon van PAX6-fosforylering. Chromatine-mapping (ChIP-seq) en gerichte DNA-bindingsassays lieten zien dat gefosforyleerd PAX6, samen met JNK3, onder stress sterker gebonden raakt aan de regelregio’s van sleutelgenen die pro-apoptotisch zijn, zoals Bax en Gadd45a, waardoor hun activiteit wordt verhoogd. Wanneer ofwel PAX6 werd gedoofd of JNK3 genetisch werd verwijderd, waren deze binding en de bijbehorende activatie van pro-doodgenen sterk verminderd.
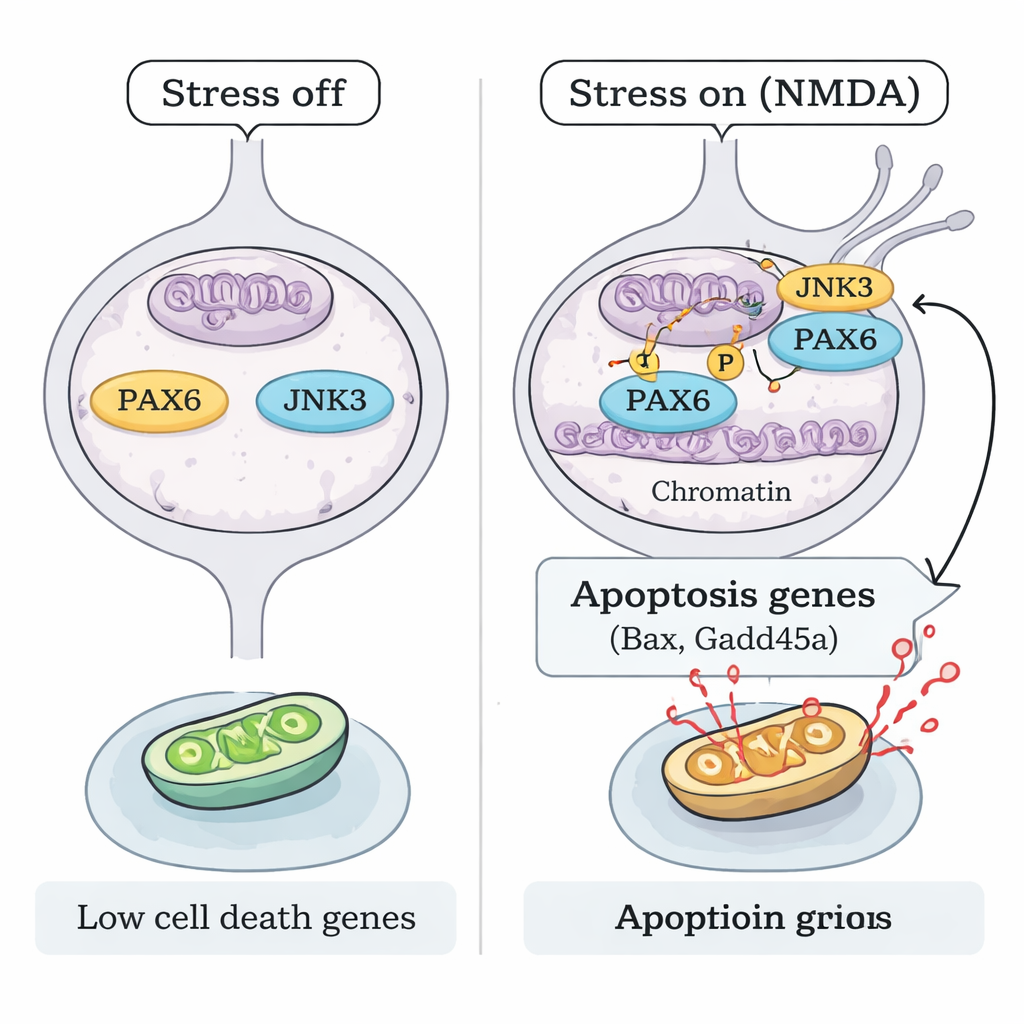
Het doodsprogramma uitzetten om het zicht te beschermen
Tot slot onderzochten de onderzoekers of het blokkeren van deze JNK3–PAX6-as voldoende is om zichtkritische cellen te beschermen. Zowel in PAX6-knockdownmuizen als in JNK3-deficiënte muizen bleven RGCs significant behouden na NMDA-blootstelling, met minder stervende cellen en een gezondere retinale structuur. Dit wijst op een helder mechanistisch model: onder excitotoxische stress fosforyleert JNK3 het persistent tot expressie gebrachte PAX6, waardoor het verandert van een ontwikkelingsbouwer in een krachtige activator van een celdood-genprogramma in volwassen RGCs. Het onderbreken van die koppeling — door PAX6 te silencen of JNK3 uit te schakelen — houdt veel van deze neuronen in leven. Voor patiënten suggereert dit werk dat toekomstige glaucoombehandelingen verder kunnen gaan dan het verlagen van de oogdruk en direct de genetische schakelaars kunnen richten die bepalen of retinale neuronen leven of sterven.
Bronvermelding: Kim, JY., An, MJ., Kim, J. et al. Aberrant maintenance of developmental transcription factor PAX6 promotes neuronal cell death via JNK3 signaling. Cell Death Dis 17, 161 (2026). https://doi.org/10.1038/s41419-026-08417-6
Trefwoorden: glaucoom, retinale ganglioncellen, PAX6, JNK3, neurodegeneratie