Clear Sky Science · nl
Het richten op ENO1 herprogrammeert macrophage-polarisatie om antitumorale immuniteit te activeren en verbetert het therapeutische effect van radiotherapie
Van tumorbescherming naar doelwit
Kanker overleeft vaak niet alleen door snel te groeien, maar ook door stilletjes de afweer van het lichaam uit te schakelen. Deze studie onderzoekt een verborgen molecuul op kankercellen, genaamd ENO1, dat tumoren helpt het immuunsysteem te ontwijken en weerstand te bieden tegen bestraling. Door een nieuw antilichaammedicijn te ontwikkelen dat ENO1 targeten, laten de onderzoekers zien dat het mogelijk is de beschermende chemie van de tumor af te voeren, immuuncellen te activeren en bestraling effectiever te maken in modellen van colorectale en triple-negatieve borstkanker. 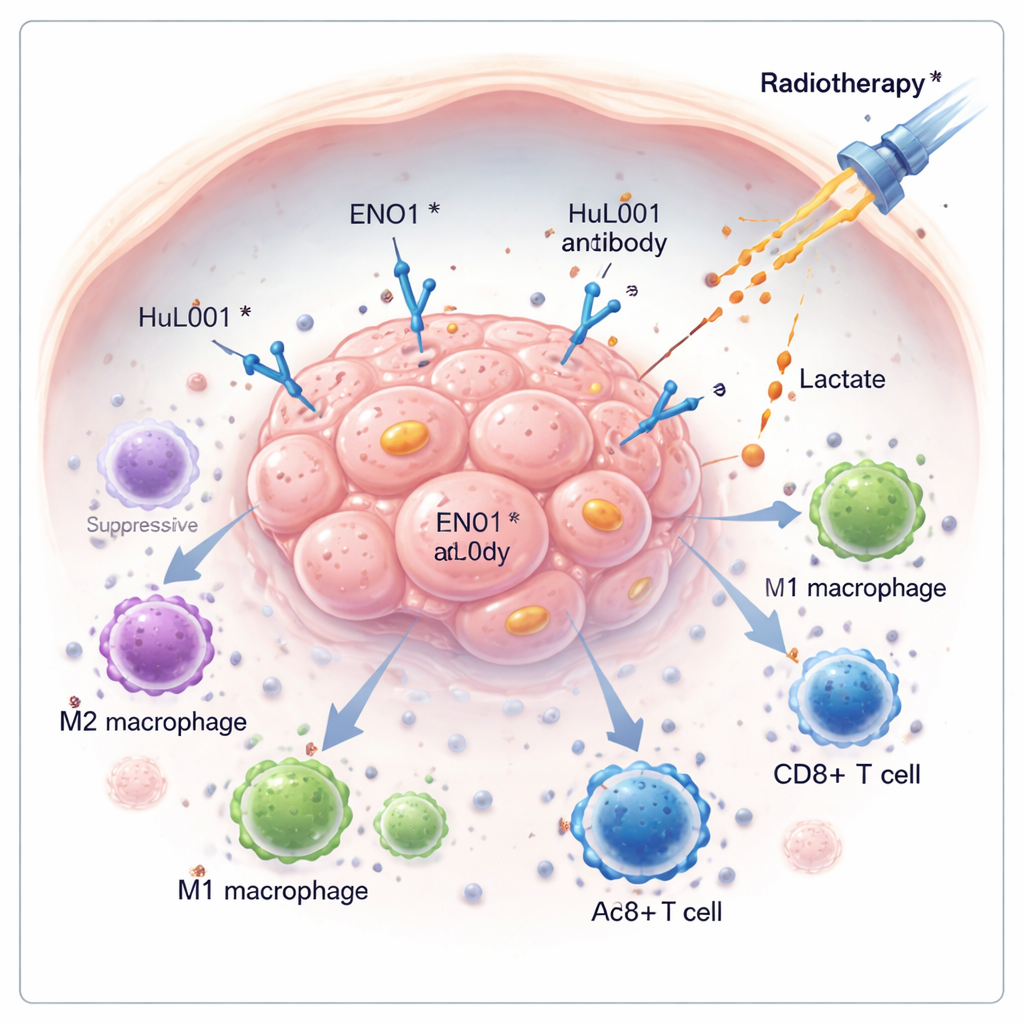
Een metabole truc die de immuniteit doet zwijgen
Veel tumoren herschikken hun energiegebruik en breken suiker af op een manier die grote hoeveelheden melkzuur (lactaat) produceert, zelfs wanneer er zuurstof beschikbaar is. Dit lactaat wordt uit de kankercellen gepompt en hoopt zich op rond de tumor, waardoor de omgeving zuur en vijandig wordt voor een immuunaanval. In dit werk richten de auteurs zich op ENO1, een enzym betrokken bij suikerafbraak dat ook op het celoppervlak van kankercellen kan verschijnen. Wanneer ENO1 aan het celoppervlak zit, werkt het samen met een andere eiwittransporter, MCT4, om lactaat naar buiten te exporteren—waardoor een omgeving ontstaat die tumorgroei bevordert en immuuncellen onderdrukt.
Hoe bestraling averechts kan werken
Radiotherapie is bedoeld om tumordna te beschadigen en immuunreacties op te wekken, maar het heeft ook bijwerkingen in het tumormicro-omgeving. Het team ontdekte dat signalen aangedreven door een molecuul genaamd TGFβ1, die door bestraling worden versterkt, een enzym (PRMT5) activeren dat ENO1 chemisch wijzigt en naar het celoppervlak verplaatst. Eenmaal daar interacteert ENO1 fysiek met MCT4 om dit te stabiliseren en lactaatexport te bevorderen. Hogere niveaus van oppervlakte-ENO1 werden gevonden bij patiënten met gevorderde colorectale en triple-negatieve borstkankers en waren gelinkt aan meer metastasen en slechtere overleving, wat suggereert dat bestraling onbedoeld een lactaatgedreven, immuunsuppressief schild rond tumoren kan versterken.
Het herprogrammeren van vriendelijke en vijandige immuuncellen
In de zure halo rond tumoren worden immuuncellen die macrophages heten in een "hersteler"-toestand geduwd (vaak M2 genoemd) die tumoren juist helpt door ontsteking te dempen en herstel te bevorderen, in plaats van kankercellen te doden. De onderzoekers maakten een gehumaniseerd antilichaam, HuL001, dat ENO1 herkent op zowel muis- als menselijke kankercellen. In celkweek en muismodellen verstoorde HuL001 de ondersteuning van MCT4 door ENO1, verminderde de lactaatafgifte en verschuifde macrophages weg van de tumorbevorderende M2-toestand naar een M1-toestand, die agressiever is tegen kanker en beter in het opruimen van tumorcellen. Belangrijk is dat HuL001 macrophages niet simpelweg doodde; in plaats daarvan heropvoedde het ze terwijl het direct de celdood van kankercellen verhoogde.
Bestraling effectiever maken
Wanneer HuL001 werd gecombineerd met radiotherapie in muismodellen van colorectale en triple-negatieve borstkanker, krompen tumoren meer, groeiden ze langzamer terug en verdwenen ze bij veel dieren volledig. 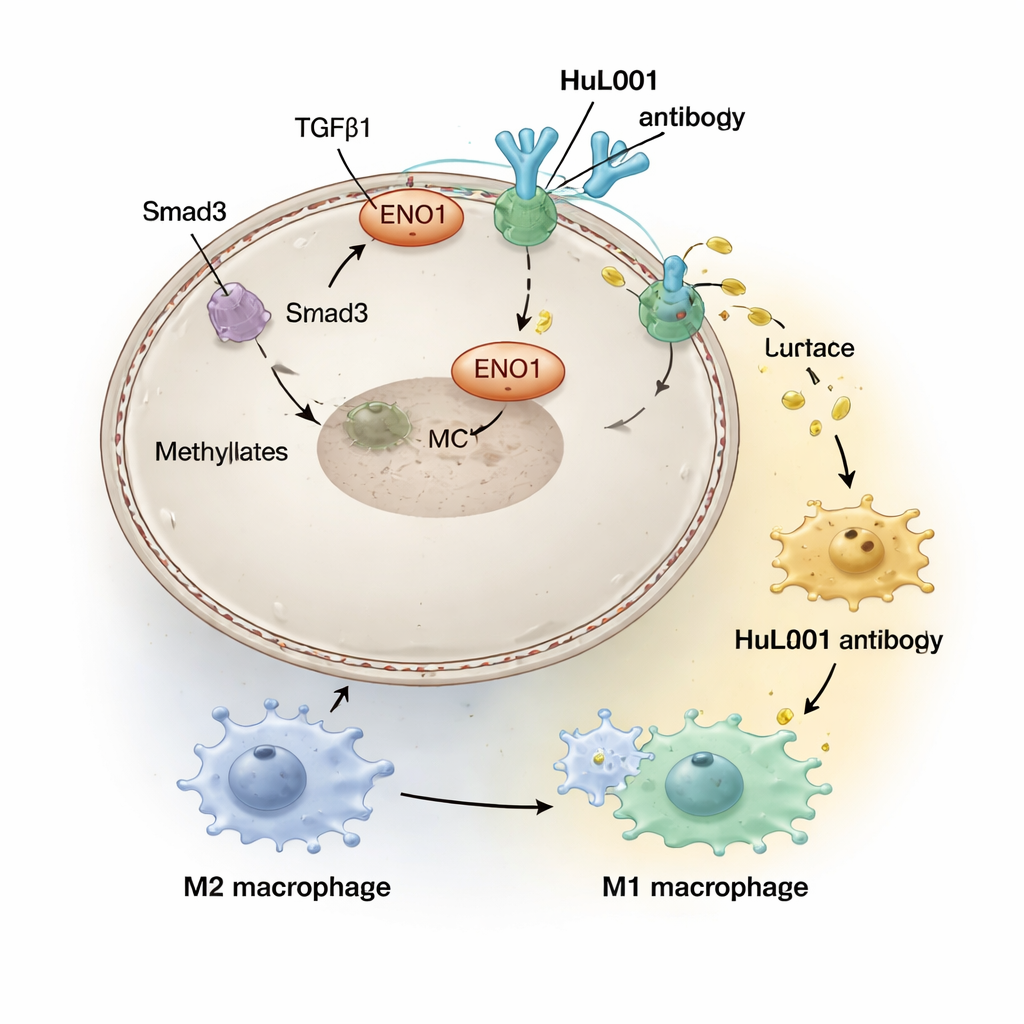
Van complexe paden naar praktische belofte
Voor niet-specialisten is de boodschap van deze studie dat de chemie van een tumor en zijn buurt van immuuncellen diep met elkaar verweven zijn. ENO1 staat op een kruispunt: het helpt tumoren suiker te verbranden, lactaat te exporteren en de verkeerde soort immuunhulp aan te trekken. Door oppervlak-ENO1 te blokkeren met een gericht antilichaam konden de onderzoekers schadelijke lactaatophopingen verminderen, macrophages van tumorghulpen naar tumorkrijgers draaien en radiotherapie effectiever maken in moeilijk te behandelen kankermodellen. Hoewel HuL001 nog geen klinisch geneesmiddel is, suggereert het werk dat het richten op metabole poortwachters zoals ENO1 een krachtige manier kan worden om de verdediging van een tumor tegen zichzelf te keren en bestaande therapieën zoals radiotherapie te versterken.
Bronvermelding: Lin, YS., Chang, HY., Hong, WZ. et al. Targeting ENO1 reprograms macrophage polarization to trigger antitumor immunity and improves the therapeutic effect of radiotherapy. Cell Death Dis 17, 194 (2026). https://doi.org/10.1038/s41419-026-08416-7
Trefwoorden: tumormetabolisme, macrophage-polarisatie, radiotherapie, immunotherapie, lactaat