Clear Sky Science · nl
Sec8: een nieuwe positieve regulator van RIG-I in de afweer tegen RNA-virussen
Hoe onze cellen sluwe virussen detecteren
Veel gevaarlijke virussen, waaronder influenza en opkomende dierlijke virussen, dragen hun genetisch materiaal in de vorm van RNA. Onze cellen vertrouwen op interne alarmsystemen om deze indringers snel op te merken en een antivirale respons te starten. Dit artikel onderzoekt een weinig bekend celproteïne genaamd Sec8 en laat zien dat het stilletjes een centrale rol speelt in het in leven en actief houden van een van onze belangrijkste virussensoren, RIG-I, lang genoeg om ons te beschermen.
Een cellulair inbraakalarm onder druk
RIG-I is een moleculair “inbraakalarm” dat binnenin cellen patrouilleert op zoek naar stukjes viraal RNA. Wanneer het verdacht RNA detecteert, verandert het van vorm, wordt geactiveerd en geeft signalen af die uiteindelijk type I-interferonen opwekken—krachtige waarschuwingsmoleculen die naburige cellen helpen resistent te worden tegen infectie en immuunverdedigingen activeren. Omdat een overactief alarm schadelijke ontsteking of auto-immuunziekte kan veroorzaken, houden cellen de RIG-I-niveaus nauwkeurig in bedwang. Verschillende andere eiwitten kunnen RIG-I markeren voor afbraak door kleine ubiquitineketens aan te hechten, waardoor het bij het cellulaire “versnipperaar”complex, het proteasoom, terechtkomt. Tot op heden was onduidelijk welke aanvullende cellulaire factoren RIG-I beschermen tegen voortijdige vernietiging, vooral tijdens actieve RNA-virusinfecties.
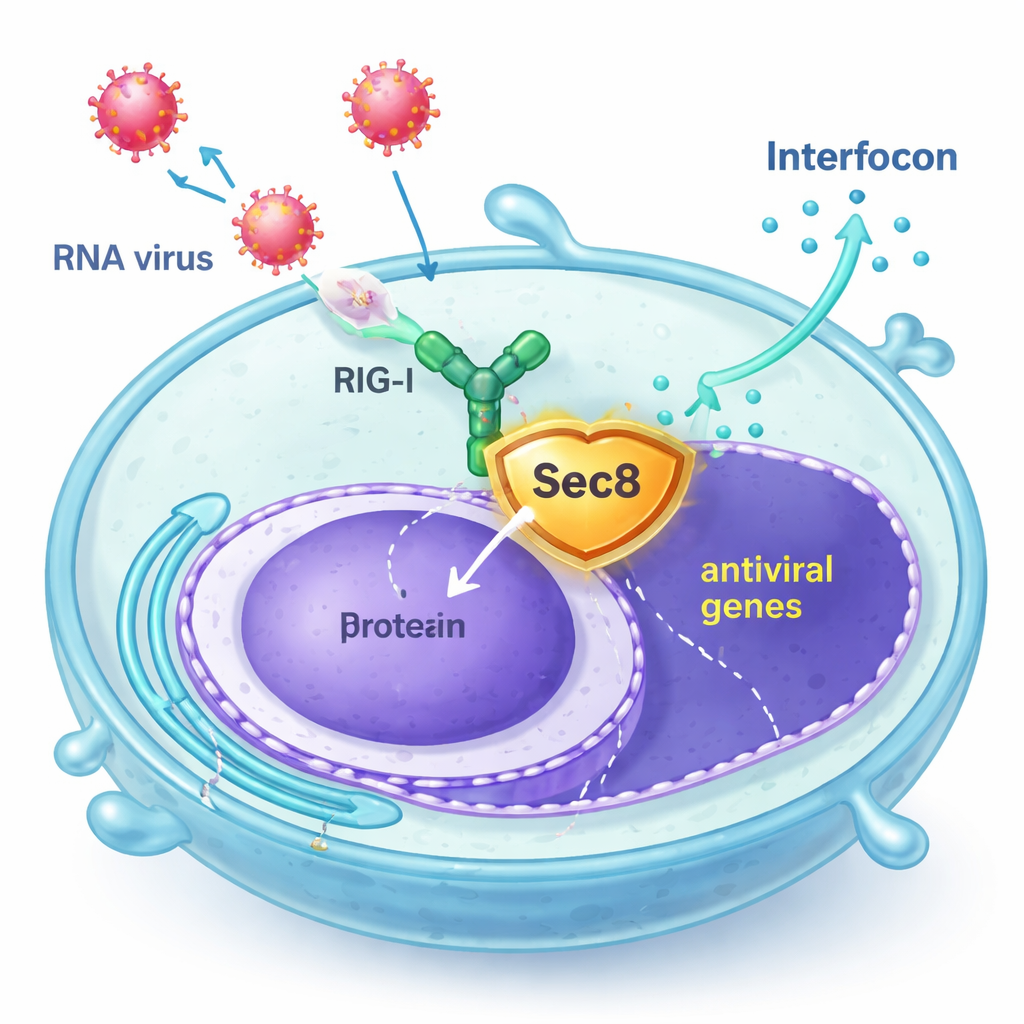
Sec8 treedt op als lijfwacht
De auteurs ontdekten dat Sec8, vooral bekend als onderdeel van een acht-eiwitcomplex dat secretievesikels helpt versmelten met het celoppervlak, eigenlijk antivirale signalering versterkt. In menselijke cellijnen en in primaire muisimmuuncellen leidde verhoogde Sec8-expressie tot sterkere activatie van interferon-gerelateerde genen na infectie met RNA-virussen zoals vesiculair stomatitisvirus (VSV) en Sendai-virus, of na blootstelling aan synthetisch viraal RNA. Omgekeerd leidde vermindering van Sec8 tot lagere productie van interferon en interferon-gestimuleerde genen, waardoor cellen minder goed in staat waren virale replicatie te weerstaan. Deze bevindingen suggereren dat Sec8 niet alleen in secretie werkt, maar ook fungeert als een positieve regulator binnen de antivirale alarmpathway.
De cellulaire versnipperaar blokkeren
Dieper graven leerde de onderzoekers dat Sec8 de expressie van het RIG-I-gen niet verhoogt; in plaats daarvan voorkomt het dat het RIG-I-eiwit wordt afgebroken. Wanneer Sec8 werd verwijderd, daalden de RIG-I-niveaus sneller, en dit verlies kon worden tegengegaan door medicijnen die het proteasoom blokkeren, wat de betrokkenheid van het eiwitrecyclingsapparaat van de cel impliceert. Het team identificeerde een ander eiwit, STUB1, als een sleutel ’tagger’ die een specifiek type ubiquitineketen (K48-verbonden) aan RIG-I hecht op een aminozuur genaamd lysine 190. Dit merkteken geeft RIG-I aan voor afbraak. Sec8 verstoort dit proces op twee manieren: het concurreert fysiek met STUB1 voor binding aan hetzelfde activatieregion op RIG-I, en het verlaagt de hoeveelheid STUB1 die de cel in de eerste plaats aanmaakt.
Sec8, p53 en de controle van de tagger
Om te verklaren hoe Sec8 de STUB1-productie vermindert, richtten de auteurs zich op genregulatie. Ze identificeerden een korte DNA-sequentie die fungeert als de kern-aanzet (promoter) voor het STUB1-gen en toonden aan dat het beroemde tumorremsende eiwit p53 aan dit gebied bindt en STUB1-niveaus verhoogt. Sec8 dempt zowel de hoeveelheid als de activerende fosforylering van p53, zodat p53 STUB1-productie niet langer zo effectief kan stimuleren. Wanneer p53 werd geblokkeerd of STUB1 werd uitgeschakeld, werden de schadelijke effecten van het verlies van Sec8 op interferonproductie en virusgroei grotendeels teruggedraaid. Dit plaatst Sec8 bovenaan een regulerende keten die loopt van p53 naar STUB1 en uiteindelijk naar de stabiliteit van RIG-I.
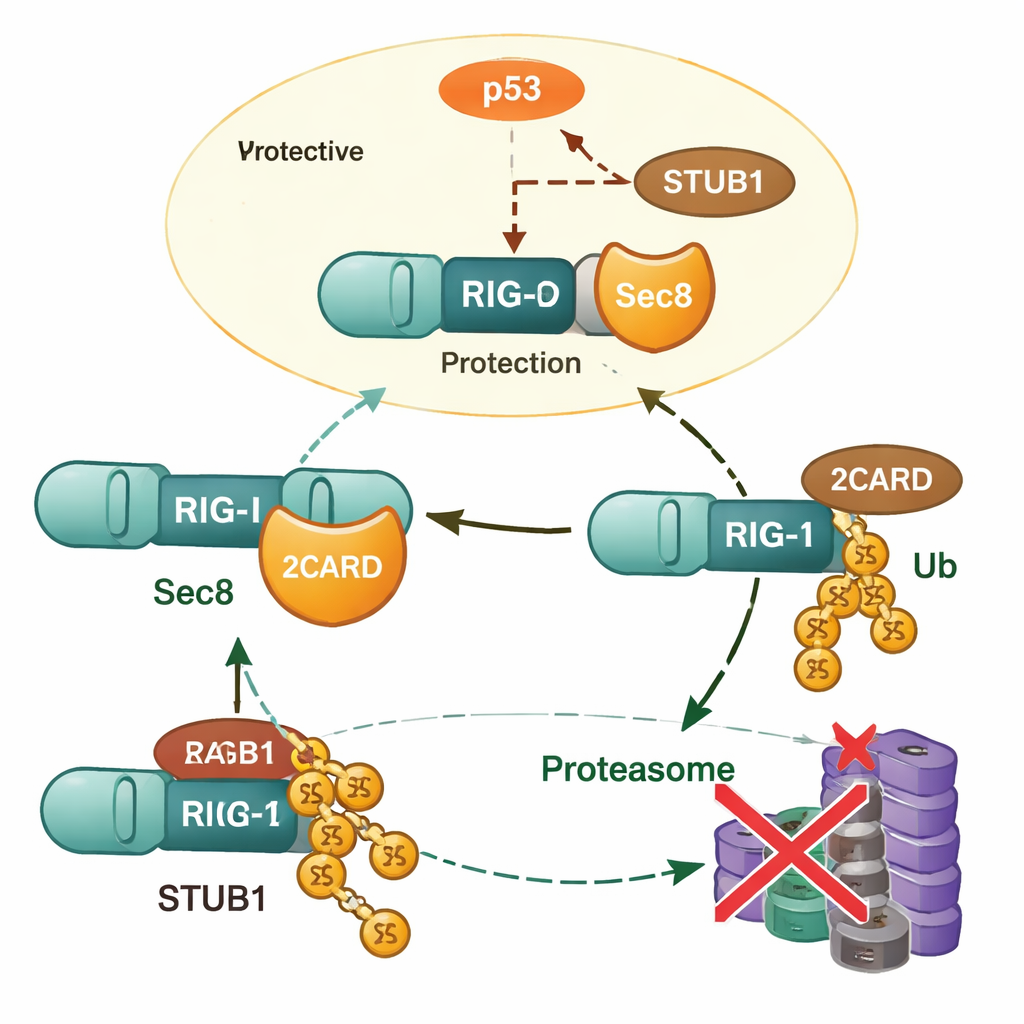
Van petrischaal naar levende dieren
Het team testte vervolgens het belang van Sec8 in muizen die zo waren ontworpen dat het Sec8-gen specifiek in bepaalde immuuncellen ontbrak. Na infectie met VSV produceerden deze dieren minder interferon, droegen ze hogere viuslasten in organen zoals milt, lever en longen, en vertoonden ze ernstiger longschade, groter gewichtsverlies en lagere overleving dan controlemuizen. Deze in vivo-resultaten bevestigden dat Sec8 geen marginale speler is maar een belangrijke beschermer tegen RNA-virusinfectie in een heel organisme.
Waarom dit belangrijk is voor toekomstige therapieën
Simpel gezegd toont deze studie aan dat Sec8 fungeert als een lijfwacht voor de antivirale sensor RIG-I. Door het ’tagger’eiwit STUB1 in toom te houden en RIG-I rechtstreeks te beschermen tegen verzending naar de cellulaire versnipperaar, maakt Sec8 het cellen mogelijk een tijdig interferonrespons op te bouwen en RNA-virussen beter te beheersen. Inzicht in deze nieuw beschreven p53–STUB1–RIG-I-as opent de deur naar toekomstige antivirale strategieën die RIG-I stabiliseren of Sec8’s beschermende handelingen nabootsen, wat mogelijk onze verdediging tegen een breed scala aan RNA-gebaseerde virusinfecties kan versterken.
Bronvermelding: Wang, L., Ma, W., Hou, P. et al. Sec8: a novel positive regulator of RIG-I in anti-RNA viral defense. Cell Death Dis 17, 165 (2026). https://doi.org/10.1038/s41419-026-08414-9
Trefwoorden: aangeboren immuniteit, RNA-virussen, RIG-I, ubiquitinering, interferonsignalering