Clear Sky Science · nl
Lactaatoverdracht van hypoxische tumorcellen bevordert macrophage‑senescentie en M2‑polariteit via de DNMT1‑NHE7‑as en versnelt zo de voortgang van endometriumcarcinoom
Waarom het tekort aan zuurstof voor tumoren ertoe doet
Endometriumcarcinoom, dat ontstaat uit het slijmvlies van de baarmoeder, komt wereldwijd steeds vaker voor. Veel gevorderde tumoren zijn moeilijk te behandelen omdat ze terugkeren, uitzaaien of resistent zijn tegen standaardtherapieën. Deze studie onderzoekt wat er binnen die tumoren gebeurt wanneer ze weinig zuurstof hebben — een veelvoorkomend kenmerk van snelgroeiende kankers — en toont aan hoe een eenvoudig afvalproduct, lactaat, nabije immuuncellen kan herprogrammeren zodat ze de kanker helpen groeien in plaats van bestrijden.
Weinig zuurstof verandert tumoren in lactaatfabrieken
Terwijl endometriumkankercellen zich delen, kan hun bloedvoorziening niet volgen, waardoor er gebieden met weinig zuurstof ontstaan, of hypoxie. De cellen reageren door een hoofdregelaar genaamd HIF1A aan te zetten die hun energieproductie herprogrammeert. In plaats van hoofdzakelijk te vertrouwen op efficiënte energieopwekking, verhogen de cellen glycolyse, een snelle maar inefficiënte route die grote hoeveelheden lactaat produceert. De onderzoekers analyseerden tumorgegevens van honderden patiënten en vonden dat hogere HIF1A‑niveaus samenhingen met verhoogde activiteit van veel glycolysegerelateerde genen en transporters die lactaat uit de kankercellen pompen. Patiënten van wie de tumoren meer HIF1A hadden, hadden doorgaans een slechtere prognose, wat suggereert dat deze metabole verschuiving nauw verbonden is met agressieve ziekte.
Hoe tumoraal afval behulpzame immuuncellen hervormt
Macrophagen zijn immuuncellen die, afhankelijk van hun toestand, tumoren kunnen aanvallen of juist ondersteunen. In dit werk toonde het team aan dat onder hypoxie endometriumkankercellen veel meer lactaat in hun omgeving loslaten. Dit lactaat wordt uitgescheiden via een transporter genaamd MCT3 op tumorcellen en vervolgens geïmporteerd in macrophagen via een andere transporter, MCT1. Eenmaal binnen duwt lactaat macrophagen weg van een verdedigende modus in de richting van de zogenaamde M2‑toestand, die geassocieerd wordt met weefselherstel, onderdrukking van ontsteking en, helaas, ondersteuning van tumorontwikkeling. In laboratoriumexperimenten vertoonden macrophagen die blootgesteld werden aan lactaatrijke tumorvloeistof meer markers van het M2‑type, en de door hen uitgescheiden vloeistof stimuleerde op haar beurt de groeisnelheid, migratie en invasie van kankercellen. 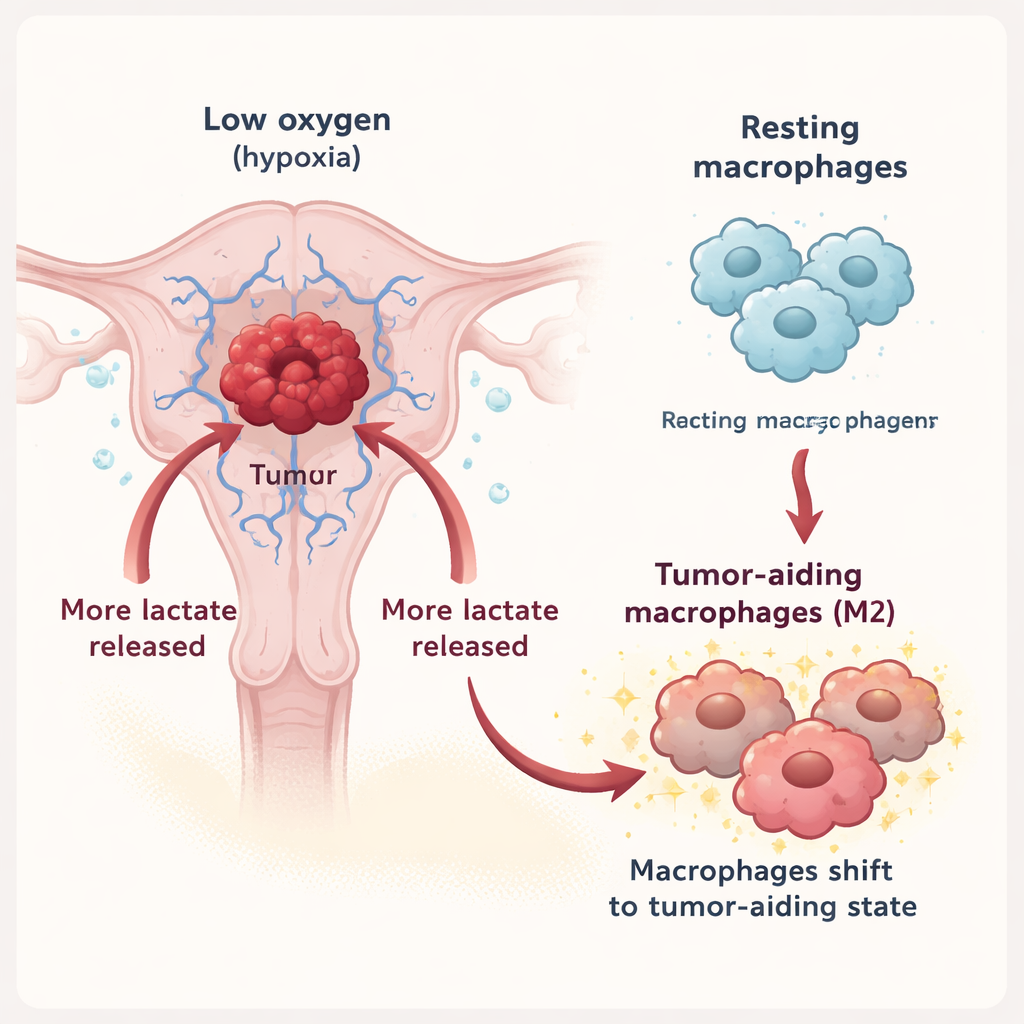
Een epigenetische schakelaar die een cellulaire “pH‑klep” stillegt
De studie gaat een stap verder door de moleculaire schakel in macrophagen bloot te leggen die tumoraal lactaat verbindt met dit schadelijke gedrag. Lactaat blijft niet alleen in de omgeving hangen; het kan histon‑eiwitten in de celkern wijzigen — een chemische markering bekend als lactylatie — die beïnvloedt welke genen aan of uit staan. De onderzoekers ontdekten dat lactaat een specifieke histonmarkering verhoogt in het controlegebied van het DNMT1‑gen, waardoor de activiteit daarvan toeneemt. DNMT1 is een enzym dat methylgroepen aan DNA toevoegt en genen kan uitschakelen. Een doelwit hiervan is NHE7, een eiwit dat helpt de zuurtegraad in bepaalde celcompartimenten te regelen. Wanneer DNMT1 wordt opgevoerd, verhoogt dat de methylatie van het NHE7‑gen, waardoor het minder actief wordt. Verminderde NHE7 verstoort de interne pH‑balans en activeert een signaalroute bekend als het MAPK‑pad. Dit pad duwt op zijn beurt macrophagen naar de tumorbevorderende M2‑toestand en een vorm van veroudering die senescentie wordt genoemd, waardoor ze vastgezet worden in een chronische, tumorstimulerende modus.
Van moleculaire kettingreactie naar sneller groeiende tumoren
Om te onderzoeken of deze keten van gebeurtenissen van belang is in levende organismen, creëerden de wetenschappers muismodellen waarin humane endometriumkankercellen samen werden gekweekt met mensachtige macrophagen. Wanneer extra lactaat werd toegevoegd, groeiden de tumoren groter, toonden ze meer delende cellen en bevatten ze meer M2‑type, senescente macrophagen met hoog DNMT1 en laag NHE7. Opvallend was dat wanneer de macrophagen zodanig werden gemodificeerd dat ze meer NHE7 produceerden, dit het tumorbevorderende effect van lactaat afzwakte: de tumoren waren kleiner, hadden meer afstervende cellen en bevatten minder M2‑ en senescente macrophagen. Het remmen van het DNMT1‑enzym of het MAPK‑pad verzwakte eveneens de mogelijkheid van lactaat om macrophagen te herprogrammeren, wat het idee versterkt dat deze moleculen een verbonden as vormen. 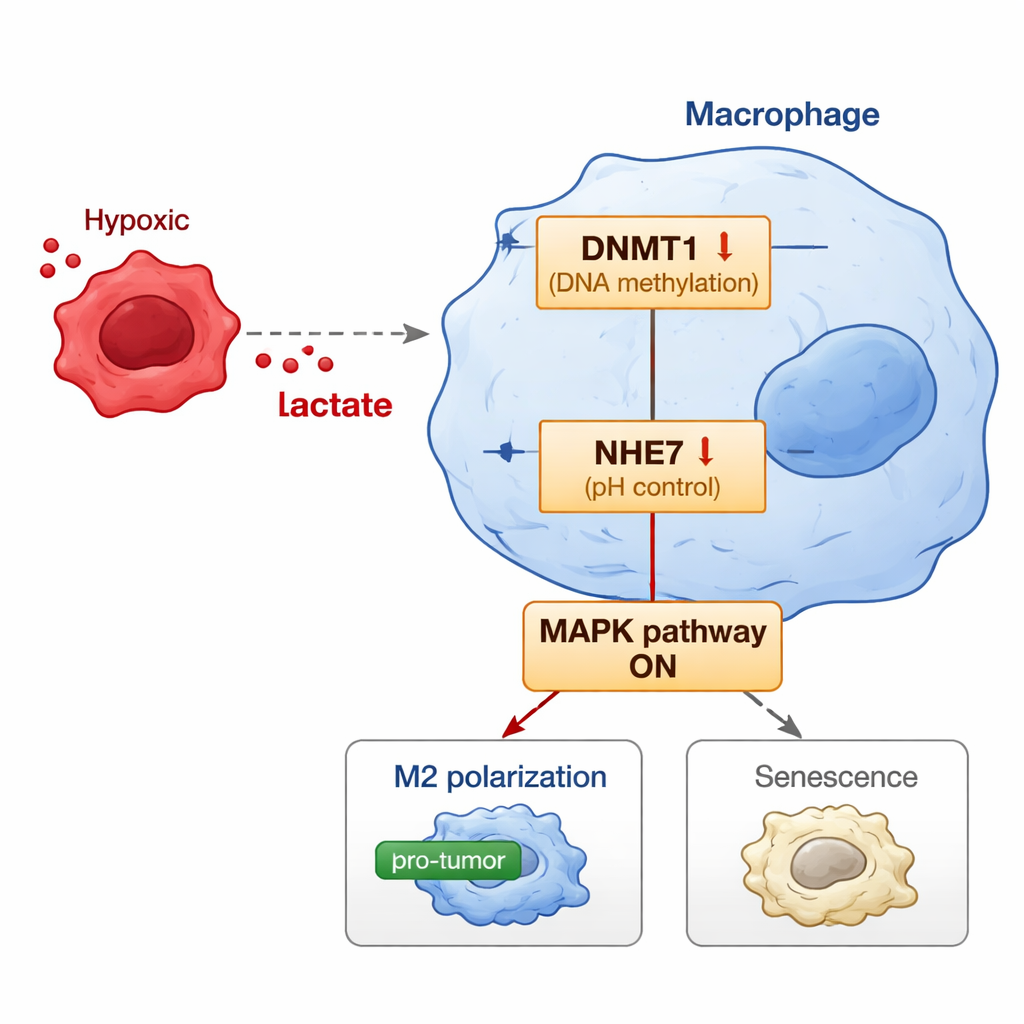
De trucs van een tumor als behandelbare doelen inzetten
Voor niet‑specialisten is de kernboodschap dat endometriumtumoren lage zuurstof en lactaat — ooit gezien als louter cellulaire restproducten — kunnen gebruiken om nabije immuuncellen te "hersenspoelen" zodat ze de kanker helpen. Ze doen dit via een epigenetische relais: lactaat verhoogt DNMT1, dat NHE7 uitschakelt, wat vervolgens signalering activeert die macrophagen vastzet in een tumorvriendelijke, verouderde staat. Door in te grijpen op een van de stappen in deze lactaat–DNMT1–NHE7–MAPK‑keten, kan het mogelijk zijn om een meer antitumorimmuunrespons te herstellen en de kankergroei te vertragen. Dit werk wijst op toekomstige therapieën die niet alleen de kankercellen direct aanvallen, maar ook de omgevingsexcellen heropvoeden waar de tumor van profiteert.
Bronvermelding: Yang, S., Ma, Y., Wu, T. et al. Lactate transmission from hypoxic tumor cells promotes macrophage senescence and M2 polarization via the DNMT1-NHE7 axis to accelerate endometrial cancer progression. Cell Death Dis 17, 185 (2026). https://doi.org/10.1038/s41419-026-08411-y
Trefwoorden: endometriumcarcinoom, tumormicro‑omgeving, lactaatmetabolisme, macrophage‑polarizatie, epigenetische regulatie