Clear Sky Science · nl
Spectrum en functies van ionkanalen en transporters in osteoclasten
Waarom onze botten kleine poortwachters nodig hebben
Ons skelet lijkt stevig en onveranderlijk, maar het wordt voortdurend afgebroken en opnieuw opgebouwd. Gespecialiseerde cellen, osteoclasten, fungeren als de sloopploeg en lossen oud bot op zodat nieuw bot kan ontstaan. Dit overzichtsartikel belicht een verborgen gezelschap microscopische “poortwachters” — ionkanalen en transporters — die geladen deeltjes en voedingsstoffen in en uit osteoclasten laten bewegen. Door te begrijpen hoe deze kleine poorten de botafbraak reguleren, hopen wetenschappers betere behandelingen te ontwikkelen voor osteoporose en andere botziekten.
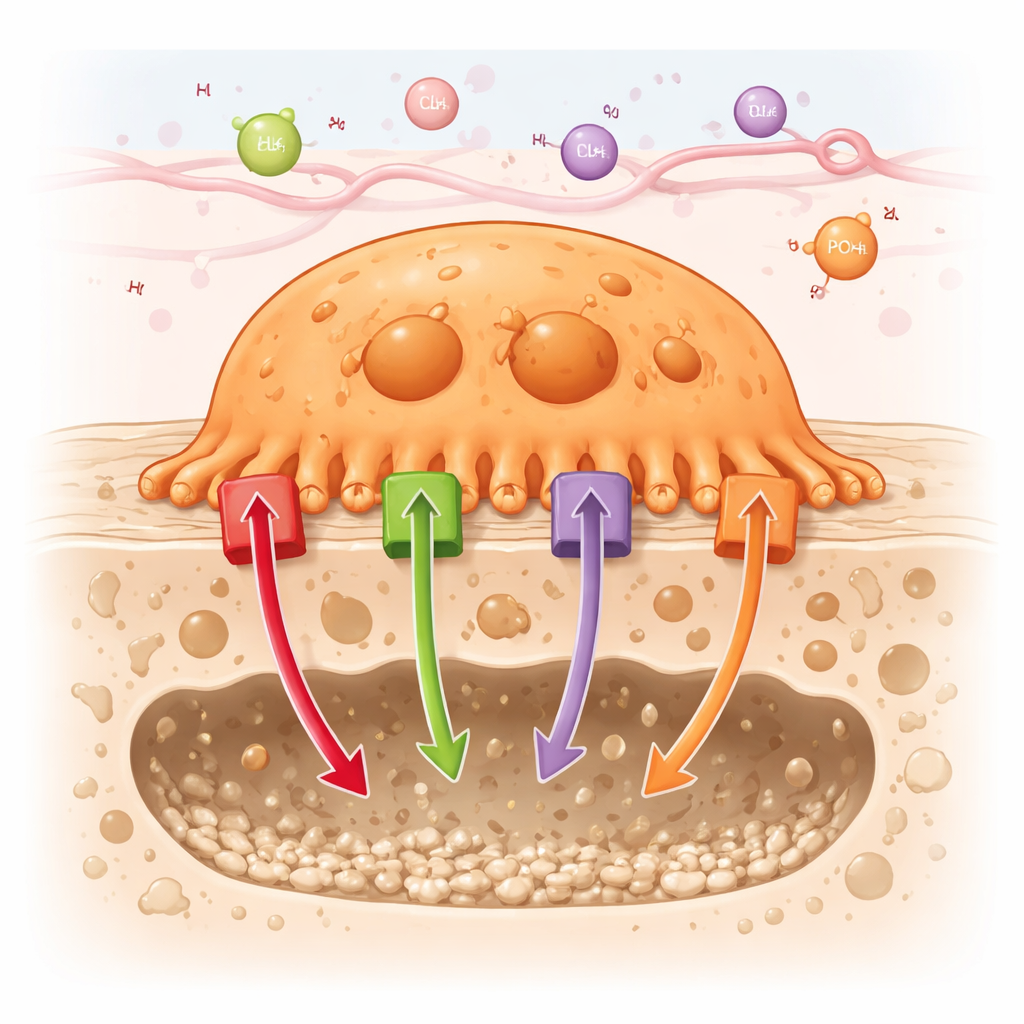
Hoe bot-etende cellen hun werk doen
Osteoclasten hechten zich stevig aan het botoppervlak en creëren een afgesloten holte waarin ze veilig mineraal kunnen oplossen en eiwitten kunnen verteren. Om deze miniatuurlijke “verteringskamer” extreem zuur te maken, pompen osteoclasten grote aantallen protonen (waterstofionen) in de holte. Tegelijkertijd verplaatsen ze andere ionen — zoals chloride, calcium en fosfaat — door hun membraanen en inwendige compartimenten. Het artikel behandelt ongeveer 90 verschillende kanalen en transporters die in osteoclasten worden aangetroffen en groepeert ze in zes families, waaronder energieg aangedreven pompen (ATPases), kation- en anionkanalen, gekoppelde transporters, voedingsstofdragers en ATP-bindende cassette (ABC)-transporters.
Zuur, zout en energie: de kernmachinerie
Twee proteinsystemen springen eruit als centraal voor botresorptie. Ten eerste drijven vacuolaire protonpompen, bekend als V-ATPases, actief protonen in de resorptieholte, waardoor die zuur genoeg wordt om botmineraal op te lossen en eiwitknippende enzymen te activeren. Specifieke V-ATPase-subunits, zoals a3, d2 en verschillende V1-componenten, zijn verrijkt bij de gerimpelde grens van de osteoclast en in lysosomen; genetische defecten in deze subunits kunnen leiden tot zwakkere botten of abnormale botverdikking. Ten tweede brengt een chloride–proton-uitwisselaar, ClC-7, die samenwerkt met een eiwit genaamd OSTM1, chloride-ionen in hetzelfde gebied. Dit balanceert de elektrische lading en maakt continue protonpompwerking mogelijk. Wanneer ClC-7 gemuteerd is, ontwikkelen mensen en muizen osteopetrose — een aandoening met te dichte maar broze botten — wat illustreert hoe essentieel correcte ionstroom is voor normale skeletgezondheid.
Calcium, fosfaat en andere ondersteunende spelers
Naast zuurproductie zijn osteoclasten afhankelijk van nauwkeurig gereguleerde calcium- en fosfaathandling. Een netwerk van calciumkanalen en -pompen in het celmembraan, het endoplasmatisch reticulum, lysosomen en mitochondriën genereert ritmische calcium“oscillaties” die sleutelgenen voor osteoclastvorming en fusie inschakelen. Transporters aan de gerimpelde grens en de tegenoverliggende zijde van de cel verplaatsen calcium en fosfaat uit opgelost bot, recyclen deze binnen de cel of geven ze terug aan de bloedbaan. Andere metalen en mineralen — zoals mangaan, magnesium, zink, koper en ijzer — worden eveneens gereguleerd door gespecialiseerde transporters en beïnvloeden hoe agressief osteoclasten bot resorberen. Bijvoorbeeld kunnen ijzer en bepaalde vormen van celdood die met ijzer samenhangen de osteoclastactiviteit verhogen of verlagen, terwijl zinktransporters vaak overmatig botverlies remmen.
Verkeersregeling binnen de cel
Ionkanalen zijn niet beperkt tot het buitenmembraan. Veel van deze kanalen bevinden zich op interne compartimenten zoals lysosomen, endosomen, het Golgi-apparaat en mitochondriën, en vormen een gelaagd transportnetwerk. Deze interne poorten helpen de pH in verteringsvesikels te bepalen, de energieproductie in mitochondriën te ondersteunen en het transport van enzymen en afvalstoffen te regelen. De review benadrukt hoe meerdere kanalenystemen samenwerken: natrium–waterstofwisselaars reguleren de interne zuurtegraad, kalium–chloride-cotransporters helpen het membraanpotentiaal en de chloridebalans te handhaven, en purinerge en mechanosensitieve kanalen vertalen chemische of mechanische signalen naar veranderingen in botresorptie. Voedingsstoffentransporters voor glucose, aminozuren, nucleosiden en vitamine C ondersteunen bovendien de hoge energie- en biosynthetische vraag van actief resorberende osteoclasten.
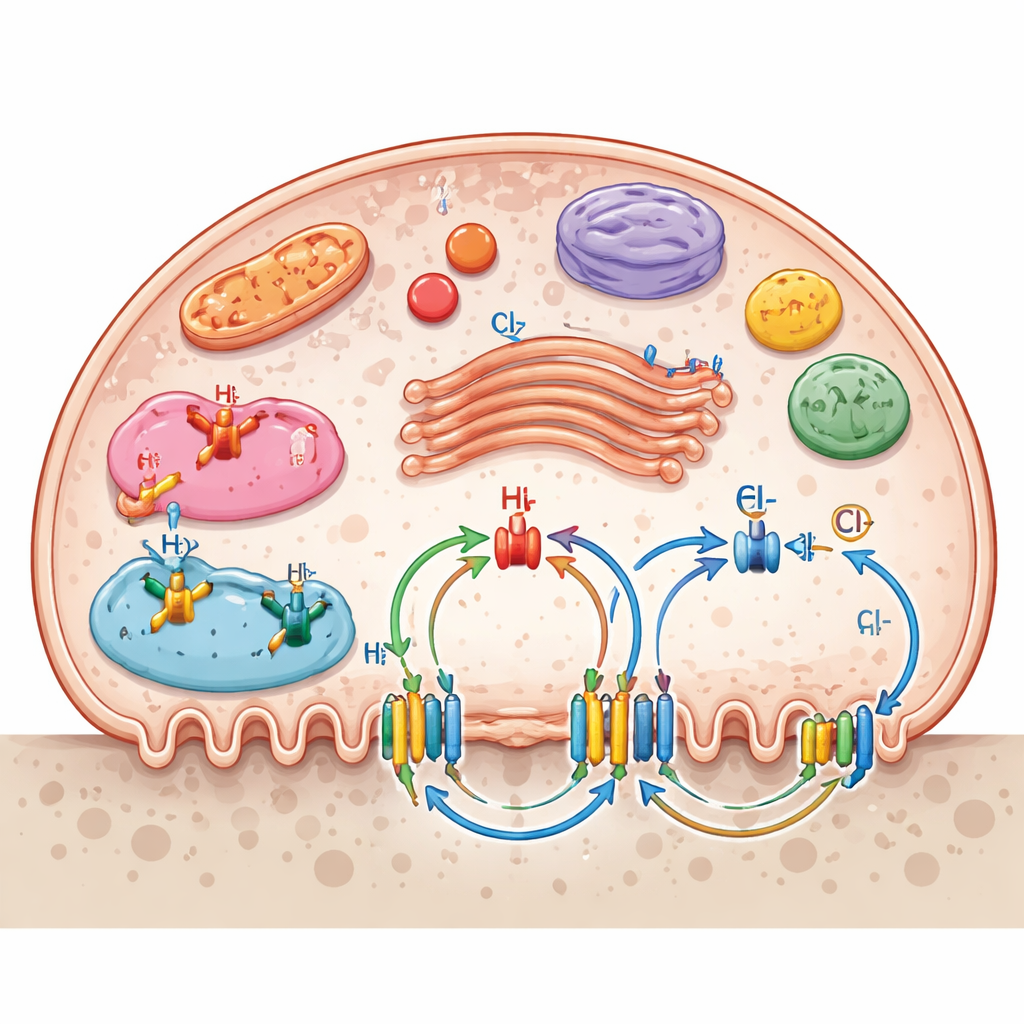
Van basale biologie naar nieuwe behandelingen
Aangezien veel botstoornissen ontstaan wanneer osteoclasten te actief of te weinig actief zijn, vormen de kanalen en transporters die hun gedrag sturen aantrekkelijke medicijndoelen. De auteurs bespreken bestaande en experimentele verbindingen die V-ATPases, TRP-calciumkanalen, chloridewisselaars, purinerge receptoren en andere transporters blokkeren, evenals nieuwere ideeën zoals het verstoren van specifieke subuniteinteracties of het gebruik van gerichte nanodeeltjes om geneesmiddelen direct naar bot te brengen. Ze benadrukken dat veel van deze eiwitten ook in andere weefsels voorkomen, waardoor het bereiken van echte osteoclast-specificiteit een uitdaging blijft. Toch zal, naarmate genomische en beeldvormingstechnieken meer onthullen over waar deze kanalen zitten en hoe ze met elkaar samenwerken, de uitbreidende “ionenkaart” van osteoclasten waarschijnlijk meer precieze therapieën opleveren voor osteoporose, inflammatoir botverlies en zeldzame genetische botziekten.
Bronvermelding: Chen, H., Zhang, Y., Zhu, Y. et al. Spectrum and functions of ion channels and transporters in osteoclasts. Bone Res 14, 35 (2026). https://doi.org/10.1038/s41413-026-00513-9
Trefwoorden: osteoclasten, ionkanalen, botresorptie, V-ATPase, osteoporose