Clear Sky Science · nl
PRMT6 is vereist voor het initiëren en versterken van door macrofagen geïnduceerde ontsteking bij heterotope ossificatie door verhoging van CCL2-expressie
Wanneer genezing te ver gaat
Soms probeert het lichaam na een ernstige verwonding of operatie zo hard te genezen dat het daadwerkelijk nieuw bot vormt op plaatsen waar dat niet hoort. Deze pijnlijke aandoening, waarbij ongewenst bot groeit in zachte weefsels, kan gewrichten verstijven, amputaties bemoeilijken en dagelijkse beweging lastig maken. Huidige behandelingen zijn beperkt en slagen er vaak niet in herhaling te voorkomen. Deze studie onthult een belangrijke vroege schakel in het immuunsysteem die trauma koppelt aan deze abnormale botvorming — en wijst op een korte, kritieke periode waarin gerichte behandeling het proces mogelijk kan stoppen voordat het begint. 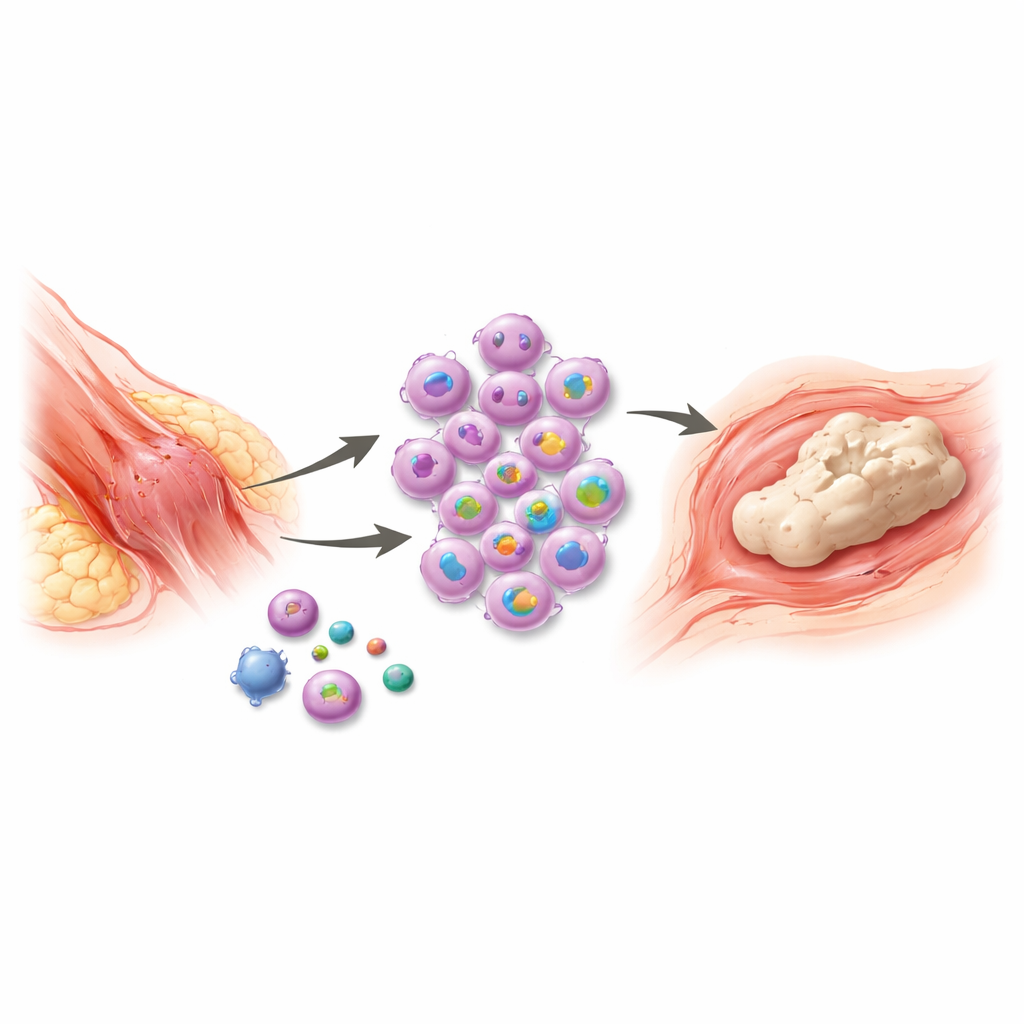
Het probleem van bot op de verkeerde plaats
Na zwaar trauma, zoals brandwonden, fracturen of orthopedische chirurgie, ontwikkelen sommige patiënten eilandjes van bot in spieren, pezen en andere zachte weefsels. Het nieuwe bot ontstaat via een proces dat lijkt op normale botontwikkeling, beginnend met ontsteking en eindigend met rijp, gemineraliseerd weefsel. Hoewel artsen weten dat immuuncellen die macrofagen heten centraal staan in deze reactie, was tot nu toe onduidelijk hoe zij stap voor stap ontsteking ontsteken en in stand houden. Zonder die kennis behandelen therapieën zoals ontstekingsremmers, bestraling of late chirurgische verwijdering vooral de consequenties, niet de oorzaak, en recidief komt vaak voor.
De sleutelmiddelaar van ontsteking
Met een muismodel dat peesletsel combineert met een brandwond — en daarmee ernstig trauma bij mensen goed nabootst — volgden de onderzoekers wat er in de tijd op de plaats van verwonding gebeurt. Ze zagen een snelle ophoping van macrofagen in de eerste dagen na het letsel, die vervolgens aanhield terwijl abnormaal bot vormde. Wanneer ze deze cellen uitputten, verdween het extra bot bijna volledig en toonde het omringende weefsel veel minder verstoring van bloedvaten en ondersteunende cellen. Een diepere genanalyse van het gewonde weefsel lichtte één molecuul in deze macrofagen uit: PRMT6, een enzym dat eiwitten modificeert en helpt bepalen welke genen worden aangezet.
Een moleculaire volumeknop voor ontsteking
Het team vond dat PRMT6-niveaus in macrofagen snel stegen na letsel en als reactie op waarschuwingssignalen en bacteriële componenten in het laboratorium. Muizen zonder PRMT6, of muizen waarin PRMT6 selectief alleen in macrofagen was verminderd, hadden veel minder macrofagen op de plaats van verwonding en ontwikkelden aanzienlijk minder abnormaal bot. Belangrijk is dat de gewonde pezen in deze dieren feitelijk beter genazen, met ordelijker weefsel en minder littekenvorming. Dit wijst erop dat PRMT6 niet nodig is voor gezonde reparatie, maar eerder als een volumeknop fungeert die schadelijke ontsteking versterkt. Toen de onderzoekers PRMT6 met een middel blokkeerden, werkte dat alleen als het vroeg werd gegeven — in de eerste weken na het letsel. Later beginnen met de behandeling had weinig effect, wat wijst op een smal maar krachtig therapeutisch venster. 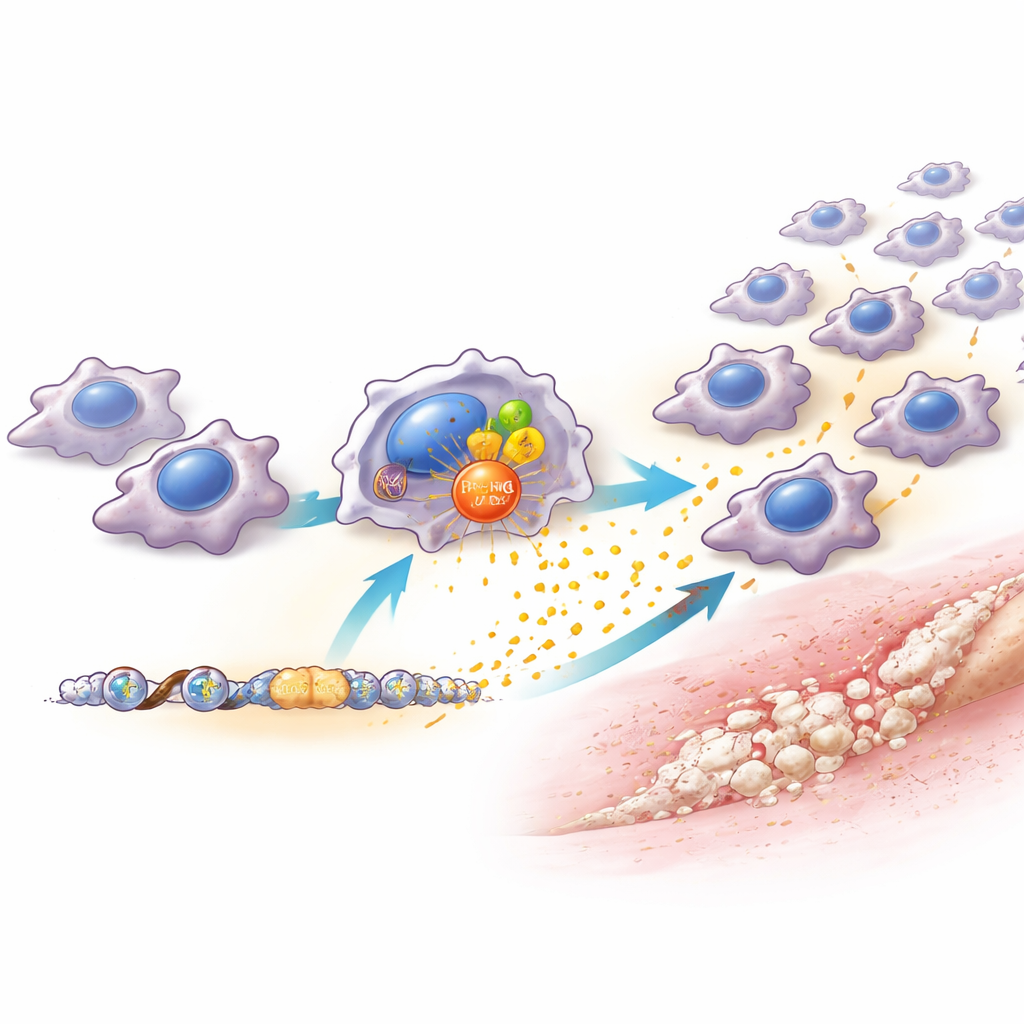
Hoe één signaal veel immuuncellen aantrekt
Om te begrijpen hoe PRMT6 dit effect veroorzaakt, bestudeerden de wetenschappers macrofagen in detail. Zonder PRMT6 produceerden deze cellen veel lagere hoeveelheden van verschillende chemische aantrekstoffen, vooral één genaamd CCL2, die normaal gesproken meer monocyten en macrofagen uit de bloedbaan naar beschadigd weefsel trekt. PRMT6 helpt het CCL2-gen op twee manieren aan te zetten: het werkt samen met de bekende ontstekingsregelaar NF-κB, en het markeert chemisch nabije DNA-verpakkingsproteïnen (histonen) zodat dat gen gemakkelijker afgelezen kan worden. Als gevolg pompen macrofagen met hoog PRMT6 meer CCL2 uit, trekken ze extra macrofagen aan en bouwen ze een “ontstekingscentrum” dat bloedvaten en botvormende voorlopercellen ondersteunt. Wanneer CCL2 specifiek alleen in macrofagen werd verminderd, leek de uitkomst sterk op het verlies van PRMT6 — minder macrofagen, zwakkere inflammatoire niches en minder extra bot. Het teruggeven van CCL2 herstelde gedeeltelijk zowel de instroom van macrofagen als de abnormale botvorming.
Een gerichte kans om ongewenst bot te voorkomen
Samengevat laat de studie zien dat PRMT6 in macrofagen fungeert als een vroege epigenetische versterker: het verhoogt een sleutelsignaal dat meer immuuncellen rekruteert, wat op zijn beurt botvorming op ongepaste plaatsen stimuleert. Omdat blokkering van PRMT6 alleen tijdens de vroege ontstekingsfase het ongewenste bot sterk verminderde terwijl normale peesgenezing intact bleef — en zelfs de weefselorganisatie verbeterde — biedt deze route een veelbelovende nieuwe strategie. In principe zou een korte, goed getimed toegediende behandeling gericht op PRMT6 na zwaar trauma of chirurgie langdurige invaliditeit door ectopisch bot kunnen voorkomen, zonder het natuurlijke vermogen van het lichaam om zichzelf te herstellen in gevaar te brengen.
Bronvermelding: Chu, W., Peng, W., Wu, Z. et al. PRMT6 is required for initiating and amplifying macrophage-induced inflammation in heterotopic ossification by increasing CCL2 expression. Bone Res 14, 29 (2026). https://doi.org/10.1038/s41413-026-00512-w
Trefwoorden: heterotope ossificatie, macrofagen, ontsteking, epigenetische regulatie, CCL2-signaal