Clear Sky Science · nl
TGF-β-geïnduceerde littekenvorming beperkt herstel na ruggenmergletsel
Waarom littekens in het ruggenmerg er toe doen
Wanneer het ruggenmerg ernstig beschadigd raakt, houden veel mensen blijvende verlamming of gevoelsverlies over omdat beschadigde zenuwvezels niet teruggroeien. Deze studie stelt een eenvoudige maar cruciale vraag: wat blokkeert die teruggroei precies — en kunnen we die barrière veilig wegnemen? Door te onthullen hoe een bepaald type litteken binnen het beschadigde merg ontstaat, wijzen de auteurs op een nieuwe manier om het zenuwstelsel bij herstel te helpen.
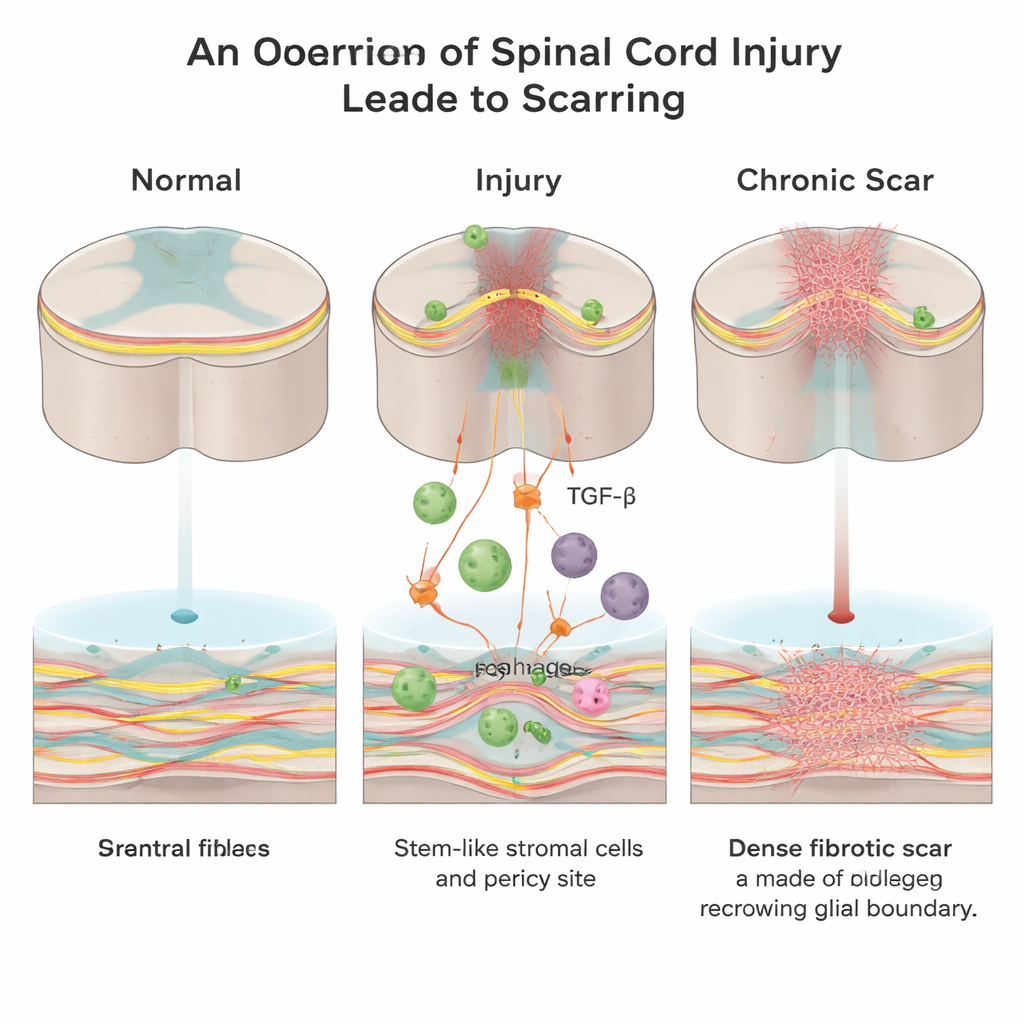
Een verborgen muur in de wond
Na een ruggenmergletsel haast het lichaam zich om de wond te sluiten. Er ontstaan twee belangrijke soorten littekenweefsel: een “gliaal” litteken gemaakt door ondersteunende cellen, astrocyten genoemd, en een “fibrotisch” litteken dat rijk is aan collageen, fibronectine en fibroblasten. Terwijl het gliale litteken mogelijk beschermende rollen vervult, vormt het fibrotische litteken een dichte fysieke en chemische barrière die groeiende zenuwvezels niet gemakkelijk kunnen passeren. Tot nu toe wisten wetenschappers veel minder over hoe deze fibrotische kern ontstaat en welke signalen de vorming ervan aansturen.
De rol van immuuncellen en een krachtig signaal
De onderzoekers werkten met volwassen muizen en concentreerden zich op een signaalmolecuul genaamd transforming growth factor‑beta (TGF‑β), dat helpt bij het coördineren van wondgenezing door het hele lichaam en vaak overactief is bij fibrotische aandoeningen. Zij ontdekten dat na ruggenmergletsel binnendringende immuuncellen, bekend als macrofagen, een belangrijke bron worden van actieve TGF‑β1 ter plaatse van de laesie. Deze toename van TGF‑β1 rekruteert lokale mesenchymale stromale/stamcellen en vaatgebonden cellen genaamd pericyten en zet ze aan tot transdifferentiatie naar fibroblasten — de cellen die het collageenrijke fibrotische litteken afzetten.
Het signaal dempen om een pad te openen
Om te testen of deze route daadwerkelijk schadelijke verharding veroorzaakt, gebruikte het team verschillende genetische ingrepen bij muizen. Wanneer ze macrofagen verwijderden, of het TGF‑β1-gen alleen in macrofaagafstammingscellen verwijderden, daalde de hoeveelheid fibrotisch weefsel in het beschadigde merg sterk en konden meer zenuwvezels en serotonine‑houdende banen de laesiezone oversteken. Evenzo verminderde het specifieke verwijderen van de TGF‑β‑receptor in pericyten hun reactie op TGF‑β, leidde tot minder collageenophoping en verbeterde beweging en sensatie in gedragsproeven. Belangrijk: pericyten en aanverwante stam‑achtige cellen bleven bestaan maar waren minder geneigd om scar‑vormende fibroblasten te worden.
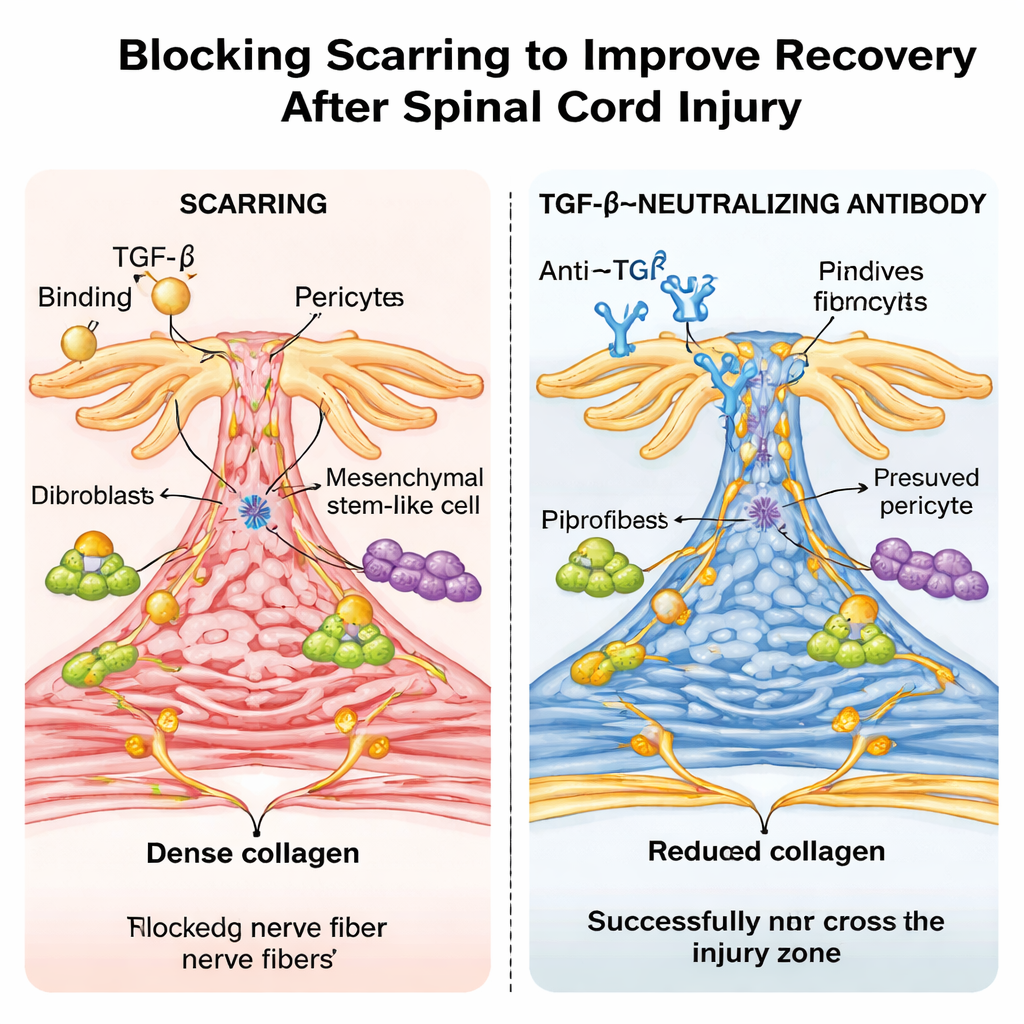
Een medicijnachtige antilichaambehandeling en een verrassend effect van leeftijd
De onderzoekers probeerden vervolgens een klinisch relevantere benadering: het behandelen van gewone muizen met een laboratoriumantilichaam dat TGF‑β neutraliseert. Herhaalde doses na het letsel verlaagden de actieve TGF‑β‑niveaus in bloed en ruggenmerg, verkleinden het fibrotische litteken en lieten zenuwvezels de laesie effectiever overbruggen, met duidelijke verbeteringen in lopen en sensorische functies. Single‑cell RNA‑sequencing bevestigde dat TGF‑β‑responsieve genen sterk actief waren in litteken‑vormende celtypen bij onbehandelde muizen en werden geremd door het antilichaam. Opvallend was dat wanneer dezelfde vorm van compressieletsel werd uitgevoerd bij pasgeboren muizen, de dieren vrijwel zonder fibrotisch litteken herstelden, er geen detecteerbare TGF‑β‑activatie op de beschadigingsplaats was en ze vrijwel normaal bewogen — vergelijkbaar met het littekenvrije herstel dat bij sommige niet‑zoogdieren voorkomt.
Wat dit kan betekenen voor toekomstige behandeling
Gezamenlijk suggereren de bevindingen dat overmatige activatie van TGF‑β na ruggenmergletsel nuttige herstercellen omleidt zodat ze een starre fibrotische muur bouwen die zenuwherstel en functioneel herstel blokkeert. Door deze overactivatie te voorkomen — hetzij door het richten op TGF‑β‑productie in macrofagen, het blokkeren van de receptor op pericyten en stromale cellen, of het gebruik van een neutraliserend antilichaam — kan het mogelijk zijn het schadelijke litteken te verminderen terwijl meer gunstige weefselresponsen behouden of zelfs versterkt blijven. Hoewel het vertalen van deze strategieën naar mensen zorgvuldig onderzoek vergt om bijwerkingen te vermijden, benadrukt dit werk dat TGF‑β‑gestuurde fibrotische littekenvorming een centrale en mogelijk met geneesmiddelen aan te pakken barrière vormt voor herstel van het ruggenmerg.
Bronvermelding: Pan, D., Wu, P., Noller, K. et al. TGF-β-induced fibrotic scar formation limits recovery of spinal cord injury. Bone Res 14, 27 (2026). https://doi.org/10.1038/s41413-026-00507-7
Trefwoorden: ruggenmergletsel, fibrotisch litteken, TGF-beta, macrofagen, zenuwregeneratie