Clear Sky Science · nl
HIF-1α en BMAL1 bij botregeneratie: wisselwerking tussen hypoxierespons en circadiaans ritme
Waarom gebroken botten beter genezen dan je denkt
Wanneer we een bot breken of een tand laten trekken, start ons lichaam geruisloos een opmerkelijk goed georkestreerd herstelproces. Diep in het beschadigde gebied daalt het zuurstofgehalte sterk en onze interne dag‑nachtklok blijft doortikken. Dit artikel onderzoekt hoe twee hoofdschakelaars—HIF‑1α, die lage zuurstof detecteert, en BMAL1, een kerncomponent van de klok—samenwerken om botcellen te leiden door ontsteking, nieuw weefselvorming en het herstel van uiteindelijke stevigheid. Inzicht in dit samenspel kan behandelingen voor fracturen, osteoporose, artritis en zelfs tandimplantaten verbeteren.
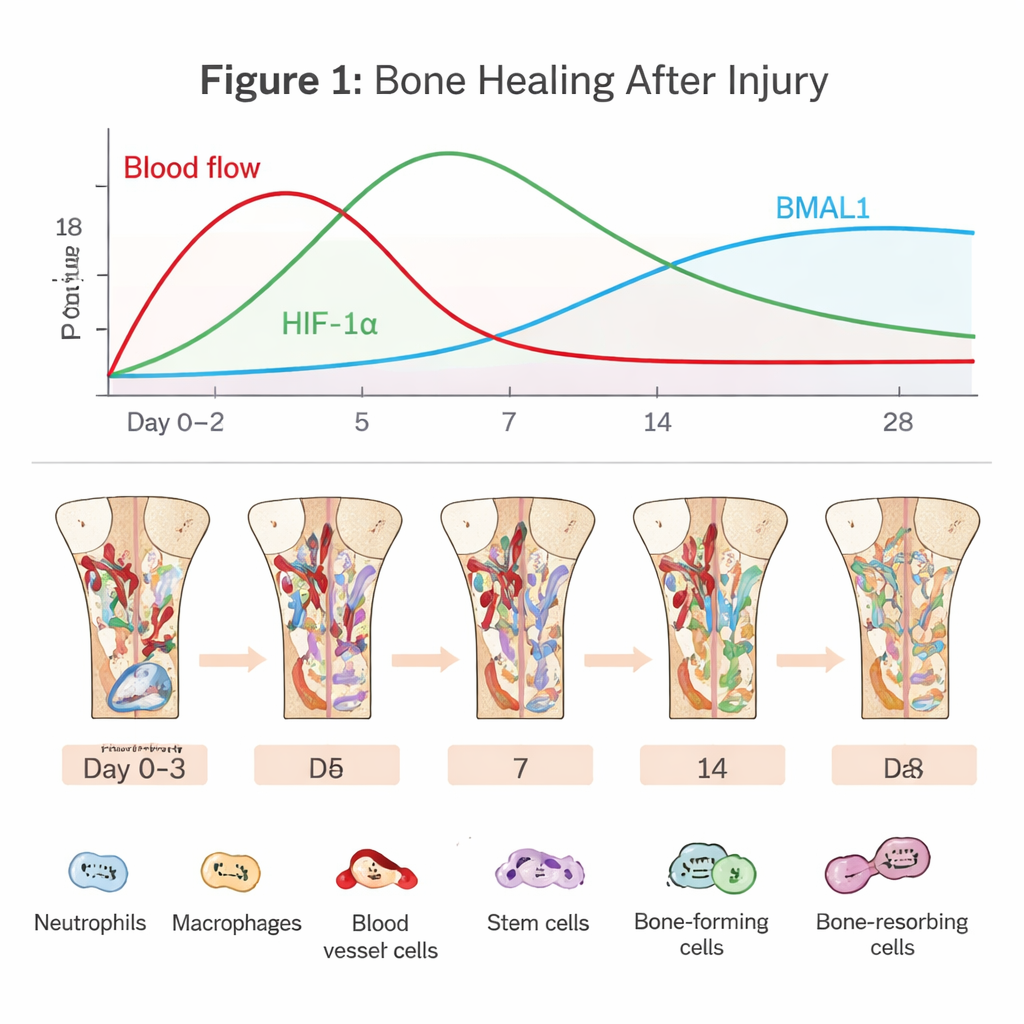
Het verborgen drama in een genezend bot
Botregeneratie begint op het moment dat bloedvaten scheuren. Er vormt zich een stolsel, waardoor een groot deel van de zuurstoftoevoer wordt afgesloten en een harde, zuurstofarme zone ontstaat. Immuuncellen zoals neutrofielen en macrofagen haasten zich naar binnen om afval op te ruimen en microben te bestrijden. Tegelijkertijd worden stamcellen uit het beenmerg en bloedvatcellen gerekruteerd om het gebied te herbouwen. Deze vroege “ontstekingsfase” is een tweesnijdend zwaard: een korte, tijdige ontstekingsreactie zet het herstel in gang, maar als die te lang aanhoudt of te hevig is, kan genezing stagneren of mislukken. Het artikel benadrukt dat het navigeren door dit smalle pad sterk afhangt van hoe cellen zuurstof en tijd waarnemen.
Hoe cellen lage zuurstof in hun voordeel gebruiken
In de zuurstofarme fractuurzone stabiliseert het eiwit HIF‑1α en schakelt genen aan die cellen helpen zich aan te passen. Het zet endotheelcellen aan tot het vormen van nieuwe bloedvaten, zodat verse zuurstof en voedingsstoffen het defect bereiken. Het herprogrammeert ook het celmetabolisme richting glycolyse, een manier om energie te maken die werkt als zuurstof schaars is. Voor stamcellen en botvormende osteoblasten kan matige activatie van HIF‑1α de proliferatie, migratie en botvorming stimuleren, deels door het verhogen van factoren zoals VEGF die bloedvatvorming koppelen aan nieuw bot. Maar als hypoxie te ernstig of te langdurig is, hopen stressmoleculen en reactieve zuurstofsoorten zich op, wat osteoblasten naar celdood kan duwen en botafbrekende osteoclasten kan stimuleren. Hetzelfde hypoxiesignaal kan dus genezing ondersteunen of saboteren, afhankelijk van intensiteit en duur.
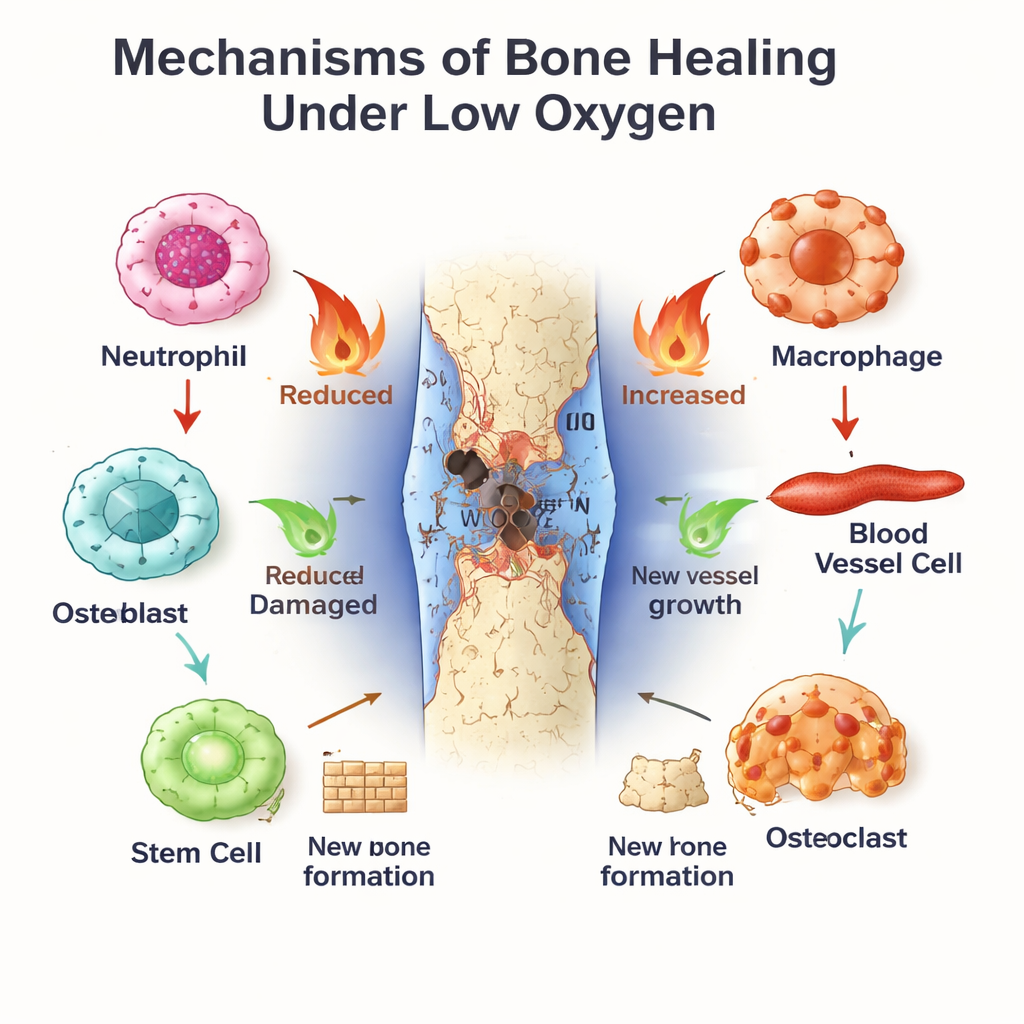
De interne klok van het lichaam als manager van botherstel
Parallel hieraan loopt de circadiane klok, een moleculaire tijdbewaarder aanwezig in bijna elke cel. BMAL1, een van de centrale componenten, helpt dagelijkse ritmes te bepalen in immuunactiviteit, bloedvatgedrag en stamceldifferentiaties. Neutrofielen en macrofagen vertonen tijd‑van‑de‑dag verschillen in hoe sterk ze op letsel reageren en hoe snel ze verouderen of overschakelen van een ontstekende (M1‑achtige) naar een herstellende (M2‑achtige) toestand. In bloedvatcellen en beenmergstamcellen bevordert BMAL1 gezonde proliferatie en ordelijke botvorming, deels door groeipaden zoals Wnt en TGF‑β/SMAD af te stemmen. Wanneer BMAL1 verstoord is—door genafwijkingen, ploegendienst of metabole ziekte—verliezen botten vaak massa, raken stamcellen uitgeput en verschuift de balans tussen botopbouw en afbraak richting verlies.
Een gesprek tussen zuurstofsensing en de biologische klok
De kern van het overzicht is de opkomende “wisselwerking” tussen HIF‑1α en BMAL1. Deze twee eiwitten delen vergelijkbare structuren en kunnen fysiek met elkaar interageren, zelfs gemengde paren vormen die aan DNA binden en overlappende genprogramma’s reguleren. De één kan de productie en stabiliteit van de ander beïnvloeden, waardoor terugkoppelingslussen ontstaan die de timing van het dag‑nachtritme koppelen aan de manier waarop cellen op hypoxie reageren. Samen beheren ze ook de cellulaire redoxbalans—hoeveel schadelijke reactieve zuurstofsoorten worden geproduceerd versus hoeveel antioxiderende capaciteit beschikbaar is—en co‑reguleren ze sleutelenzymen die bepalen of cellen meer vertrouwen op zuurstofafhankelijke ademhaling of zuurstofvrije glycolyse. Deze gezamenlijke controle helpt bepalen of de fractuuromgeving reconstrueren bevordert of juist leidt tot overmatige ontsteking en botresorptie.
Wat dit betekent voor ziekte en behandeling
Hetzelfde HIF‑1α–BMAL1‑partnerschap duikt op in veel botgerelateerde aandoeningen. Bij ploegendienstwerknemers veranderen verstoorde slaap en lichtblootstelling waarschijnlijk BMAL1, verhogen ze oxidatieve stress en verstoren ze HIF‑1α‑gestuurd herstel, wat bijdraagt aan osteoporose. Bij diabetes verzwakken hoge bloedglucosewaarden zowel klokfunctie als hypoxiesignalering, waardoor bloedvatgroei en stamcelgedreven botvorming ondermijnd worden. Bij artrose verstoort verlies van BMAL1 in kraakbeencellen hun ritme en hun beschermende relatie met HIF‑1α, wat kraakbeenslijtage versnelt. Rond titaniumimplantaten lijken gecontroleerde hypoxie en een gezonde circadiane ritme betere osseointegratie te ondersteunen, wat suggereert dat toekomstige implantaatcoatings mogelijk ontworpen kunnen worden om zowel HIF‑1α als BMAL1 voorzichtig te activeren. Over het geheel concludeert het artikel dat succesvolle botregeneratie niet alleen afhangt van welke cellen aanwezig zijn, maar van hoe ze zuurstof en tijd «lezen»—en dat het richten op deze dialoog nieuwe wegen kan openen naar sneller en sterker herstel.
Bronvermelding: Weng, Y., Xiong, J., Zhao, Q. et al. HIF-1α and BMAL1 in bone regeneration: crosstalk between hypoxia response and circadian rhythm. Bone Res 14, 25 (2026). https://doi.org/10.1038/s41413-026-00506-8
Trefwoorden: botregeneratie, circadiaans ritme, hypoxie, osteoporose, fractuurgenezing