Clear Sky Science · nl
Slimme biomaterialen voor herstel en regeneratie van verouderend skelet
Sterkere botten in een vergrijzende wereld
Veel mensen zien zwakkere botten en gewrichtspijn als onvermijdelijke aspecten van ouder worden. Wetenschappers ontwerpen echter nu "slimme" materialen die kunnen waarnemen wanneer en waar botten falen en die vervolgens helpen bij het zelfherstel. Deze materialen zijn bedoeld om fracturen betrouwbaarder te herstellen, osteoporose en artrose te vertragen of om te keren, en het aantal herhaalde operaties te verminderen—waardoor ouderen een betere kans krijgen om actief en zelfstandig te blijven.
Hoe botten verouderen en waarom ze gemakkelijker breken
Bot is een levend weefsel dat zichzelf voortdurend vernieuwt, maar met de leeftijd raakt dit evenwicht verstoord. Stamcellen in het beenmerg verschuiven van het vormen van botvormende cellen naar het maken van meer vetcellen; botopbouwende cellen raken uitgeput en botetende cellen worden overactief. De ondersteunende matrix van collageen en mineraal wordt droger en brozer, en het microscopische "steigersysteem" wordt dunner. Hormonale veranderingen, chronische laaggradige ontsteking, teveel reactieve zuurstofmoleculen en een plaatselijk zure omgeving zetten extra druk op het weefsel. Naar buiten toe uit zich dit in dunnere, meer poreuze botten, stijvere gewrichten, gekromde wervelkolom en een hoger risico op fracturen en aandoeningen zoals osteoporose en artrose.
Waarom de huidige behandelingen niet voldoende zijn
De belangrijkste huidige behandelingen bestaan uit geneesmiddelen die botverlies vertragen of botvorming stimuleren, samen met operaties en metalen of keramische implantaten om fracturen te stabiliseren of beschadigde gewrichten te vervangen. Deze benaderingen hebben veel levens gered maar hebben belangrijke nadelen. Systemische medicijnen bereiken vaak slechts een zeer klein deel van het botweefsel en kunnen bijwerkingen veroorzaken zoals kaakproblemen, bloedstolsels of zelfs een verhoogd kankerrisico bij langdurig gebruik. Stamceltherapieën laten belofte zien in diermodellen maar kampen met problemen rond overleving van cellen, onvoorspelbaar gedrag en het potentiële risico op tumorvorming. Conventionele implantaten bieden stevigheid maar zijn "domme" objecten: ze registreren hun omgeving niet, kunnen de afgifte van medicijnen niet aanpassen en kunnen falen in broos, ouder bot.
Slimme medicijndragers die het lichaam patrouilleren
Slimme biomaterialen brengen intelligentie in dit plaatje. Een belangrijke strategie is systemische "slimme toediening" van medicatie met behulp van nanodeeltjes of zachte gels die in de bloedbaan circuleren en alleen in probleemgebieden actief worden. Deze dragers kunnen zo worden gebouwd dat ze reageren op interne signalen zoals zuurgraad, hoge niveaus van schadelijke zuurstofsoorten of bot-oplossende enzymen; of op externe prikkels zoals licht, ultrageluid, warmte of magnetische velden. Bijvoorbeeld: sommige deeltjes blijven intact in normaal weefsel maar openen zich en geven hun medicijn vrij in zure, enzymrijke pockets waar overactieve osteoclasten bot afbreken. Andere ruimen overtollige reactieve zuurstof op terwijl ze langzaam een ontstekingsremmend middel afgeven, of dragen beeldgevingskleurstoffen zodat artsen in realtime kunnen zien waar ze naartoe gaan. Door meerdere triggers te combineren—bijv. zowel pH als oxidanten—kunnen onderzoekers de targeting verscherpen en bijwerkingen verminderen.
Lokale steigers die functioneren als tijdelijke slimme botten
Wanneer verouderde botten grote defecten of complexe fracturen hebben, kunnen lokale "slimme steigers" direct in het gat worden geïmplanteerd. Deze 3D-structuren, gemaakt van metalen, keramiek, polymeren of combinaties daarvan, zijn zo ontworpen dat ze overeenkomen met bot qua sterkte, porositeit en flexibiliteit. Hun sponsachtige architectuur laat bloedvaten en nieuw bot ingroeien, terwijl het materiaal geleidelijk oplost en wordt vervangen door het eigen weefsel van de patiënt. 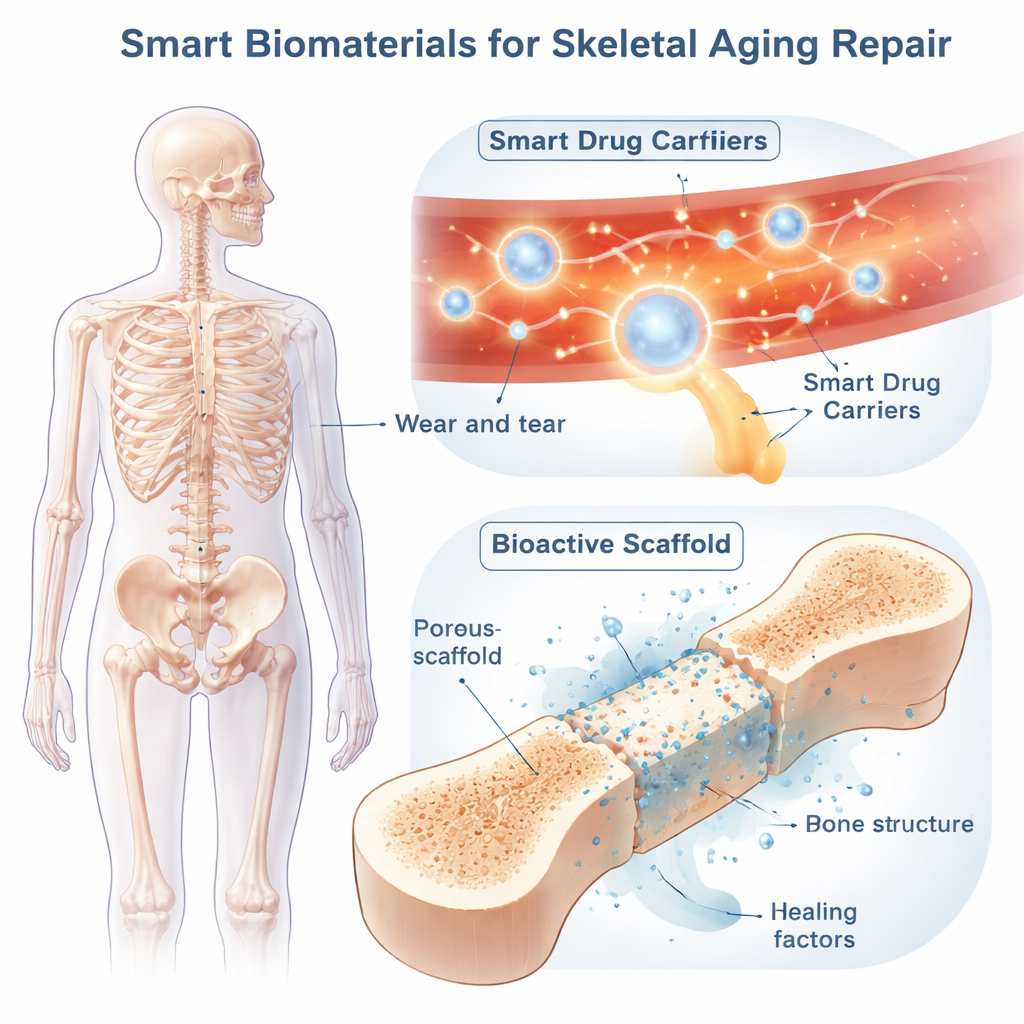
Van laboratorium naar kliniek: hulpmiddelen, obstakels en toekomstige richtingen
Om deze ingewikkelde systemen te maken gebruiken wetenschappers geavanceerde productietechnieken zoals 3D-printen en additive manufacturing om poriegrootte, stijfheid en medicijnlading met hoge precisie af te stemmen. Toch is het vertalen van slimme biomaterialen naar routinematige behandelingen een uitdaging. De meeste geïnjecteerde deeltjes hopen zich nog steeds op in organen zoals de lever en milt in plaats van in bot, en veel diermodellen vangen de complexiteit van verouderende mensen niet goed. Grootschalige productie, kwaliteitscontrole, toelating door regelgevende instanties en kosten blijven grote obstakels. Onderzoekers zien hoop in het combineren van slimme materialen met kunstmatige intelligentie om scaffoldontwerp en medicatiedosering te personaliseren, evenals in het toevoegen van ingebouwde sensoren die genezing kunnen volgen en de therapie automatisch kunnen aanpassen in een "closed-loop"-systeem. 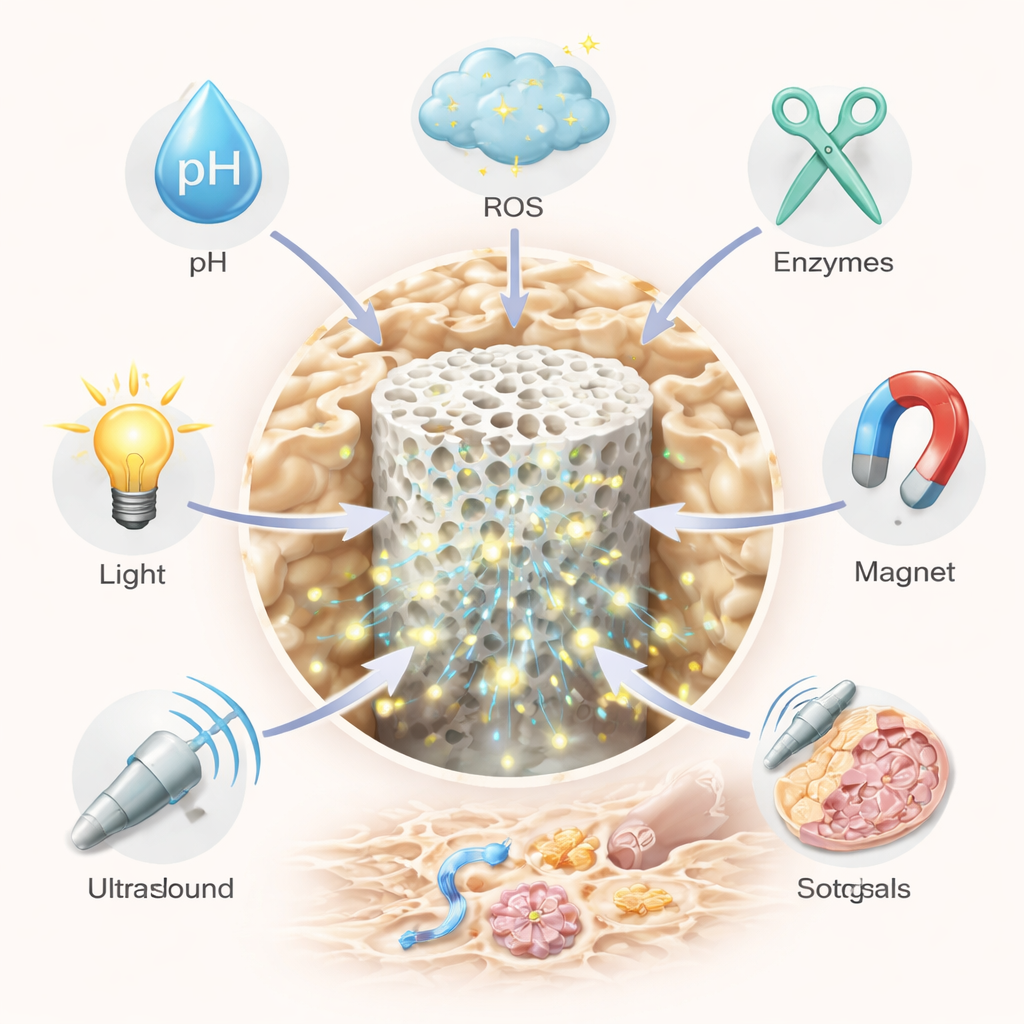
Wat dit voor patiënten zou kunnen betekenen
In wezen laat dit werk zien dat botfragiliteit op oudere leeftijd niet simpelweg een onomkeerbare aftakeling is, maar een complex technisch probleem dat mogelijk oplosbaar is. Slimme biomaterialen fungeren als kleine, programmeerbare reparatieteams: ze patrouilleren door de bloedbaan, nestelen zich in beschadigde plekken en geven precies vrij wat nodig is, wanneer dat nodig is, om botstructuur en functie te herstellen. Hoewel deze technologieën nog grotendeels in de onderzoeksfase verkeren, wijzen ze op een toekomst waarin fracturen sneller genezen, implantaten langer meegaan en therapieën zijn afgestemd op ieders unieke botbiologie—waardoor meer mensen mobiel en zelfstandig kunnen blijven tot ver in de ouderdom.
Bronvermelding: Liang, D., Wang, H., Jiang, Y. et al. Smart biomaterials for skeletal aging repair and regeneration. Bone Res 14, 24 (2026). https://doi.org/10.1038/s41413-026-00505-9
Trefwoorden: slimme biomaterialen, skeletveroudering, botregeneratie, osteoporose, stimuli-responsieve steigers