Clear Sky Science · nl
Astrocytaire APOE3-Christchurch-expressie verzacht amyloïde-β-pathologie in de hersenen van 5xFAD-muizen
Waarom deze hersenvariant van belang is
De ziekte van Alzheimer wordt vaak voorgesteld als een onstuitbare opeenhoping van schadelijke eiwitklonten in de hersenen. Toch lijken enkele mensen buitengewoon veerkrachtig te zijn en blijven ze scherp ondanks sterke genetische risico’s. Deze studie zoomt in op één zo’n beschermende variant in een veelvoorkomend gen dat cholesterol reguleert, en stelt een praktische vraag: als we de hersenen meer van deze beschermende versie geven — specifiek afkomstig van steunende cellen genaamd astrocyten — kunnen we dan Alzheimer-achtige veranderingen minder schadelijk maken?
Een beschermende genvariant in de schijnwerpers
Het werk concentreert zich op een zeldzame versie van het APOE-gen, genoemd APOE3-Christchurch. In een opmerkelijk praktijkgeval bleef een vrouw die een krachtige mutatie voor vroegbeginende Alzheimer droeg decennialang cognitief intact, en deze APOE-variant leek een belangrijke verklaring. Eerdere dierstudies suggereerden dat APOE3-Christchurch de verspreiding van een andere Alzheimer‑kenmerkende eiwit, tau, kan vertragen. Maar de invloed op amyloïde‑beta, het eiwit dat de klassieke plaque’s in Alzheimerhersen vormt, was nog niet volledig duidelijk. De onderzoekers wilden zien hoe deze variant zich gedraagt wanneer hij specifiek door astrocyten tot expressie wordt gebracht — de stervormige cellen die neuronen voeden en beschermen.
De variant testen in een Alzheimer‑achtig muismodel
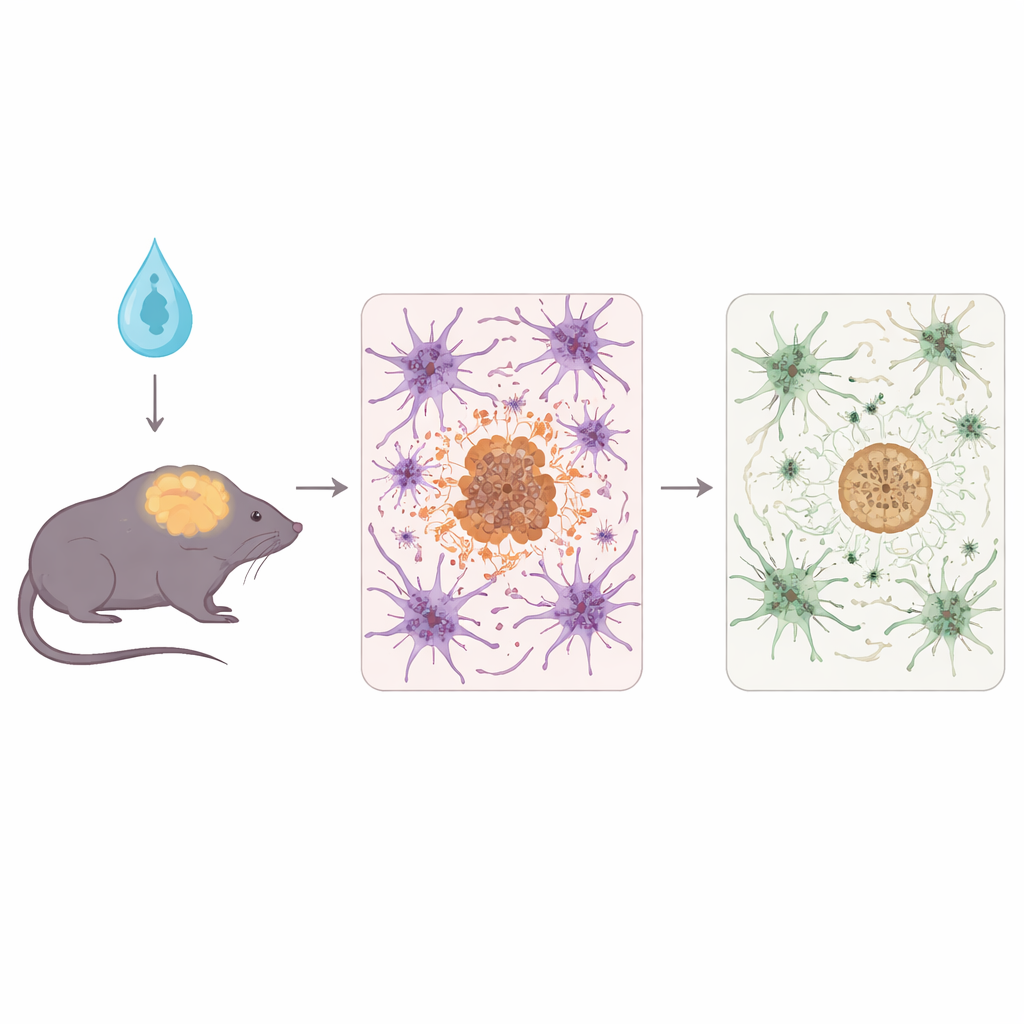
Om dit te onderzoeken gebruikten de onderzoekers 5xFAD‑muizen, een bekend model dat snel zware amyloïde‑ophopingen en bijbehorende hersenschade ontwikkelt. Kort na de geboorte kregen de muizen een onschadelijk virale vector waardoor hun astrocyten ofwel het reguliere menselijke APOE3, de beschermende APOE3‑Christchurch‑versie, of een neutraal controle-eiwit gingen maken. De wetenschappers analyseerden de dieren vervolgens in een gevorderd ziekte stadium en onderzochten hersenweefsel met biochemische testen, fluorescentiemicroscopie en RNA‑sequencing om te zien hoe amyloïde, nabije zenuwvezels en immuunreacties waren veranderd.
Maak plaques minder toxisch, niet alleen minder talrijk
Beide vormen van APOE geproduceerd door astrocyten verminderden de totale amyloïde‑plaque‑belasting en tekenen van schade rond die plaques vergeleken met controles. Maar APOE3‑Christchurch liet enkele belangrijke verfijningen zien. Het verschoof amyloïde naar meer compacte, bolvormige, fibrillaire plaques en verlaagde de niveaus van bepaalde oplosbare en oligomere vormen van amyloïde‑beta — soorten waarvan men denkt dat ze met name toxisch zijn voor synapsen. Neurieten, de dunne uitlopers van zenuwcellen nabij plaques, vertoonden minder vervorming en schade wanneer APOE3‑Christchurch aanwezig was. Tegelijkertijd waren de immuuncellen van de hersenen, microgliën en astrocyten, over het algemeen minder reactief, en transcriptome‑analyses toonden verzwakte immuun‑ en eiwit‑stresspaden, wat wijst op een rustigere, minder vijandige omgeving voor neuronen.
Aanwijzingen uit celculturen en genactiviteit
Om te bevestigen dat deze effecten niet beperkt bleven tot muizen, gebruikte het team ook uit menselijke stamcellen afgeleide astrocyten die waren aangepast om ofwel APOE3 of de Christchurch‑variant te dragen. Astrocyten met APOE3‑Christchurch scheidden meer APOE‑eiwit uit, en hun geconditioneerde medium verminderde de vorming van amyloïde‑beta‑oligomeren in een gecontroleerde reageerbuisproef. In muizenhersenen veranderde de expressie van APOE3‑Christchurch netwerken van genen die betrokken zijn bij eiwitvouwing, cellulaire stress en immuunsignalering, en verlaagde het niveaus van eiwitten die gekoppeld zijn aan stressreacties en verstoord lipidebeheer. Samen suggereren deze bewijslijnen dat APOE3‑Christchurch niet simpelweg de hoeveelheid amyloïde verandert — het verandert de vorm ervan en hoe hersencellen erop reageren.
Wat dit kan betekenen voor toekomstige behandelingen
Hoewel de hier waargenomen beschermende effecten bescheiden zijn en geen wonderen, zijn ze zeer informatief. De studie toont aan dat het versterken van APOE3‑Christchurch specifiek in astrocyten amyloïdeafzettingen compacter en schijnbaar minder toxisch kan maken, nabije zenuwschade kan verminderen en inflammatoire en stresssignalen kan dempen, zelfs zonder amyloïde volledig te verwijderen. Voor de niet‑specialist is de belangrijkste conclusie dat niet alle plaques even schadelijk zijn: het herschikken en neutraliseren ervan kan net zo belangrijk zijn als het verwijderen. Deze bevindingen ondersteunen het idee dat therapieën geïnspireerd op APOE3‑Christchurch — mogelijk geleverd via gentherapie of medicijnen die zijn werking nabootsen — de hersenen kunnen helpen beter samen te leven met amyloïde en mogelijk het verloop van de ziekte van Alzheimer kunnen vertragen of verzachten.
Bronvermelding: Raulin, AC., Alnobani, A., Rodriguez-Martinez, P. et al. Astrocytic APOE3-Christchurch expression ameliorates brain amyloid-β pathology in 5xFAD mice. Transl Psychiatry 16, 224 (2026). https://doi.org/10.1038/s41398-026-04002-9
Trefwoorden: Ziekte van Alzheimer, APOE3-Christchurch, amyloïde-beta, astrocyten, gentherapie