Clear Sky Science · nl
MicroRNA-132/212 moduleert opioïdebeloning negatief door de dopaminetransporter in het ventrale tegmentale gebied te richten
Waarom dit onderzoek van belang is voor het dagelijks leven
Opioïde pijnstillers en verwante middelen kunnen verlichting bieden, maar brengen ook een ernstig risico op verslaving met zich mee. Deze studie kijkt onder de motorkap van het beloningssysteem in de hersenen om kleine genetische schakelaars te identificeren die beïnvloeden hoe sterk opioïden als belonend worden ervaren. Door deze schakelaars te begrijpen, hopen wetenschappers slimmere behandelingen te ontwerpen die pijn verlichten of afhankelijkheid beperken zonder de pleziercircuits van de hersenen te kapen.
Kleine moleculen met grote invloed
Onze hersenen vertrouwen op een chemische stof genaamd dopamine om plezier te signaleren en ons te motiveren belonende ervaringen na te streven, van lekker eten tot verslavende drugs. De sterkte en duur van dit signaal worden deels geregeld door een eiwit dat de dopaminetransporter heet, dat fungeert als een stofzuiger die dopamine terug de zenuwcellen in zuigt. De auteurs richtten zich op twee zeer kleine stukjes genetisch materiaal, microRNA-132 en microRNA-212, die de productie van specifieke eiwitten kunnen terugschakelen. Eerder werk koppelde deze microRNA's aan cocaïnegebruik en stress. Hier vroeg het team of ze ook bepalen hoe de hersenen reageren op opioïde medicijnen, in het bijzonder morfine.
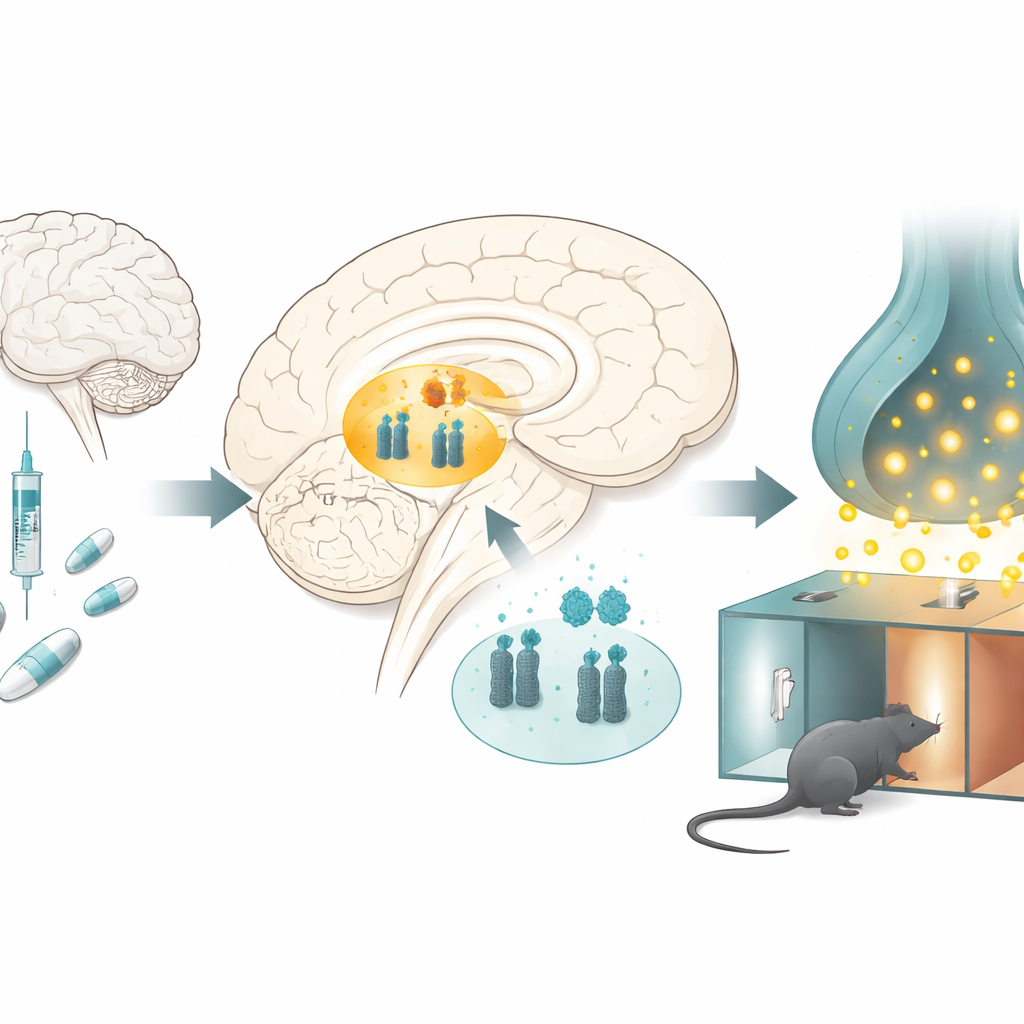
Hoe opioïden het beloningscentrum van de hersenen veranderen
De onderzoekers bestudeerden ratten die herhaalde doses morfine kregen in een klassieke test voor drugbeloning, waarbij dieren leren een kamer te verkiezen die geassocieerd is met het middel. Na enkele dagen brachten de morfine-behandelde ratten meer tijd door in de morfine-gepaarde kamer, wat aantoont dat het middel belonend werd. Toen de wetenschappers een belangrijk beloningsgebied diep in de hersenen onderzochten, het ventrale tegmentale gebied, vonden ze een opvallend patroon: de niveaus van microRNA-132 en microRNA-212 waren verlaagd, terwijl de niveaus van de dopaminetransporter verhoogd waren. Vergelijkbare veranderingen verschenen wanneer ratten morfine ontvingen zonder de plaats-leertaak, wat suggereert dat chronische blootstelling aan het middel zelf deze moleculaire balans verschuift.
Een directe moleculaire link aanwijzen
Om te zien of deze microRNA's daadwerkelijk de dopaminetransporter regelen, ging het team aan de slag met mensachtige zenuwcellen in het laboratorium. Door kunstmatig microRNA-132 of microRNA-212 te verhogen, zagen ze een daling zowel in het genetische bericht als in het eiwit van de transporter. Het blokkeren van de microRNA's had het tegenovergestelde effect. Ze bouwden vervolgens een rapportconstruct waarbij een lichtproducerend enzym gekoppeld was aan de regulerende staart van de transporter. Het toevoegen van de microRNA's dempte het lichtsignaal, maar dit effect verdween toen een paar sleutelbasen in de bindingsplaats gemuteerd werden. Samen toonden deze experimenten aan dat microRNA-132 en microRNA-212 rechtstreeks aan het boodschapper-RNA van de transporter binden en diens productie onderdrukken.
Van moleculen naar dopaminelevels en gedrag
Vervolgens onderzochten de onderzoekers hoe deze moleculaire controle zich uit in levende hersencellen. In gekweekte zenuwcellen verminderde het verhogen van de microRNA's de opname van dopamine, terwijl het blokkeren ervan de dopamine‑schoonmaak verbeterde. Wanneer ze kunstmatig de niveaus van de dopaminetransporter verhoogden of verlaagden, nam de invloed van de microRNA's overeenkomstig toe of af, wat bevestigt dat de transporter de belangrijkste tussenpersoon is. In levende ratten leidde het verhogen van microRNA-132 in het ventrale tegmentale gebied tot hogere dopamineconcentraties die naar verbonden regio's overstroomden, wat wijst op zwakkere transporteractiviteit. Gedragsmatig zorgden virale hulpmiddelen die microRNA-132 of microRNA-212 in dit hersengebied ‘opslokten’ ("spongen") ervoor dat ratten een sterkere voorkeur voor morfine leerden, samen met hogere transporterniveaus. Omgekeerd verlaagde het geforceerd extra inbrengen van microRNA-132 in hetzelfde gebied de transporterniveaus en verminderde de morfinevoorkeur bij mannelijke, vrouwelijke en adolescenten dieren, zonder de beweging of het genot van natuurlijke beloningen zoals suikerwater te beïnvloeden.
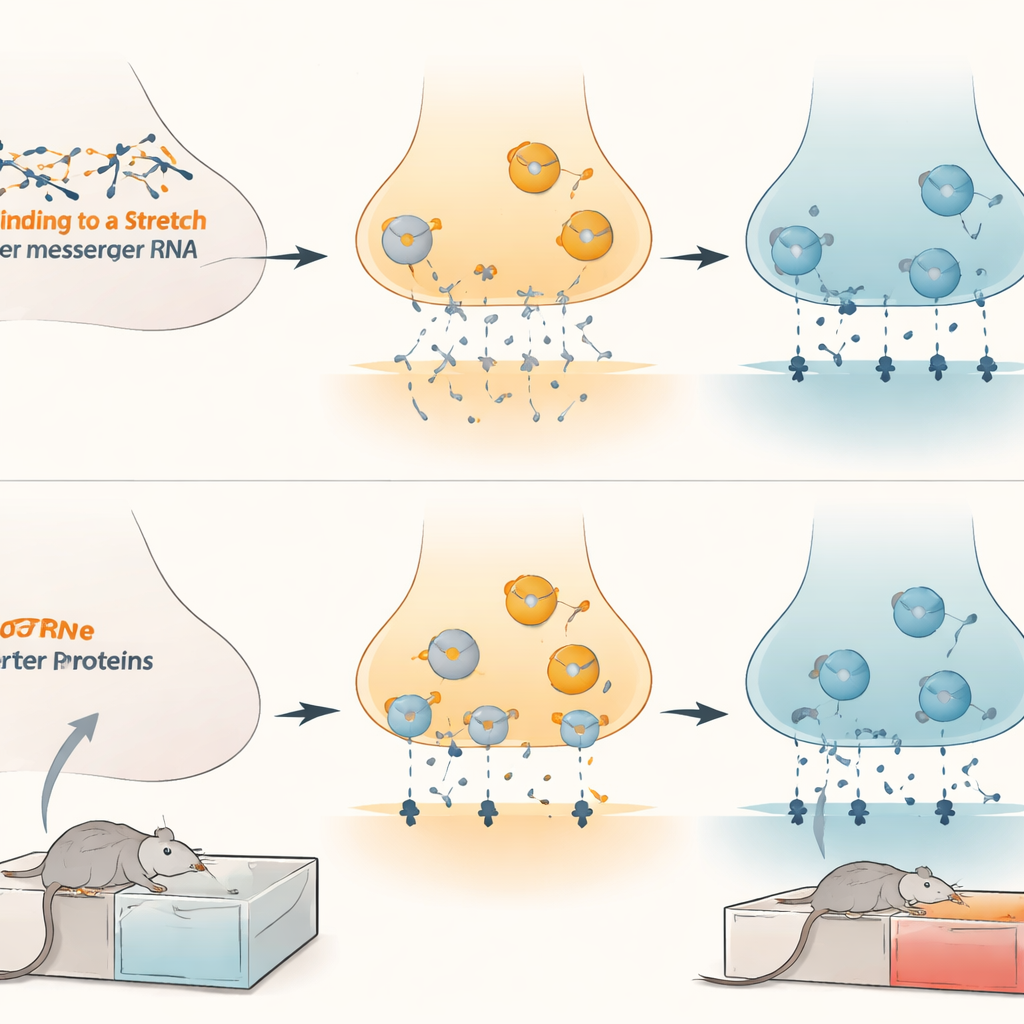
Implicaties voor de behandeling van opioïdeverslaving
Deze bevindingen onthullen een fijn afgestemd remsysteem binnen de beloningscircuitry van de hersenen: microRNA-132 en microRNA-212 houden de dopaminetransporter in toom en bepalen hoe sterk opioïden als belonend worden ervaren. Chronische morfine lijkt deze rem los te laten door de microRNA's te verlagen, waardoor de transporterniveaus stijgen en druggerelateerde beloningssignalen worden geconsolideerd. Door de werking van deze microRNA's specifiek in het ventrale tegmentale gebied te herstellen of na te bootsen, kan het mogelijk zijn de greep van opioïdebeloning te verzachten zonder breed plezier of beweging te onderdrukken. Hoewel er nog veel werk nodig is voordat dergelijke strategieën bij mensen getest kunnen worden, wijst deze studie op een nieuwe, zeer gerichte route voor toekomstige behandelingen die verslaving op het niveau van de moleculaire knoppen van de hersenen aanpakken.
Bronvermelding: Meng, J., Li, Z., Zhang, Y. et al. MicroRNA-132/212 negatively modulates opioid reward by targeting dopamine transporter in the ventral tegmental area. Transl Psychiatry 16, 152 (2026). https://doi.org/10.1038/s41398-026-03915-9
Trefwoorden: opioïdeverslaving, dopaminetransporter, microRNA-132, ventraal tegmentaal gebied, morfinebeloning