Clear Sky Science · nl
Lage concentraties amyloid-bèta-oligomeren veroorzaken synaptogenese kenmerkend voor milde cognitieve stoornissen en veranderen het de novo-proteoom
Vroege veranderingen die geheugenproblemen kunnen aankondigen
Voordat de ziekte van Alzheimer het geheugen aantast, gaat de hersenen door een vaag tussenstadium dat bekendstaat als milde cognitieve stoornis. In deze fase zijn de denkproblemen merkbaar maar het dagelijks leven gaat vaak gewoon door. Vreemd genoeg tonen sommige hersengebieden in dit stadium meer, en niet minder, verbindingen tussen zenuwcellen. In deze studie onderzoeken de onderzoekers of kleine hoeveelheden van een toxisch Alzheimer-gerelateerd molecuul deze uitbarsting van nieuwe verbindingen kunnen veroorzaken, en of een middel dat al bij kankerpatiënten is getest deze zeer vroege veranderingen kan dempen.
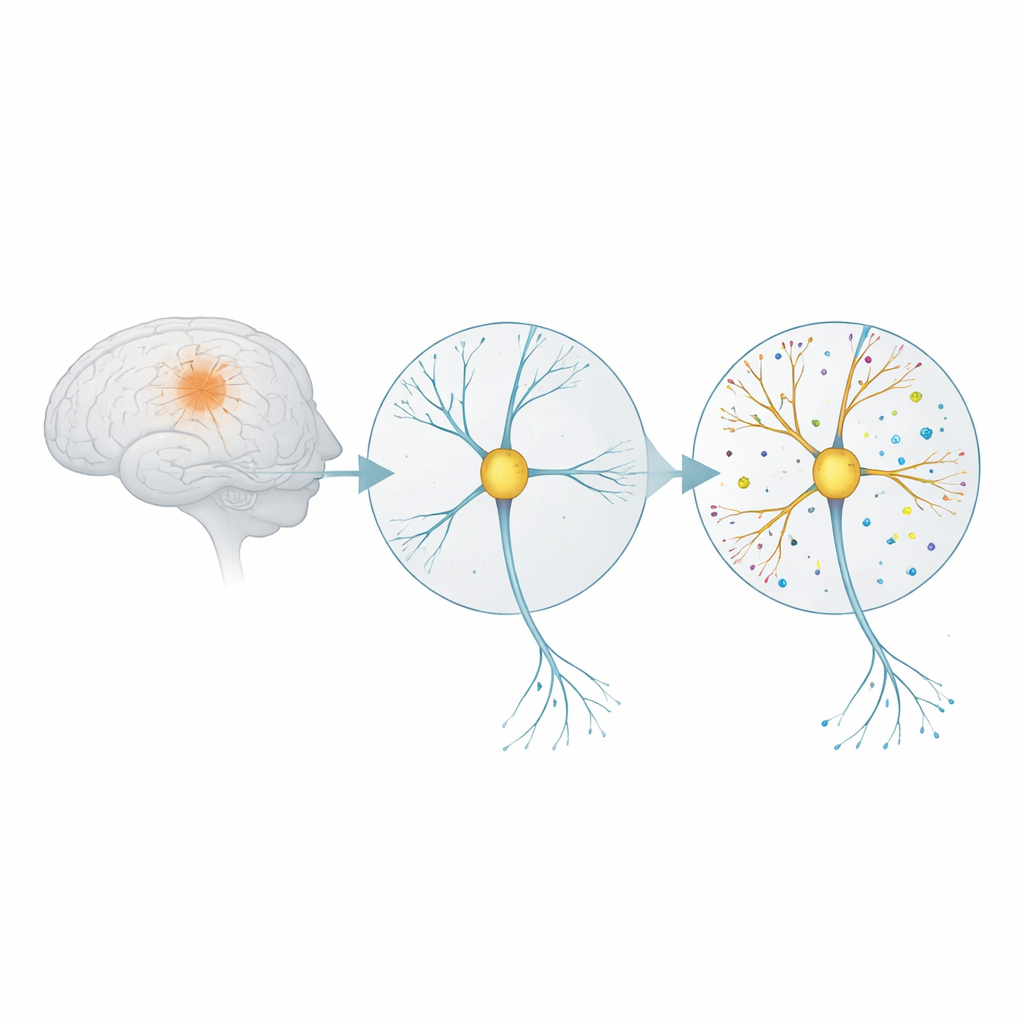
Hoe hersenverbindingen reageren op een toxische prikkel
De ziekte van Alzheimer wordt sterk geassocieerd met kleine klompjes van een eiwitfragment dat amyloid‑bèta heet. In zijn oligomeervorm is dit fragment bijzonder schadelijk voor synapsen — de contactpunten waarop zenuwcellen met elkaar communiceren. De onderzoekers lieten rattenhersencellen in een schotel groeien tot ze rijpe netwerken vormden en stelden ze vervolgens gedurende vijf dagen bloot aan een lage dosis amyloid‑bèta-oligomeren. Ze onderzochten ook wat er gebeurde wanneer ze een verbinding genaamd eFT508 toevoegden, die een signaalenzym (MNK) blokkeert dat betrokken is bij het opstarten van eiwitproductie in cellen. Deze opzet was bedoeld om de zeer vroege ziektestadia na te bootsen, voordat wijdverbreide celdood optreedt.
Verborgen details van nieuwe synapsen zichtbaar maken
Om te onderzoeken hoe verbindingen veranderden, gebruikte het team “expansion microscopy”, een techniek die vastgelegde cellen fysiek laat opzwellen in een zacht gel zodat microscopisch kleine structuren veel gedetailleerder zichtbaar worden. Ze markeerden zenuwvezels en beide zijden van de synaps met fluorescente labels en reconstrueerden ze in 3D. Blootstelling aan amyloid‑bèta veroorzaakte een duidelijke toename van het aantal synapsen langs de takken van zenuwcellen. Vooral waren er meer enkele boutons — eenvoudige één-op-één contacten — en zeldzame “multi-geïnnerveerde spines”, waarbij meer dan één inkomende vezel samenkomt op één ontvangend punt. Deze patronen lijken op de synaptische toename die is gerapporteerd bij mensen met milde cognitieve stoornis. In aanwezigheid van eFT508 zakte het aantal synapsen weer richting het normale, wat suggereert dat het middel deze vroege overgroei kan tegengaan.
Nieuwe eiwitten veranderen, zelfs als de totale productie dat niet doet
Synapsen herstructureren zich voortdurend door eiwitten te maken en af te breken. Het team onderzocht vervolgens welke eiwitten nieuw werden aangemaakt tijdens en na blootstelling aan amyloid‑bèta. Ze voedden de neuronen met een onschadelijk kunstmatig aminozuur dat wordt ingebouwd in verse eiwitten, en gebruikten daarna chemische “click”-reacties en massaspectrometrie om deze moleculen te isoleren en te identificeren. Verrassend genoeg veranderde de totale hoeveelheid nieuwgemaakt eiwit niet na meerdere dagen lage dosis amyloid‑bèta, met of zonder eFT508. Maar bij nader onderzoek welke specifieke eiwitten werden geproduceerd, bleek het beeld heel anders: er werden meer dan duizend nieuwgemaakte eiwitten gedetecteerd, en tientallen daarvan verschilden in op- of neerwaartse richting als reactie op amyloid‑bèta. Veel betroffen eiwitten die betrokken zijn bij synaptische communicatie, het cellulaire skelet, energieproducerende mitochondriën, afvalverwerkende systemen en eiwitkwaliteitscontrole.
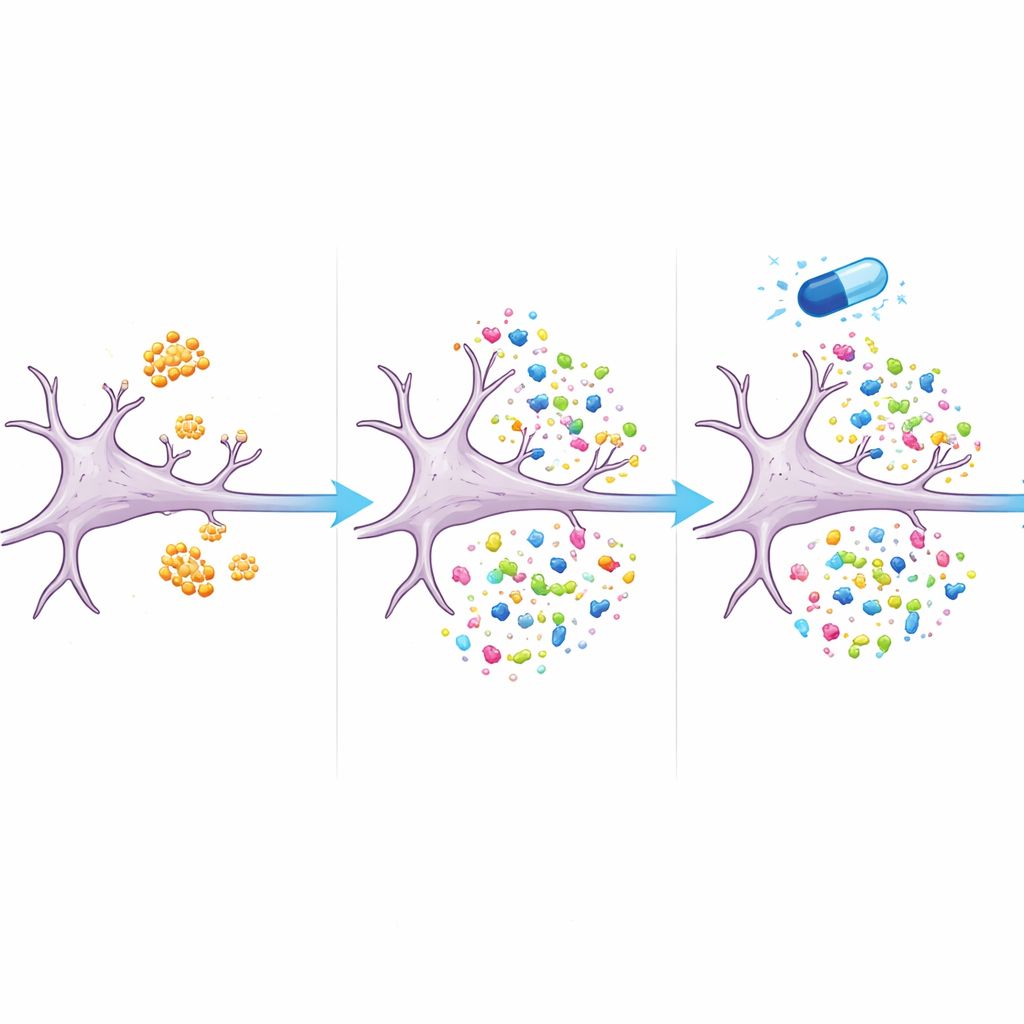
Een middel dat het eiwitbalans stuurt
Cruciaal is dat veel van de verstoorde eiwitten weer naar normale niveaus bewogen toen cellen werden behandeld met eFT508 samen met amyloid‑bèta. Meer dan twee derde van de eiwitten die door amyloid‑bèta alleen werden veranderd, verschilde niet langer significant van onbehandelde cellen wanneer het middel aanwezig was. Daartoe behoorden eiwitten die gelinkt zijn aan synapsstructuur en -functie, evenals componenten van het recyclingsysteem en de energiehuishouding van de cel. De resultaten suggereren dat eFT508 niet simpelweg de eiwitsynthese uitschakelt; het lijkt eerder te hervormen welke eiwitten worden gemaakt, waardoor het systeem wordt afgeschopt van een Alzheimer‑achtig patroon en richting een gezondere balans wordt gestuurd.
Wat dit kan betekenen voor toekomstige behandeling
Dit werk schetst een beeld van vroege Alzheimer‑gerelateerde schade als een fase van over‑verbinding en subtiele eiwitverstoring in plaats van directe verlies. Lage niveaus van amyloid‑bèta stimuleren de vorming van extra, soms ongewone synapsen en vertekenen selectief het palet aan eiwitten dat zenuwcellen maken. In dit in-vitro model kan eFT508 zowel het aantal synapsen normaliseren als veel van de eiwitveranderingen corrigeren, wat erop wijst dat het nauwkeurig afstemmen van eiwitsynthese mogelijk de voortgang van milde cognitieve stoornis naar volledige dementie kan vertragen of voorkomen. Hoewel er nog veel getest moet worden in levende dieren en mensen, benadrukt de studie een nieuwe manier van denken over — en mogelijk interveniëren in — de vroegste stadia van de ziekte van Alzheimer.
Bronvermelding: Wu, K., Lee, S., Martinez-Serra, R. et al. Low concentrations of amyloid-beta oligomers induce synaptogenesis characteristic for mild cognitive impairment and alter the de novo proteome. Transl Psychiatry 16, 132 (2026). https://doi.org/10.1038/s41398-026-03905-x
Trefwoorden: Ziekte van Alzheimer, synaptische veranderingen, amyloid-bèta-oligomeren, eiwitsynthese, vroege neurodegeneratie