Clear Sky Science · nl
Prenatale en postnatale effecten van moederlijke immuunactivatie op synaptische en neuro-ontwikkelingspaden via epigenetische mechanismen
Hoe het immuunsysteem van een moeder het brein van een kind vormt
Infecties tijdens de zwangerschap worden al lang in verband gebracht met een verhoogd risico op aandoeningen zoals schizofrenie, autisme en ADHD bij kinderen, maar de biologische “brug” tussen een zieke moeder en een kwetsbaar volwassen brein was onduidelijk. Deze studie gebruikt muizen om te laten zien hoe de immuunreactie van een moeder op griep tijdens de zwangerschap blijvende chemische sporen in het zich ontwikkelende brein kan achterlaten, waardoor de communicatie tussen hersencellen verandert en het risico op latere psychische en neurologische problemen kan toenemen.
Ziekte tijdens de zwangerschap en levenslang breinrisico
Epidemiologische studies bij mensen hebben aangetoond dat wanneer zwangere vrouwen infecties doormaken, hun kinderen later een grotere kans hebben op een reeks psychiatrische en neuro-ontwikkelingsstoornissen. De auteurs richten zich op moederlijke immuunactivatie, de cascade van immuunsignalen die vrijkomt wanneer het lichaam een infectie bestrijdt. Deze signalen kunnen de placenta passeren of beïnvloeden en in wisselwerking treden met het zich ontwikkelende brein op een moment waarop circuits worden aangelegd. De frontale cortex — cruciaal voor plannen, beslissen en emotionele beheersing — ontwikkelt zich over een lange periode en is bijzonder gevoelig voor vroege verstoringen.
Ontleden van effecten voor en na de geboorte
Om te scheiden wat gebeurt in de baarmoeder van wat gebeurt na de geboorte, infecteerden de onderzoekers zwangere muizen met een milde, niet-dodelijke influenzavirus tijdens een vroeg stadium van de dracht dat overeenkomt met het einde van het eerste trimester bij mensen. Sommige pups bleven bij hun biologische moeder, terwijl anderen binnen 24 uur na de geboorte bij pleegmoeders werden ondergebracht. Dit creëerde vier groepen: nakomelingen zonder blootstelling voor of na de geboorte, nakomelingen blootgesteld alleen voor de geboorte, alleen na de geboorte, of tijdens beide perioden. Toen de nakomelingen de volwassenheid bereikten, onderzocht het team neuronen uit de frontale cortex en keek zowel naar genactiviteit als naar “epigenetische” markeringen — chemische labels op eiwitten die DNA verpakken en helpen bepalen welke genen aan of uit staan. 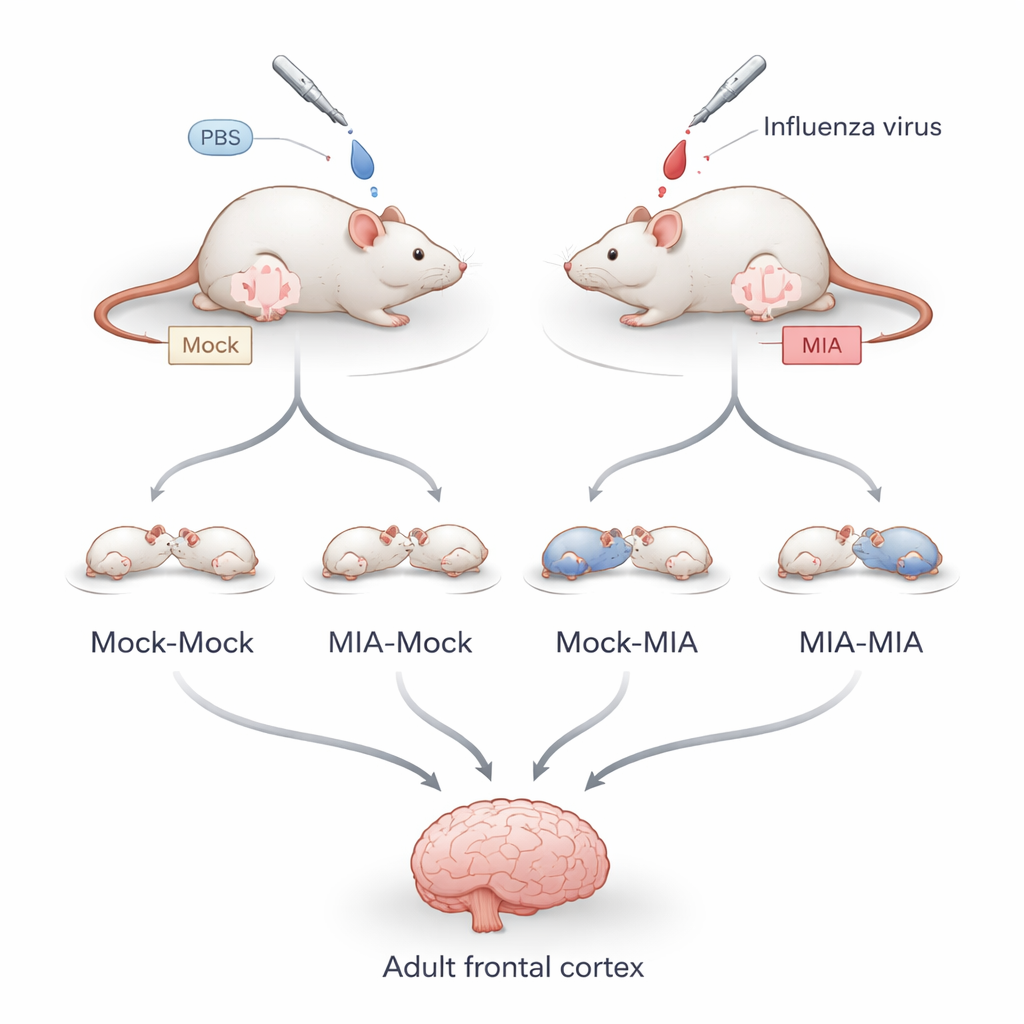
Blijvende chemische sporen op hersen-DNA
De studie concentreerde zich op twee histonmarkeringen, H3K27ac en H3K4me3, die actieve schakelaars en startpunten voor genen aanduiden. Met gevoelige sequenceringstechnieken brachten de auteurs tienduizenden van deze regelgevende regio’s in kaart en maten welke genen in elke groep meer of minder actief waren. Ze vonden dat moederlijke immuunactivatie vóór de geboorte wijdverspreide en blijvende veranderingen in enhancer-regio’s veroorzaakte — DNA-streken die fungeren als regelknoppen voor genexpressie. Deze veranderingen waren vooral verrijkt in genen die betrokken zijn bij de bouw van de voorhersenen, het sturen van groeiende zenuwvezels en het opzetten van vroege contactpunten tussen neuronen. Veel van dezelfde genen toonden ook veranderde activiteit na de geboorte wanneer pups werden grootgebracht door immuun-geactiveerde moeders, wat wijst op een aanhoudende regulerende traject door de ontwikkeling heen in plaats van een kortstondige schok.
Van epigenetische verschuivingen naar synaps- en circuitveranderingen
Zowel prenatale als postnatale blootstelling beïnvloedde moleculaire paden die bepalen hoe neuronen met elkaar signaleren. Genen gekoppeld aan glutamaat (de belangrijkste exciterende neurotransmitter), GABA (de belangrijkste remmende neurotransmitter) en dopamine (belangrijk voor motivatie en beloning) toonden gecoördineerde veranderingen in hun regelgevende elementen en expressieniveaus. Deze systemen worden herhaaldelijk in verband gebracht met schizofrenie, depressie, autisme en verslaving. De auteurs vonden ook dat genen betrokken bij synapsorganisatie, axongroei en verfijning van hersencircuits werden beïnvloed, vooral door postnatale blootstelling, wat suggereert dat moederlijk gedrag en aanhoudende immuungerelateerde veranderingen na de geboorte helpen bepalen hoe neurale netwerken worden bekabeld en bijgesteld. Netwerkanalyses benadrukten een kernset van transcriptiefactoren — meesterregelaars van genactiviteit — die in beide tijdsvensters verstoord waren.
Verbanden met menselijk psychiatrisch risico
Om te testen hoe relevant deze muisveranderingen zijn voor menselijke ziekten, zetten de onderzoekers de muizen-enhancer- en promotorlocaties om naar hun dichtstbijzijnde menselijke tegenhangers en vergeleken die met grootschalige genetische onderzoeken naar psychiatrische stoornissen. Regio’s die door moederlijke immuunactivatie waren veranderd, waren sterk verrijkt in menselijke risicoloci voor schizofrenie, bipolaire stoornis, depressie, neuroticisme en ADHD, maar niet voor de meeste niet-psychiatrische aandoeningen. Dit patroon suggereert dat dezelfde typen regelgevend DNA die erfelijk genetisch risico voor psychische ziekten dragen ook gevoelig zijn voor immuunuitdagingen tijdens de zwangerschap en het vroege leven, waardoor ze een convergentiepunt vormen voor genen en omgeving. 
Wat dit betekent voor de menselijke gezondheid
Voor de niet-specialist is de kernboodschap dat de immuunreactie van een moeder — niet alleen de infectie zelf — duurzame “aantekeningen in de marge” van het instructieboek van het zich ontwikkelende brein kan achterlaten. Deze epigenetische aantekeningen, geschreven voor en kort na de geboorte, kunnen subtiel veranderen hoe hersencellen groeien en met elkaar communiceren in circuits die denken, stemming en gedrag reguleren. Hoewel de meeste kinderen van zieke moeders geen psychiatrische stoornissen zullen ontwikkelen, helpt dit werk verklaren waarom sommige kinderen kwetsbaarder kunnen zijn, en benadrukt het het belang van het voorkomen en beheersen van infecties en ontsteking tijdens de zwangerschap en het vroege leven als onderdeel van langetermijnbreingezondheid.
Bronvermelding: Zhu, B., Li, G., Saunders, J.M. et al. Prenatal and postnatal effects of gestational immune activation on synaptic and neurodevelopmental pathways via epigenetic mechanisms. Transl Psychiatry 16, 82 (2026). https://doi.org/10.1038/s41398-026-03884-z
Trefwoorden: moederlijke immuunactivatie, epigenetica, neuro-ontwikkeling, synaptische signalering, psychiatrisch risico