Clear Sky Science · nl
METTL3-gemedieerde m6A-modificatie reguleert CDKN1A om door chronisch slaaptekort veroorzaakte cognitieve stoornissen en neuronale apoptose bij ratten te verminderen
Waarom slapeloze nachten je geheugen kunnen schaden
Veel mensen nemen chronisch slaaptekort voor lief als een normaal onderdeel van het moderne leven, maar de wetenschap laat zien dat slaapverlies stilletjes de hersengebieden kan beschadigen die leren en geheugen ondersteunen. Deze studie bij ratten kijkt op het niveau van individuele moleculen in hippocampale neuronen en identificeert een specifieke chemische schakelaar — METTL3 — die hersencellen lijkt te beschermen tegen de schadelijke effecten van chronisch slaaptekort. Inzicht in deze schakelaar zou uiteindelijk kunnen wijzen op nieuwe manieren om het geheugen te beschermen bij mensen die slaapverlies moeilijk kunnen vermijden, zoals ploegendiensten, mantelzorgers en patiënten met slaapproblemen.
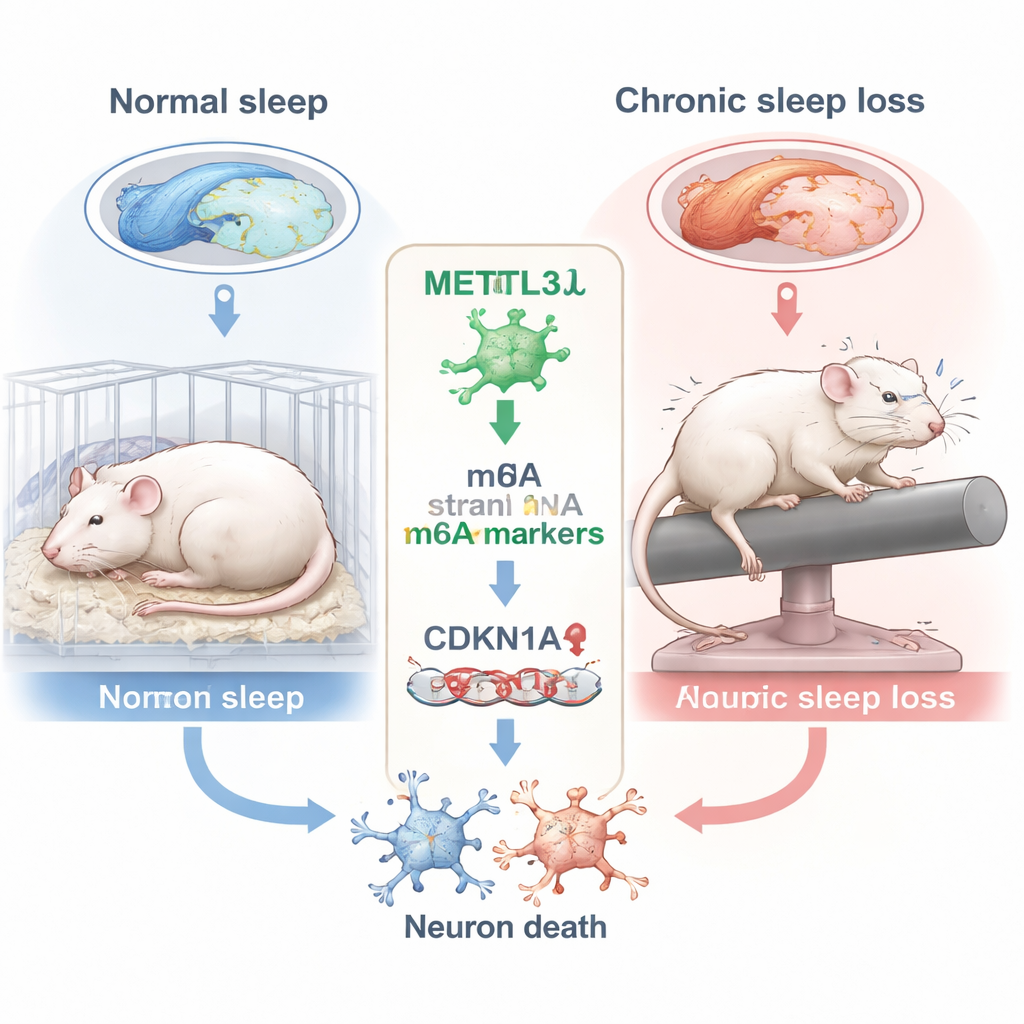
Hoe langdurig slaaptekort het geheugen-centrum beschadigt
De onderzoekers richtten zich op de hippocampus, een zeepaardvormig hersengebied dat essentieel is voor het vormen van nieuwe herinneringen. Binnen de hippocampus zoomden ze in op een subregio genaamd CA3, die helpt bij het coderen en ophalen van ruimtelijke informatie — vaardigheden die worden getest met taken zoals het vinden van een verborgen platform in water. Ratten werden gedurende zes weken elke dag 10 uur wakker gehouden met een zachte roterende staaf die ze herhaaldelijk uit de slaap duwde. Bij de bekende Morris Water Maze namen de slaapgebrekratten minder directe routes, staken ze de eerdere platformlocatie minder vaak over en brachten ze minder tijd door in het doelkwadrant — allemaal tekenen van een verstoord ruimtelijk geheugen vergeleken met goed uitgeruste dieren.
Een chemische markering op RNA die verdwijnt
Om te begrijpen wat er in CA3-neuronen gebeurde, analyseerde het team een chemische markering op RNA genaamd m6A, een van de meest voorkomende interne merktekens op boodschapper-RNA. Deze merkers helpen bepalen hoe lang RNA-moleculen blijven bestaan en hoe efficiënt ze worden gebruikt om eiwitten te maken. Een belangrijke enzym dat m6A-markeringen aanbrengt is METTL3. Met behulp van grootschalige m6A-sequencing en genexpressieanalyse vonden de wetenschappers dat chronisch slaaptekort METTL3 in de CA3-regio significant verminderde. Deze daling werd bevestigd op zowel RNA- als proteïneniveau. Het patroon van aangetaste genen suggereerde verstoringen in de controle van de celcyclus en stressreacties, wat erop wijst dat slaapverlies neuronen mogelijk naar ongezonde toestanden duwt.
Van moleculaire verandering naar celdood
Om te zien hoe lagere METTL3 neuronen direct zou kunnen beïnvloeden, gebruikten de onderzoekers muishippocampale cellen gekweekt in schalen. Toen ze kleine interfererende RNA's gebruikten om METTL3 te laten zwijgen, werden de cellen veel kwetsbaarder voor schadelijke behandeling met rapamycine, een geneesmiddel dat neuronen belast. Deze METTL3-uitgeputte cellen vertoonden hogere niveaus van klassieke "zelfmoord"-eiwitten zoals Bax en gekloofd caspase-3, en meer cellen werden door flowcytometrie als apoptotisch gemarkeerd. Diepere RNA-analyses wezen op één gen, CDKN1A (dat het p21-eiwit maakt), als een sleutelspeler: wanneer METTL3 werd gereduceerd, steeg CDKN1A sterk.
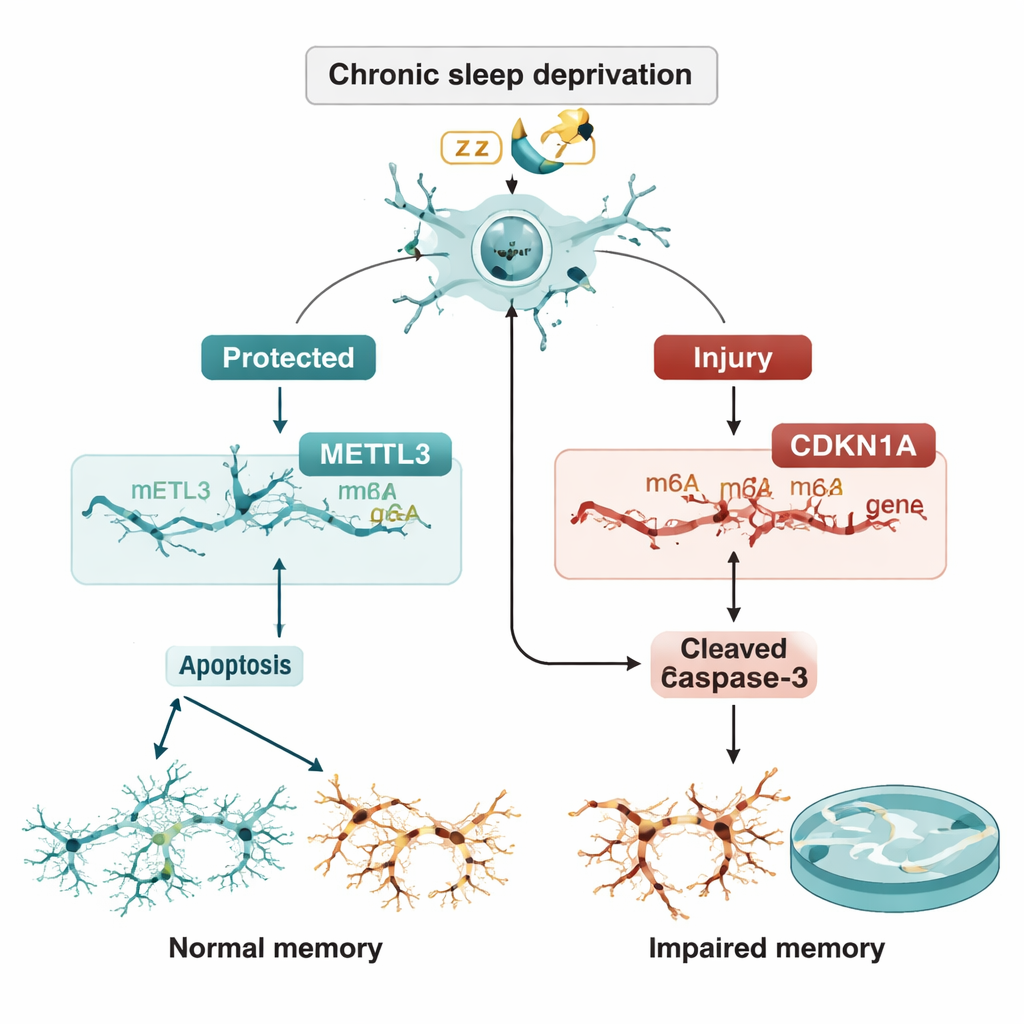
Een kwetsbaar evenwicht tussen bescherming en zelfvernietiging
Het team vroeg zich vervolgens af of METTL3 CDKN1A reguleert via m6A-markering. Ze toonden aan dat het verlagen van METTL3 de m6A-merkers op CDKN1A-RNA verminderde en dat dat RNA stabieler werd, zodat het zich ophoopte in plaats van afgebroken te worden. Hogere CDKN1A dreef op zijn beurt neuronen richting apoptose. Cruciaal was dat, wanneer CDKN1A zelf werd gereduceerd, de extra celdood veroorzaakt door verlies van METTL3 grotendeels werd teruggedraaid. Bij levende ratten verminderde het direct in CA3 toedienen van extra METTL3 met een viraal vector de CDKN1A-niveaus, verlaagde de hoeveelheid apoptose-eiwitten, behield de neuronale structuur in weefselkleuringen en verbeterde de prestaties in het watermaze ondanks aanhoudend slaapverlies.
Wat dit betekent voor mensen die niet genoeg slapen
Kort gezegd: chronisch slaaptekort lijkt een beschermend enzym, METTL3, te verzwakken in een cruciaal geheugen-circuit van de hersenen. Als METTL3 daalt, kan het bepaalde RNA's niet meer goed markeren, met name het RNA dat CDKN1A codeert. Dat RNA hoopt zich vervolgens op, waardoor neuronen richting geprogrammeerde celdood worden geduwd en geheugenproblemen ontstaan. Door METTL3 te herstellen, konden de onderzoekers CDKN1A weer naar beneden bijstellen, neuronverlies verminderen en het geheugen van slaapgebrekratten herstellen. Hoewel dit werk nog in de dierfase zit, identificeert het de METTL3–CDKN1A-route als een veelbelovende doelwit voor toekomstige medicijnen die de hersenen zouden kunnen beschermen tegen de cognitieve gevolgen van chronisch slaapverlies.
Bronvermelding: Xing, F., Shi, XS., Gu, HW. et al. METTL3-mediated m6A modification regulates CDKN1A to attenuate chronic sleep deprivation-induced cognitive impairment and neuronal apoptosis in rats. Transl Psychiatry 16, 96 (2026). https://doi.org/10.1038/s41398-026-03855-4
Trefwoorden: chronisch slaaptekort, hippocampus, RNA-methylatie, neuronale apoptose, geheugenstoornis