Clear Sky Science · nl
Verschillende en locatie-specifieke rollen van PlexinA2, PlexinA4 en NCAM in zich ontwikkelende hippocampale mossyvezels
Hoe zenuwpaden geheugenkringen vormgeven
De hippocampus, een hersengebied dat cruciaal is voor het vormen en ophalen van herinneringen, wordt verbonden door fijne zenuwvezels die zich tijdens de vroege levensfase met grote precisie moeten oriënteren. Deze studie stelt een ogenschijnlijk eenvoudige vraag: hoe weten die groeiende vezels precies waar ze heen moeten — en wat gebeurt er als hun geleidingssysteem ontspoort, mogelijk bijdragend aan aandoeningen zoals schizofrenie, autisme of epilepsie?
Twee snelwegen naar het geheugencentrum
Binnen de hippocampus sturen zenuwcellen in een gebied dat de dentate gyrus heet lange vezels, bekend als mossyvezels, richting een ander gebied genaamd CA3. Bij het binnentreden van CA3 splitsen deze vezels zich normaal gesproken in twee duidelijke “snelwegen”: één die boven een laag met CA3-cellichamen loopt en één die eronder loopt. Elke snelweg maakt verbinding met verschillende delen van CA3-cellen en helpt de balans van activiteit in dit geheugen-circuit vast te leggen. Als deze paden niet goed scheiden, kunnen vezels op de verkeerde plek terechtkomen en zo de informatiestroom door de hippocampus verstoren.
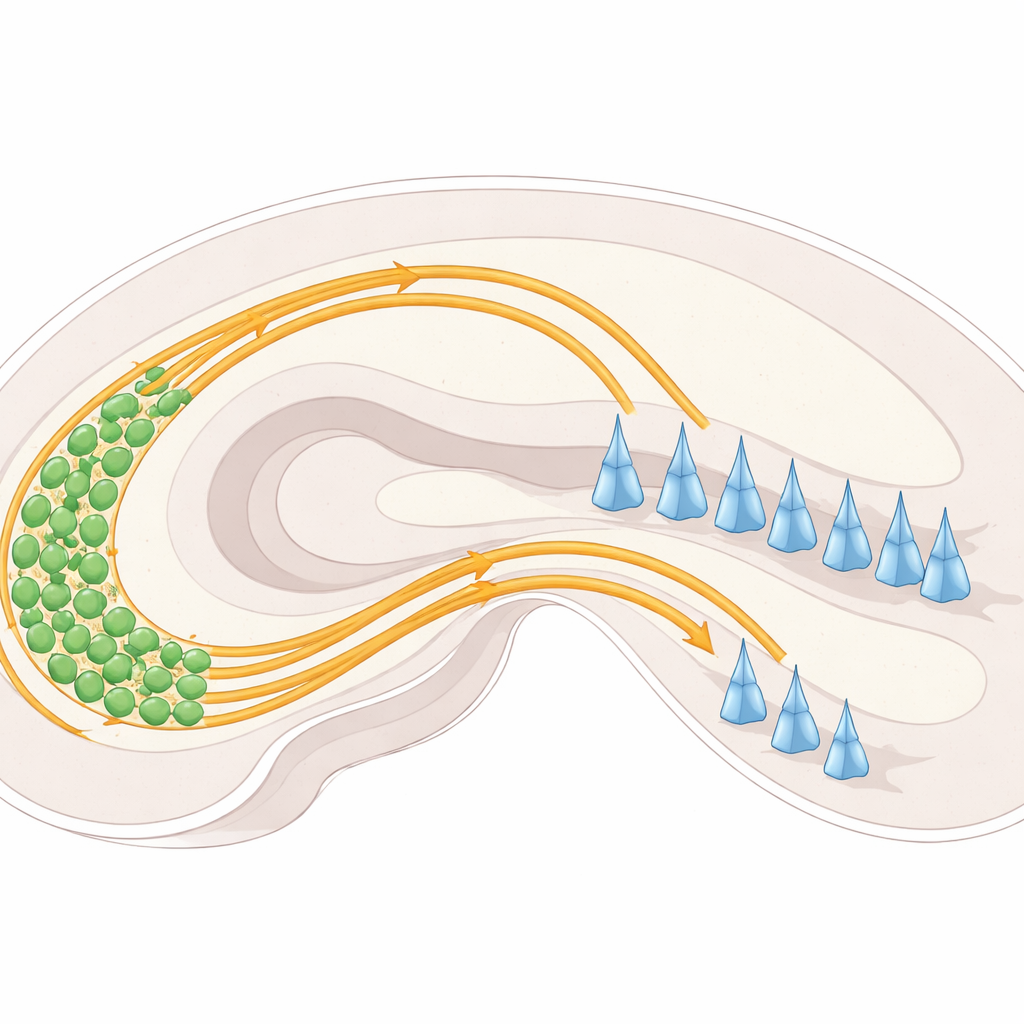
Geleidingssignalen: stuwende, trekkende en cel-tot-cel grijpkrachten
De onderzoekers concentreerden zich op een stel moleculaire wegwijzers en oppervlakte-‘handgrepen’ op zenuwcellen die mossyvezels sturen. Een familie eiwitten genaamd plexinen (PlexinA2 en PlexinA4) bevindt zich op het celoppervlak van neuronen en reageert op partnermoleculen die semaphorines heten, met name Sema6A. Deze interacties kunnen fungeren als “niet betreden”-signalen die vezels wegduwen van bepaalde regio’s, of ze kunnen fijnafstellen hoe sterk naburige vezels aan elkaar blijven plakken. Een ander oppervlakte-eiwit, NCAM, gedraagt zich meer als klittenband, bevordert adhesie en helpt vezelbundels samenhangend te houden. Door te onderzoeken waar deze eiwitten tot expressie komen en wat er gebeurt als ze bij muizen worden verwijderd of aangepast, brachten de onderzoekers in kaart hoe ze in levende hersenen samenwerken in plaats van in geïsoleerde cellen.
Ontleden van rollen met ontworpen muizen
Om elk onderdeel apart te kunnen bestuderen maakten de wetenschappers en combineerden ze 27 verschillende muizenlijnen. Sommige misten Sema6A volledig, andere misten PlexinA2 of PlexinA4, en weer andere droegen subtiele puntmutaties die slechts een specifiek “enzymcore” binnen de plexinen uitschakelden terwijl de rest van het molecuul intact bleef. Ze verwijderden ook selectief Sema6A of NCAM alleen uit bepaalde celtypen, zoals dentate granulecellen, om te testen waar het signaal echt van belang was. In muizen die Sema6A misten in deze granulecellen splitsten mossyvezels niet netjes in bovenste en onderste bundels en groeide de onderste bundel te ver door, voorbij het normale eindpunt. Vergelijkbare maar niet identieke foutieve bedrading ontstond in muizen zonder PlexinA2 of PlexinA4, wat blootlegde dat deze eiwitten op verschillende controlepunten langs hetzelfde pad werkzaam zijn.
Inzoomen op mechanismen en partnerschappen
Toen de auteurs de katalytische kern van PlexinA4 uitschakelden, traden veel — maar niet alle — van dezelfde defecten op als bij volledige PlexinA4-knockouts. Dit toonde aan dat PlexinA4 vaak op deze kern vertrouwt om het interne skelet van groeiende zenuwvezels te herschapen, zodat ze correct bundelen en op de juiste laag stoppen. PlexinA2 bleek anders te zijn: sommige van zijn rollen hingen af van die katalytische kern, andere niet, wat duidt op extra, enzymonafhankelijke signaalroutes. Het team gebruikte vervolgens een nabijheidslabeling-techniek om naburige eiwitten rond PlexinA2 op jonge hippocampale neuronen te identificeren. Meerdere celadhesiemoleculen kwamen naar voren, waarbij NCAM opviel. Genetisch gezien gaf het gelijktijdig verminderen van zowel PlexinA2 als NCAM sterkere mossyvezel-misrouting dan het verminderen van een van beide alleen, wat aantoont dat deze twee systemen samenwerken: NCAM levert adhesie, terwijl PlexinA2-geïnitieerde afstoting afstemt hoe vezels zich in bovenste en onderste banen scheiden en hoe ver de onderste baan uitstrekt.
Wanneer signalen in omgekeerde richting lopen
Interessant is dat Sema6A niet alleen fungeert als een extern ‘teken’ dat plexinen lezen; het kan ook als ontvanger op de mossyvezels zelf optreden. De onderzoekers bestudeerden muizen waarbij de interne staart van Sema6A was verwijderd terwijl het buitenste deel intact bleef. Bij deze dieren bleven sommige geleidingsdefecten bestaan — vooral de overgroei van de onderste bundel — wat aangeeft dat signalen die naar binnen lopen via de staart van Sema6A (“reverse signaling”) noodzakelijk zijn voor normale snoeiing en vormgeving van mossyvezels. Deze reverse-modus werkt waarschijnlijk samen met de meer bekende plexine-gebaseerde signalering op een stadium- en locatie-specifieke manier.
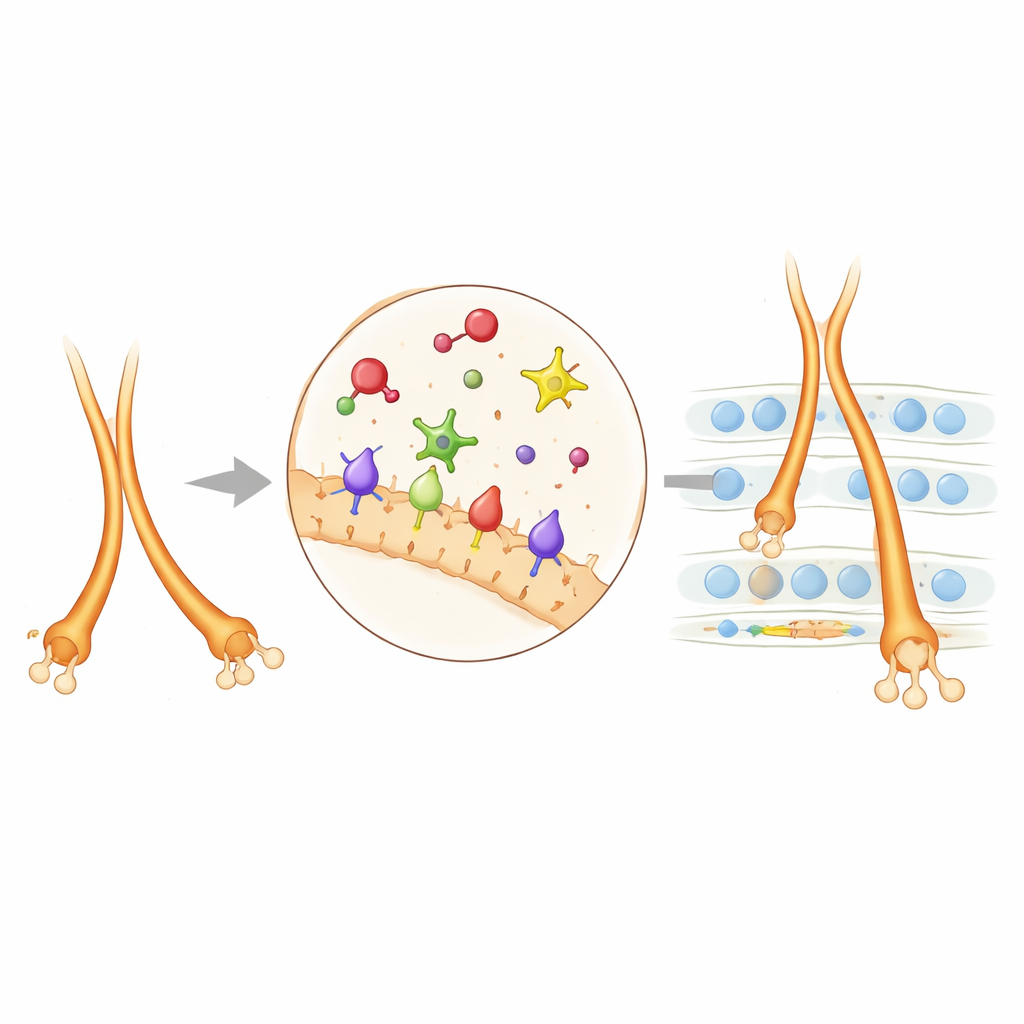
Waarom deze bedrading belangrijk is voor hersengezondheid
Mutaties in menselijke versies van PLXNA2, SEMA6A en NCAM1 zijn in verband gebracht met neuro-ontwikkelings- en psychiatrische aandoeningen, van verstandelijke beperking tot schizofrenie en autisme. Door precies te laten zien hoe deze moleculen samenwerken om de mossyvezel-paden bij muizen te vormen, biedt deze studie een concreet model voor hoe subtiele genetische veranderingen de vorming, scheiding en snoeiing van cruciale geheugenkringen kunnen verstoren. In gewone bewoordingen suggereert het werk dat de geleidingsgereedschapskist van de hersenen een zorgvuldig getimed mengsel van ‘duw’, ‘trek’ en ‘plak’-signalen gebruikt om het aansluitingsschema van de hippocampus te bouwen — en dat zelfs kleine verstoringen in deze gereedschapskist kunnen doorwerken in veranderingen in leren, geheugen en mentale gezondheid.
Bronvermelding: Zhao, XF., Kohen, R., Van Battum, E.Y. et al. Diverse and location-specific roles of PlexinA2, PlexinA4, and NCAM in developing hippocampal mossy fibers. Transl Psychiatry 16, 126 (2026). https://doi.org/10.1038/s41398-026-03846-5
Trefwoorden: hippocampale mossyvezels, axongeleiding, semaphorine-plexine signalering, NCAM en celadhesie, neuro-ontwikkelingsstoornissen