Clear Sky Science · nl
Dysfunctie van GABAerge interneuronen onderliggend aan veranderde neurale netwerkoscillaties geassocieerd met epileptiforme activiteit in PPT1-deficiënte muizen
Wanneer hersenritmes ontsporen
Aanvallen zijn niet zomaar plotselinge stormen van hersenactiviteit; ze ontstaan vaak uit subtiele veranderingen in hoe zenuwcellen met elkaar communiceren. Deze studie onderzoekt een zeldzame kinderlijke hersenaandoening, CLN1-ziekte, en stelt een eenvoudige vraag met verstrekkende implicaties: wat gebeurt er met de interne “ritmebewakers” van de hersenen wanneer een enkel enzym, PPT1, ontbreekt? Door deze veranderingen in muizen in de tijd te volgen, tonen de onderzoekers aan hoe kleine vroege fouten in remming kunnen uitgroeien tot aanvallen en wijdverspreide hersenschade.
De bewakers van hersenbalans
Onze hersenen vertrouwen op twee brede typen zenuwcellen. Exciterende cellen, zoals piramidale neuronen in de hippocampus, stuwen de activiteit voort. Inhiberende cellen, interneuronen genoemd, werken als remmen: zij houden die activiteit onder controle en vormen de elektrische ritmes van de hersenen. Onder deze groep zijn twee belangrijke typen parvalbumine-positieve (PV+) interneuronen en somatostatine-positieve (SST+) interneuronen. Zij helpen ritmische hersengolven te genereren en te coördineren, zoals theta- en gamma-oscillaties, die functies ondersteunen zoals leren en geheugen. Bij CLN1 verliezen kinderen het PPT1-enzym, dat normaal vetgroepen van eiwitten verwijdert. De auteurs gebruikten een muismodel met dezelfde mutatie als bij patiënten om te zien hoe dit verlies interneuronen en de ritmes die zij reguleren beïnvloedt.
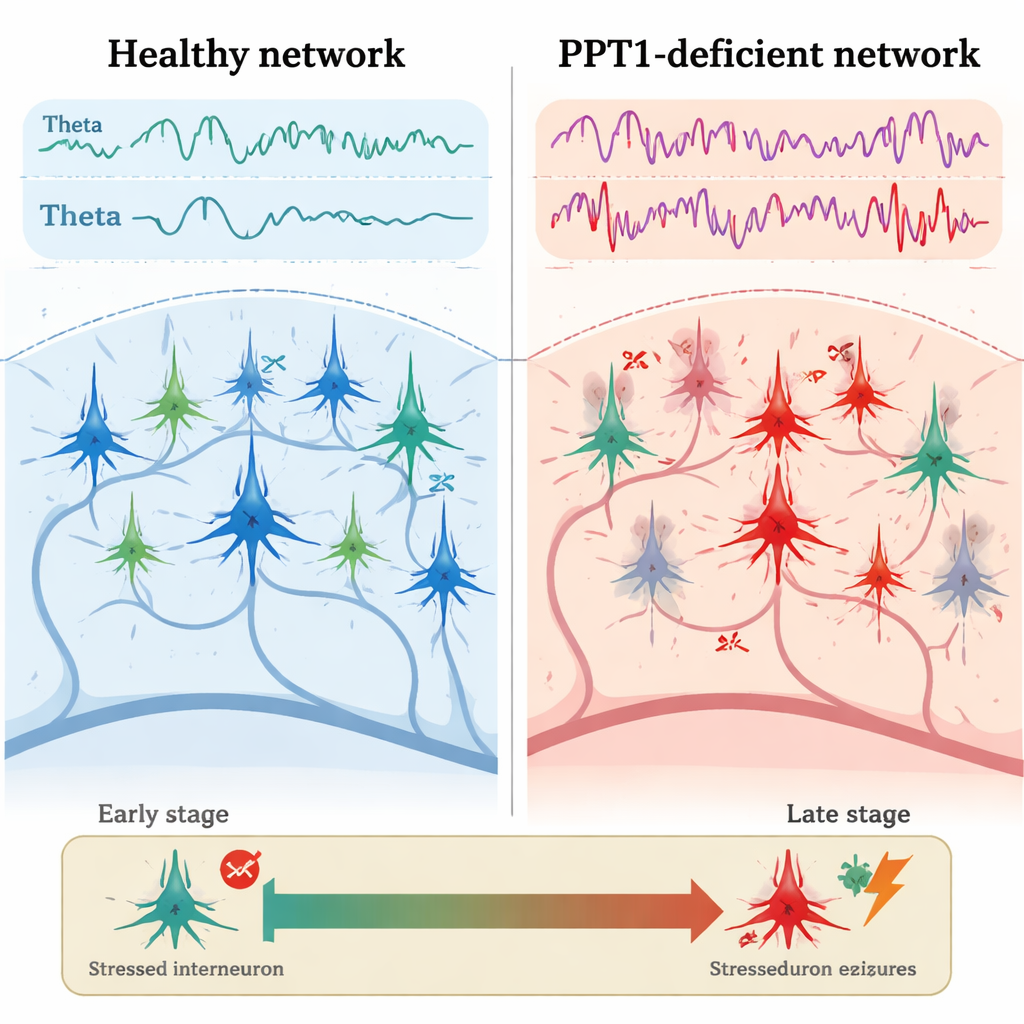
Vroege barsten in het remmingssysteem
Bij jonge volwassen mutantmuizen, ongeveer drie tot vier maanden oud, verscheen het eerste duidelijke probleem in PV+ interneuronen. Elektrische opnames uit de hippocampus toonden dat deze remmende cellen minder vaak vuren dan bij gezonde muizen, terwijl nabijgelegen piramidale neuronen sneller vuurden en met kortere tussenpozen tussen pieken. Microscopia liet zien dat veel PV+ interneuronen geactiveerd caspase-3 vertoonden, een belangrijke uitvoerder van geprogrammeerde celdood, hoewel hun totale aantallen nog niet waren afgenomen. Tegelijkertijd was het vermogen van theta- en gamma-golven verhoogd, en calciumimaging toonde sterkere activiteit in hippocampale neuronen terwijl de dieren zich voortbewogen. Cruciaal was dat de normale “kruisbestuiving” tussen theta- en gamma-ritmes — waarbij langzamere golven snellere ordenen — verzwakt was, wat wijst op een vroege ineenstorting van de fijne timing van netwerkactiviteit.
Van verstoorde ritmes naar aanvalspieken
Tegen de leeftijd van zes tot zeven maanden verslechterde het beeld. Veel PV+ interneuronen waren verdwenen, en inmiddels toonden ook SST+ interneuronen tekenen van caspase-3-activatie. Opnames uit de hippocampus onthulden spontane epileptiforme ontladingen — korte, abnormale activiteitspieken die met aanvallen geassocieerd zijn. Het team concentreerde zich op hoogfrequente “ripples”, snelle oscillaties die normaal geheugenopslag ondersteunen. Bij de mutante muizen werden fysiologische ripples (rond 140–200 hertz) minder frequent maar groter in amplitude, terwijl nog snellere “pathologische” ripples (200–500 hertz), die sterk aan epilepsie gerelateerd zijn, sterker en vaker voorkwamen. Samen suggereerden deze veranderingen een verschuiving van georganiseerde, geheugen-gerelateerde ritmes naar chaotische, aanvalsgeneigde patronen naarmate de remmende controle faalde.
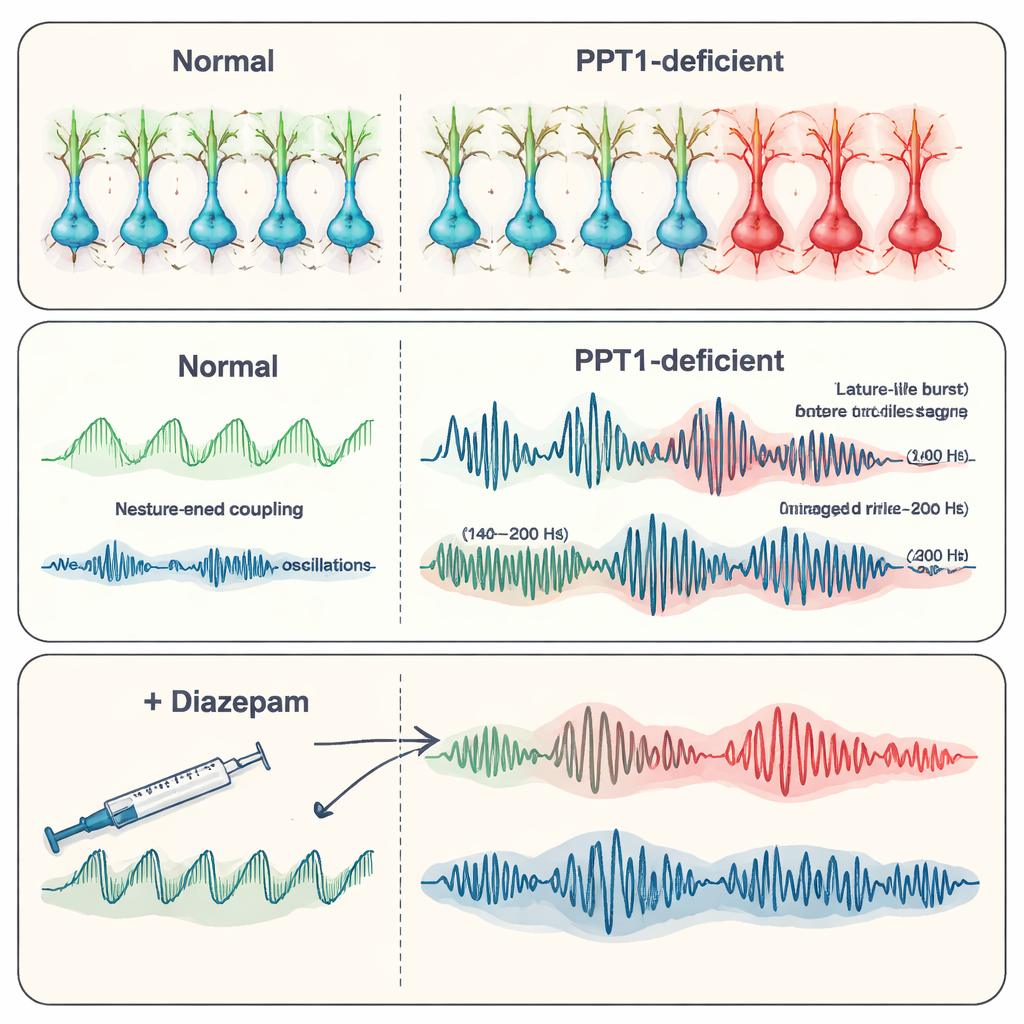
Neuronen slijten en diazepam grijpt in
Naarmate de ziekte vorderde, begon de hippocampus zelf te degenereren. Calciumsignalen in neuronen namen af, Golgi-kleuring toonde dunnere, minder vertakte dendritische bomen en er waren minder kleine uitsteeksels waar synapsen vormen. Tellingen van neuronen in sleutelregio’s van de hippocampus (CA1 en CA3) bevestigden wijdverspreid celverlies, en minder actieve units konden worden gedetecteerd in elektrische opnames. De onderzoekers testten vervolgens diazepam, een veelgebruikt middel tegen aanvallen dat de werking van de remmende stof GABA versterkt. Bij oudere mutante muizen verminderde diazepam de frequentie van epileptische ontladingen en herstelde gedeeltelijk meer normale oscillatiepatronen, inclusief ripple-gedrag, hoewel het het onderliggende receptorverlies niet repareerde. Dit suggereert dat het versterken van de resterende remmende signalen het netwerk nog steeds kan kalmeren, al is het tijdelijk.
Waarom deze bevindingen ertoe doen
Voor de niet-specialistische lezer is de kernboodschap dat CLN1-ziekte niet alleen een kwestie is van opgehoopt afval in hersencellen. Het verlies van PPT1 zet een kettingreactie in gang: eerst raken gespecialiseerde remmende interneuronen gestrest en beginnen ze te falen, waardoor overactieve piramidale neuronen losbarsten en de ritmes van de hersenen vervormen. Na verloop van tijd leidt deze disbalans tot aanvallen en uiteindelijk tot grootschalig verlies van hersencellen en verbindingen. De studie wijst op een venster van kans vroeg in de ziekte, waarin het beschermen of redden van PV+ interneuronen — mogelijk door caspase-activatie te blokkeren — latere aanvallen en degeneratie zou kunnen voorkomen. Hoewel diazepam CLN1 niet kan genezen, onderstreept het vermogen om abnormale ritmes te dempen in dit model het bredere idee dat het herstellen van remming een krachtige strategie kan zijn bij epilepsie en verwante hersenaandoeningen.
Bronvermelding: Tong, J., Liu, W., Wang, Q. et al. Dysfunction of GABAergic interneurons underlies altered neural network oscillations associated with epileptiform activity in PPT1-deficient mice. Transl Psychiatry 16, 106 (2026). https://doi.org/10.1038/s41398-026-03843-8
Trefwoorden: epilepsie, interneuronen, hippocampus, hersengolven, lysosomale opslagziekte