Clear Sky Science · nl
Vroege functionele veranderingen en plasma-GFAP in Zweedse families met autosomaal dominante Alzheimer-mutaties
Waarom dit onderzoek belangrijk is voor families
De ziekte van Alzheimer lijkt vaak plotseling te verschijnen, maar eigenlijk stapelen schadelijke veranderingen in de hersenen zich jarenlang stilletjes op. In zeldzame families die erfelijke ("autosomaal dominante") Alzheimer-mutaties dragen, kunnen wetenschappers inschatten wanneer symptomen waarschijnlijk zullen beginnen en deze vroege veranderingen volgen terwijl ze zich ontvouwen. Deze studie volgde Zweedse families met dergelijke mutaties om te begrijpen hoe het energiegebruik in de hersenen, cognitieve functies en een bloedmarker van hersensteuncellen (GFAP) veranderen ver voordat geheugenproblemen ontstaan — en hoe deze verschuivingen per gen verschillen.
De ziekteklok volgen in risicofamilies
Aangezien mensen met autosomaal dominante Alzheimer (ADAD) doorgaans symptomen op een redelijk voorspelbare leeftijd ontwikkelen, kunnen onderzoekers de "geschatte jaren tot symptoomaanvang" (EYO) berekenen — hoeveel jaren iemand verwijderd is van of voorbij hun verwachte eerste ziektenmerken. Het team bestudeerde 45 volwassenen uit Zweedse families met APP- of PSEN1-genmutaties, evenals familieleden zonder mutaties. Gedurende gemiddeld meer dan zeven jaar ondergingen deelnemers hersenscans die meten hoeveel suiker de hersenen verbruiken (FDG PET), gedetailleerde cognitieve en geheugentests en, voor een subset, bloedtesten voor GFAP, een eiwit dat vrijkomt wanneer hersensteuncellen genaamd astrocyten reactief worden. Dit ontwerp stelde de onderzoekers in staat verschillende biologische veranderingen langs een gedeelde ziektetijdlijn te plaatsen in plaats van alleen mensen op één moment te vergelijken.
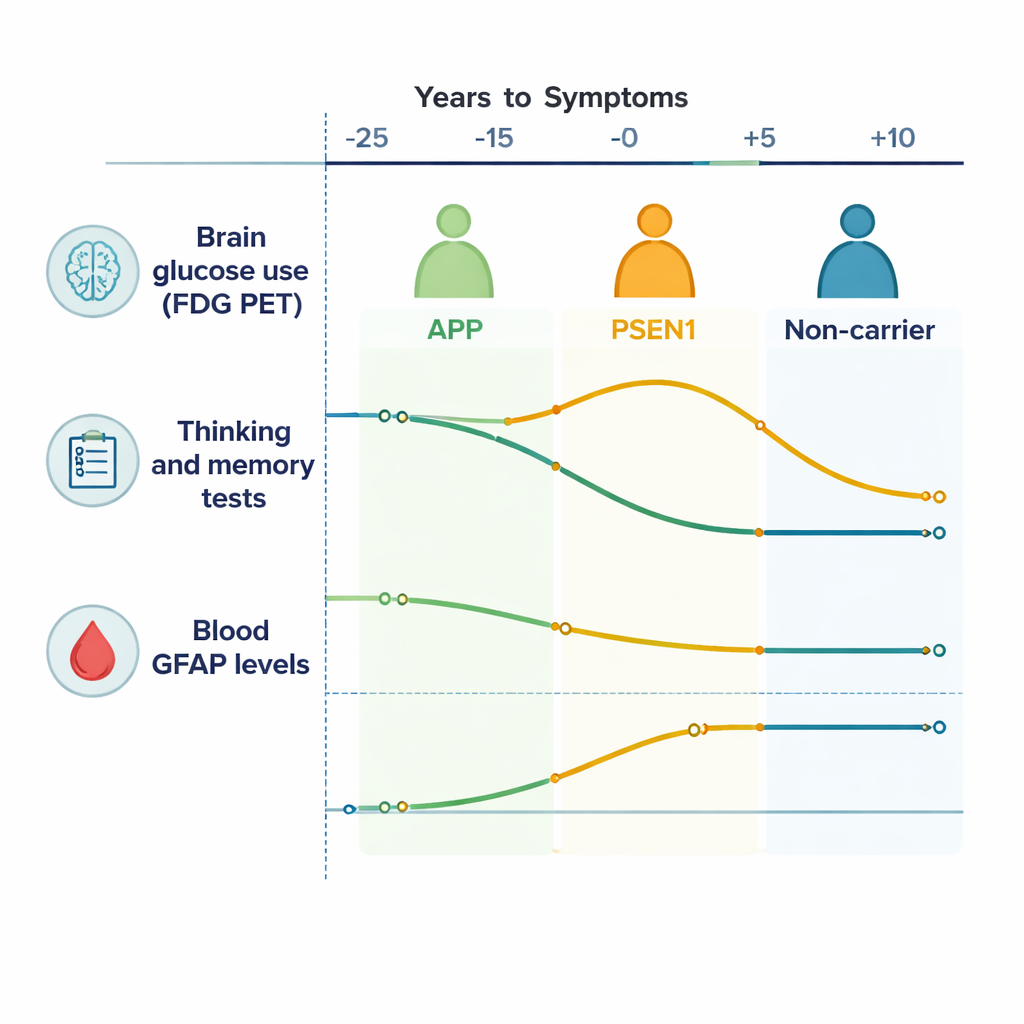
Hersenenergie en denken in kaart brengen in de tijd
Over de buitenlagen van de hersenen (de cortex) lieten mensen met Alzheimer-mutaties een geleidelijke daling van het FDG PET-signaal zien vergeleken met familieleden zonder mutaties, wat betekent dat hun hersenen in de loop van de tijd minder suiker gebruikten — een teken van achteruitgang van hersencellen. Subcorticale gebieden diep in de hersenen, met name de caudaat en thalamus, toonden ook dalende activiteit, vooral gedreven door degenen met APP-mutaties. Cognitieve en geheugentests verslechterden in meerdere domeinen, waaronder episodisch geheugen en mentale flexibiliteit, beginnend ongeveer 10–15 jaar vóór de verwachte symptomatische aanvang. Met andere woorden: zelfs terwijl mensen zich in het dagelijks leven normaal voelden en functioneerden, onthulden gevoelige tests en scans dat hun hersenen al harder en minder efficiënt aan het werk waren.
Verschillende patronen voor verschillende Alzheimer-genen
Een belangrijke conclusie was dat de twee hoofdgroepen mutaties — APP en PSEN1 — niet identieke trajecten volgden. Bij dragers van PSEN1 zagen de onderzoekers een vroege periode, ongeveer 20 tot 10 jaar vóór de verwachte symptomen, waarin delen van de hersenen juist een ongewoon hoog suikergebruik vertoonden ("hypermetabolisme"), samen met beter presteren op tests, voordat later een daling optrad. Dit weerspiegelt waarschijnlijk een tijdelijke compensatiefase, waarin de hersenen en hun steuncellen de activiteit opvoeren om om te gaan met toenemende schade. APP-dragers toonden daarentegen een meer rechtlijnige, geleidelijke daling van het hersenmetabolisme zonder deze vroege piek. Deze gen-specifieke patronen suggereren dat "ziekte van Alzheimer" geen enkel biologisch verhaal is, zelfs niet in erfelijke vormen, maar een familie van verwante processen die verschillend verlopen afhankelijk van de onderliggende mutatie.
Wat een bloedtest onthult over vroege hersenstress
GFAP, gemeten via een eenvoudige bloedafname, bood een venster op hoe astrocyten reageren op vroege Alzheimer-veranderingen. GFAP-niveaus hadden de neiging gestaag te stijgen naarmate mensen dichter bij hun verwachte symptomenleeftijd kwamen, zowel bij mutatiedragers als niet-dragers, maar de verbanden tussen GFAP, hersenmetabolisme en cognitieve prestaties waren gen-specifiek. Bij APP-dragers ging hoger GFAP gepaard met afnemend hersensuikergebruik in diepe hersengebieden en met verslechtering op de meeste cognitieve tests, wat suggereert dat astrocytactivatie nauw verbonden is met vroege schade en functieverlies. Bij PSEN1-dragers waren deze verbanden zwakker of afwezig, wat opnieuw wijst op verschillende biologische wegen naar hetzelfde klinische eindpunt van dementie.
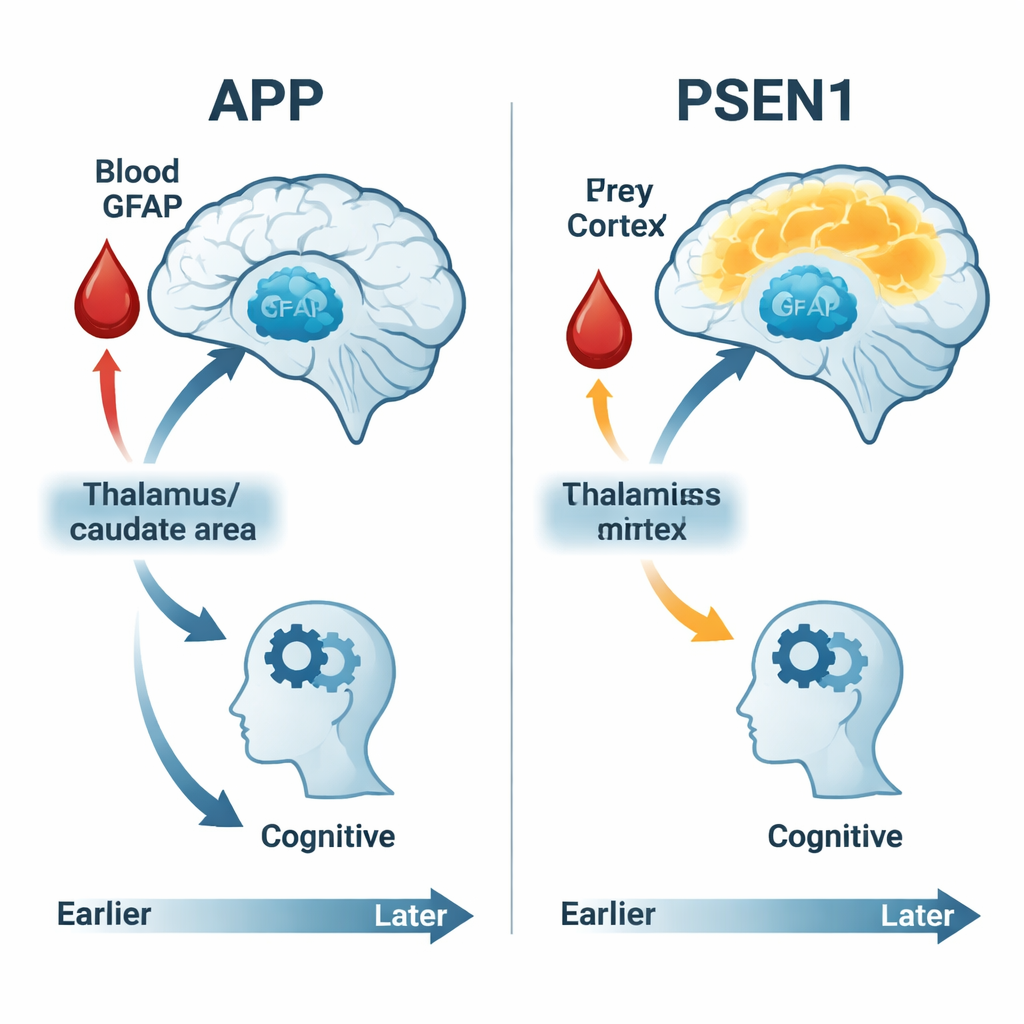
Wat dit betekent voor vroege opsporing en behandeling
Voor de algemene lezer is de hoofdboodschap dat in deze hoogrisicofamilies Alzheimer-gerelateerde veranderingen decennia vóór duidelijke geheugenverlies beginnen — en dat ze er niet voor iedereen hetzelfde uitzien. Hersenscans die suikergebruik meten, fijnmazige cognitieve tests en een enkele bloedmarker zoals GFAP kunnen samen onthullen wanneer de hersenen beginnen te worstelen en hoe snel die achteruitgang vordert. Belangrijk is dat mensen met verschillende genetische vormen van Alzheimer verschillende veranderingssequenties laten zien: sommige hebben een vroege overactieve fase, anderen tonen een gestage achteruitgang, en de bloedmarker voor astrocytstress hangt sterker samen met schade in sommige groepen dan in andere. Het herkennen van deze verschillende trajecten kan helpen toekomstige geneesmiddelen en studies beter af te stemmen op de juiste mensen op het juiste moment, en ondersteunt de belofte van bloedtests zoals GFAP om Alzheimer vroeger op te sporen — voordat symptomen mensen hun zelfstandigheid ontnemen.
Bronvermelding: Luckett, E.S., Zapater-Fajari, M., Almkvist, O. et al. Early functional changes and plasma GFAP in Swedish families with Autosomal Dominant Alzheimer’s disease mutations. Transl Psychiatry 16, 67 (2026). https://doi.org/10.1038/s41398-026-03829-6
Trefwoorden: autosomaal dominante ziekte van Alzheimer, GFAP bloedbiomarker, hersen-glucosemetabolisme, astrocyten en neurodegeneratie, vroegtijdige detectie van Alzheimer