Clear Sky Science · nl
Convergentie en divergentie van genen geïnformeerd door veelvoorkomende en zeldzame varianten van autismespectrumstoornissen in weefselspecifieke routes en genenetzwerken
Waarom het genetische raadsel van autisme ertoe doet
Families en clinici weten al lang dat autismespectrumstoornis (ASS) sterk varieert: sommige mensen hebben levenslange ondersteuning nodig, terwijl anderen zelfstandig leven maar toch sociale moeilijkheden ondervinden. Een groot deel van deze diversiteit wordt toegeschreven aan genetica, maar het risico is verspreid over duizenden DNA-veranderingen, die elk het brein en lichaam op subtiele wijze beïnvloeden. Deze studie stelt een eenvoudige maar belangrijke vraag: hoe werken zeldzame, krachtige mutaties en de vele veelvoorkomende, zwakkere DNA-varianten samen in verschillende weefsels om autisme vorm te geven — en wat betekent dat voor het begrijpen en behandelen van de aandoening?
Twee soorten genetische aanwijzingen
Onderzoekers maken onderscheid tussen zeldzame varianten, die een gen sterk kunnen verstoren maar relatief weinig mensen treffen, en veelvoorkomende varianten, die frequent in de bevolking voorkomen maar meestal kleine effecten hebben. Zeldzame varianten zijn makkelijker te koppelen aan autisme binnen individuele families, maar verklaren slechts een klein deel van het totale genetische risico. Veelvoorkomende varianten samen leveren veel meer van het erfelijke aandeel van autisme, maar elk apart is het effect klein en gemakkelijk over het hoofd te zien. De auteurs van dit artikel wilden beide signalen integreren en onderzochten of ze samenkomen in dezelfde biologische systemen of wijzen op verschillende lichaamsdelen en ziektemechanismen.
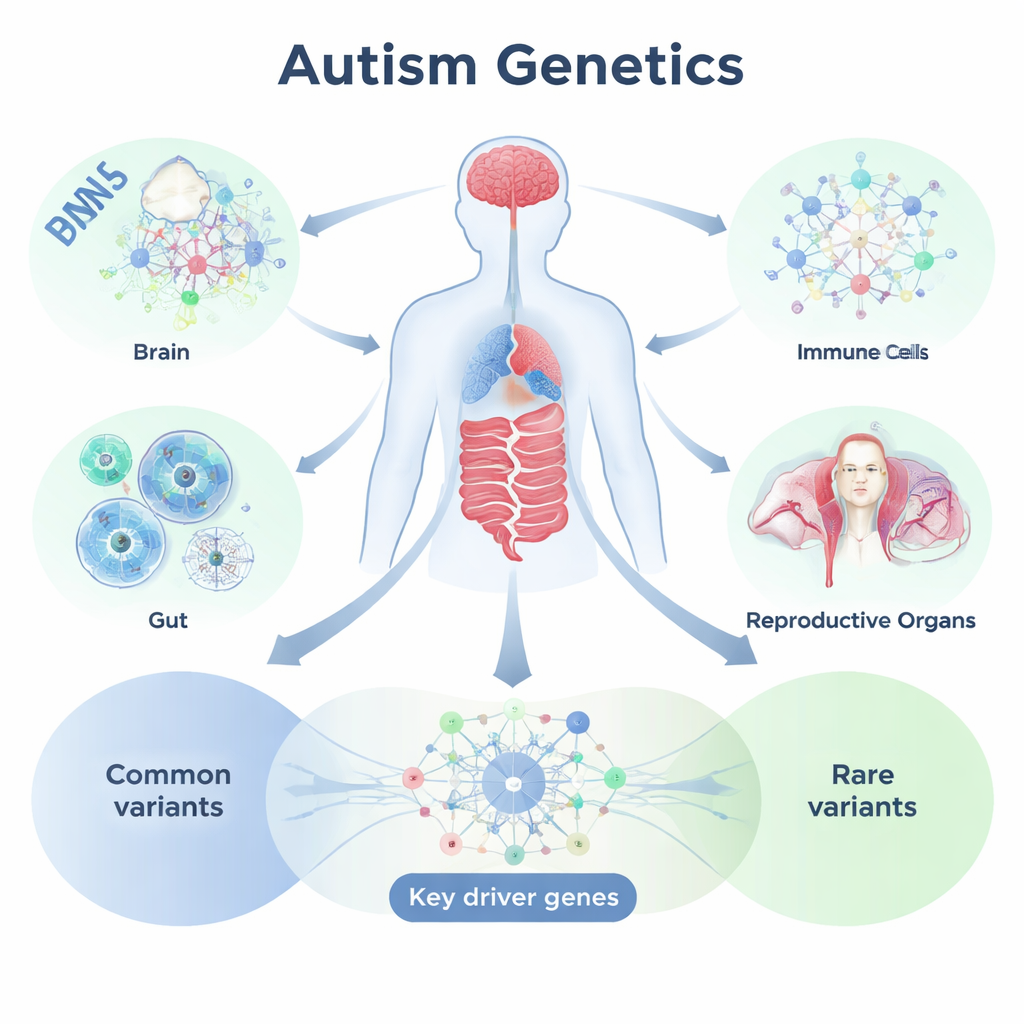
DNA-signalen in kaart brengen op weefsels en netwerken
Om dit aan te pakken gebruikte het team een analysekader genaamd Mergeomics, dat grootschalige genetische studies combineert met informatie over hoe genen aan- en uitgezet worden in specifieke weefsels. Ze begonnen met genome-wide associatiegegevens over meer dan negen miljoen veelvoorkomende DNA-varianten van meer dan 18.000 autistische personen en ongeveer 28.000 niet-autistische controles. Vervolgens koppelden ze deze varianten aan genen met behulp van gedetailleerde referentiegegevens over genactiviteit in bijna 50 weefsels, waaronder veel hersengebieden en ook spijsverterings-, immuun-, voortplantings- en andere perifere organen. Door genen te groeperen die samen worden aangezet in hetzelfde weefsel en te onderzoeken hoe sterk die genengroepen overeenkomen met autismegerelateerde varianten, identificeerden de onderzoekers weefselspecifieke “modules” en regulatorische netwerken die belangrijk lijken voor ASS.
Hersen en lichaam dragen beiden bij
De analyse bevestigde een centrale rol voor de hersenen — met name regio’s zoals de anterior cingulate cortex, amygdala, frontale cortex, cerebellum en bredere corticale gebieden, die bekend staan om hun betrokkenheid bij emotie, sociaal gedrag, denken en coördinatie. Genenetzwerken in deze hersengebieden bevatten zowel veelvoorkomende als zeldzame autismekoppelingen en waren verbonden met synaptische signalering, neuroontwikkeling en immuunregulatie binnen de hersenen. Toch stopte het beeld niet bij de schedel. Verrassend genoeg bevonden zich in veel perifere weefsels, met name in het spijsverteringsstelsel, immuunsysteem, endocriene en voortplantingsstelsels, ook genmodules die sterk werden beïnvloed door autismekoppelingen in de vorm van veelvoorkomende varianten. Deze modules waren geassocieerd met processen zoals immuunreacties, celgroei en celdeling, energieproductie, mRNA-splicing en een belangrijk regelpad dat bekendstaat als mTOR, die allemaal zijn gekoppeld aan hersenontwikkeling en gedrag.
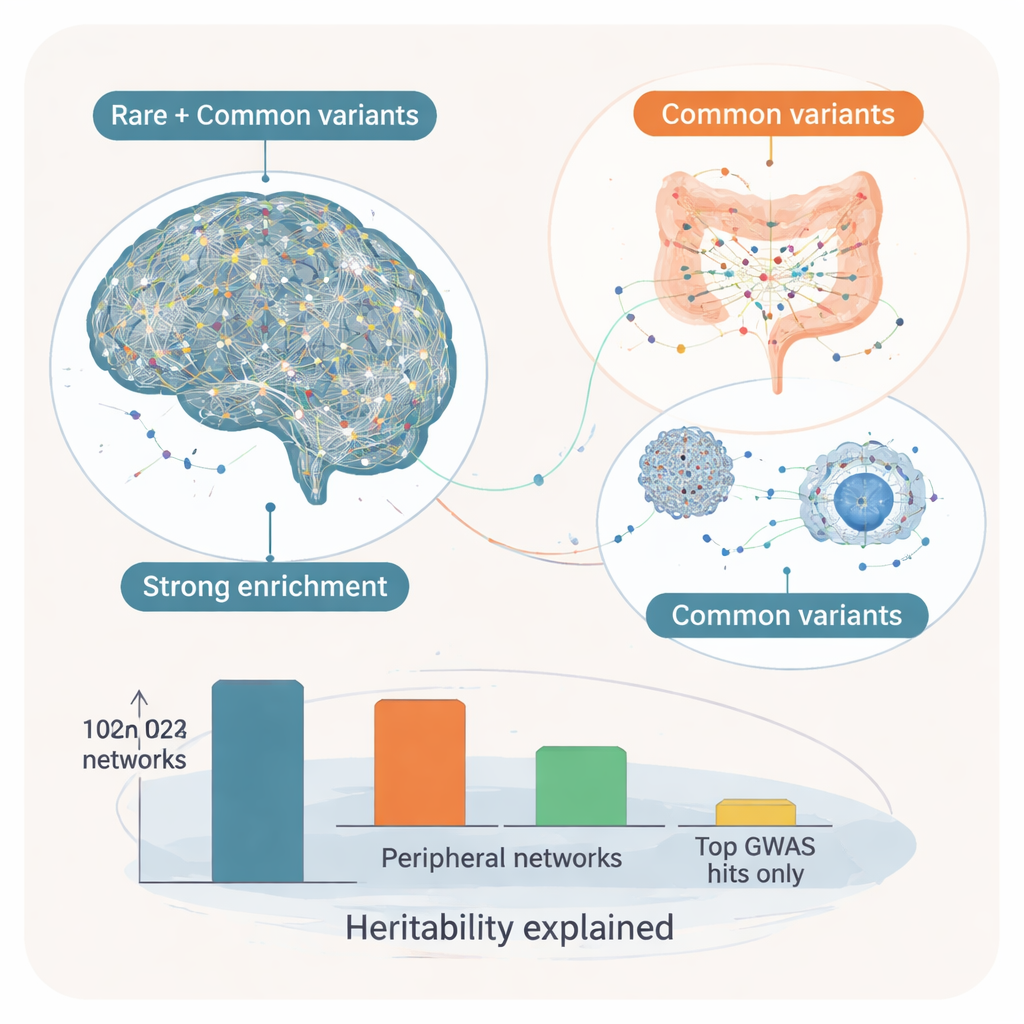
Sleutelcontrolegenen en het kern–modifier-idee
Door deze modules in richtinggevende genregulerende netwerken te plaatsen, onderzochten de onderzoekers vervolgens welke genen in de knooppunten zitten — zogenaamde “key drivers” die vele andere genen beïnvloeden. In hersennetwerken vertoonden deze key drivers sterke verrijking voor zeldzame, hoog-impact autismeveranderingen en ook voor veelvoorkomende varianten, wat suggereert dat ze een “kern” set genen vormen waar beide risicotypen samenkomen. Voorbeelden zijn SYT1, dat helpt bij het regelen van neurotransmitterafgifte bij synapsen, en ADD2, betrokken bij het vormen van neuronstructuur en connectiviteit. De omliggende netwerken bevatten een mix van bekende zeldzame autismegenen en doelwitten van veelvoorkomende varianten die betrokken zijn bij synaptische communicatie en neuronale prikkelbaarheid. In tegenstelling daarmee werden key drivers in perifere weefsels, vooral spijsverterings- en endocriene organen, meer beïnvloed door alleen veelvoorkomende varianten. Deze lijken te werken als “modifiers” die immuun-, metabole en signaalroutes afstemmen en daarmee kunnen bepalen hoe kernvulnerabiliteiten in de hersenen zich vertalen naar symptomen.
Wat dit betekent voor mensen en toekomstige behandelingen
Toen de auteurs inschatten hoeveel van het erfelijke risico op autisme aan deze netwerken kon worden toegeschreven, verklaarden hersengebaseerde modules ongeveer 7% van het erfelijke component en perifere modules nog eens 3% — samen omvatten ze bijna de volledige veelvoorkomende-variant-heritabiliteit die in de oorspronkelijke studie werd waargenomen en veel meer dan de kleine fractie verklaard door alleen de sterkste individuele DNA-signalen. Voor niet-specialisten is de conclusie dat de genetica van autisme een gelaagd patroon volgt: zeldzame en veelvoorkomende varianten komen samen op een kernset van hersengerichte netwerken die cruciaal zijn voor neuroontwikkeling, terwijl wijdverbreide veelvoorkomende varianten in darm-, immuun- en hormonale weefsels waarschijnlijk de loop en kenmerken van de aandoening moduleren. Dit kern–modifier-kader helpt verklaren waarom autisme er zo verschillend uitziet van persoon tot persoon en suggereert dat toekomstige therapieën niet alleen de hersenen, maar ook bredere lichamenstelsels die ermee in wisselwerking staan, moeten aanpakken.
Bronvermelding: Gill, C., Zuo, Y., Ha, D.Sm. et al. Convergence and divergence of genes informed by common and rare variants of autism spectrum disorders in tissue-specific pathways and gene networks. Transl Psychiatry 16, 98 (2026). https://doi.org/10.1038/s41398-026-03824-x
Trefwoorden: autisme genetica, zeldzame varianten, veelvoorkomende varianten, hersenetzwerken, darm–hersenas