Clear Sky Science · nl
Perinatale hyperandrogenisatie en immuunactivatie in knaagdiermodellen modelleren subtypen autisme
Hoe zwangerschap de zich ontwikkelende hersenen vormt
Waarom ontwikkelt het ene kind autisme en het andere niet, zelfs bij gedeelde genen en omgeving? Deze studie gebruikt muizen om twee omstandigheden te onderzoeken die bij mensen gekoppeld zijn aan een hoger risico op autisme: verhoogde mannelijke hormoonspiegels tijdens de zwangerschap en sterke immuunreacties bij de moeder. Door moederdieren en hun nakomelingen vanaf het late stadium van de zwangerschap tot de jeugd te volgen, laten de onderzoekers zien dat beide invloeden elk tot autisme‑achtige kenmerken kunnen leiden, maar met verschillende patronen van sociaal gedrag, hersenstructuur en immuunveranderingen.
Twee verschillende zwangerschapsrisico’s onder de loep
Het team richtte zich op twee reële risicofactoren. Ten eerste maakten ze een model van hoge androgeenblootstelling, vergelijkbaar met wat kan optreden bij vrouwen met polycysteus-ovariumsyndroom, een aandoening die met verhoogd testosteron gepaard gaat. Ten tweede simuleerden ze maternele immuunactivatie, wat een sterke immuunreactie op een infectie tijdens de zwangerschap nabootst. Zwangere muizen kregen of extra testosteron, een immuunstimulerend middel, beide, of geen van beide. De onderzoekers volgden vervolgens de pups’ vroege “babyroepjes”, sociaal gedrag tijdens juveniele fase, repetitief gedrag en hersenanatomie, terwijl ze ook placenta’s, foetale en pasgeboren hersenen en stress- en groeigerelateerde moleculen onderzochten.
Verschillende paden naar autisme‑achtig gedrag
Beide modellen leverden autisme‑achtige kenmerken op, maar niet op dezelfde manier. Pups die aan overtollige androgenen waren blootgesteld lieten vooral sterke veranderingen in sociale communicatie zien. Als pasgeborenen produceerden ze minder en kortere ultrasone geluiden — de hoogfrequente tonen die baby‑muizen gebruiken om de aandacht van hun moeder te trekken — maar die geluiden hadden een hogere toon dan normaal. Als juvenielen riepen deze muizen minder wanneer ze andere muizen ontmoetten en spendeerden ze minder tijd met een sociale partner. Interessant genoeg trokken ze, wanneer ze moesten kiezen tussen een bekende en een nieuwe muis, meer naar de nieuwe, wat suggereert dat hun basisdrang naar sociale verkenning veranderd was in plaats van gewoon verminderd. Daarentegen toonden nakomelingen van immuungeactiveerde moeders mildere sociale veranderingen maar een duidelijke toename van repetitief gedrag: ze begroeven in een standaardtest meer knikkers, wat repetitief, dwangmatig graafgedrag vastlegt.
Binnenin het veranderende brein en immuunsysteem
Hersenscans toonden dat mannelijken die aan androgenen waren blootgesteld een algeheel kleinere hersenomvang hadden — ongeveer 4 procent verminderd — maar dat bepaalde sleutelregio’s die betrokken zijn bij motivatie en sociaal gedrag, zoals de nucleus accumbens en een nabijgelegen stress- en emotiegerelateerd gebied genaamd de bed nucleus of the stria terminalis, relatief vergroot waren. Maternele immuunactivatie liet daarentegen de totale hersengrootte intact maar vergrootte selectief delen van de cortex, inclusief het cingulategebied, dat vaak wordt gekoppeld aan repetitief gedrag bij mensen met autisme. Op cellulair niveau toonden juvenielen die aan androgenen waren blootgesteld tekenen van aanhoudende neuro‑inflammatie: immuuncellen in de hippocampus, microglia genoemd, leken actiever en minder vertakt, een toestand die kan beïnvloeden hoe neurale circuits worden gesnoeid en verfijnd. De twee modellen produceerden ook verschillende handtekeningen in placentaire en neonatale hersenimmuunmoleculen, en tegenovergestelde veranderingen in twee belangrijke herseneiwitten — BDNF, dat de groei van neuronen ondersteunt, en de dopamine D2‑receptor, die helpt bij de regulatie van motivatie en beloning.
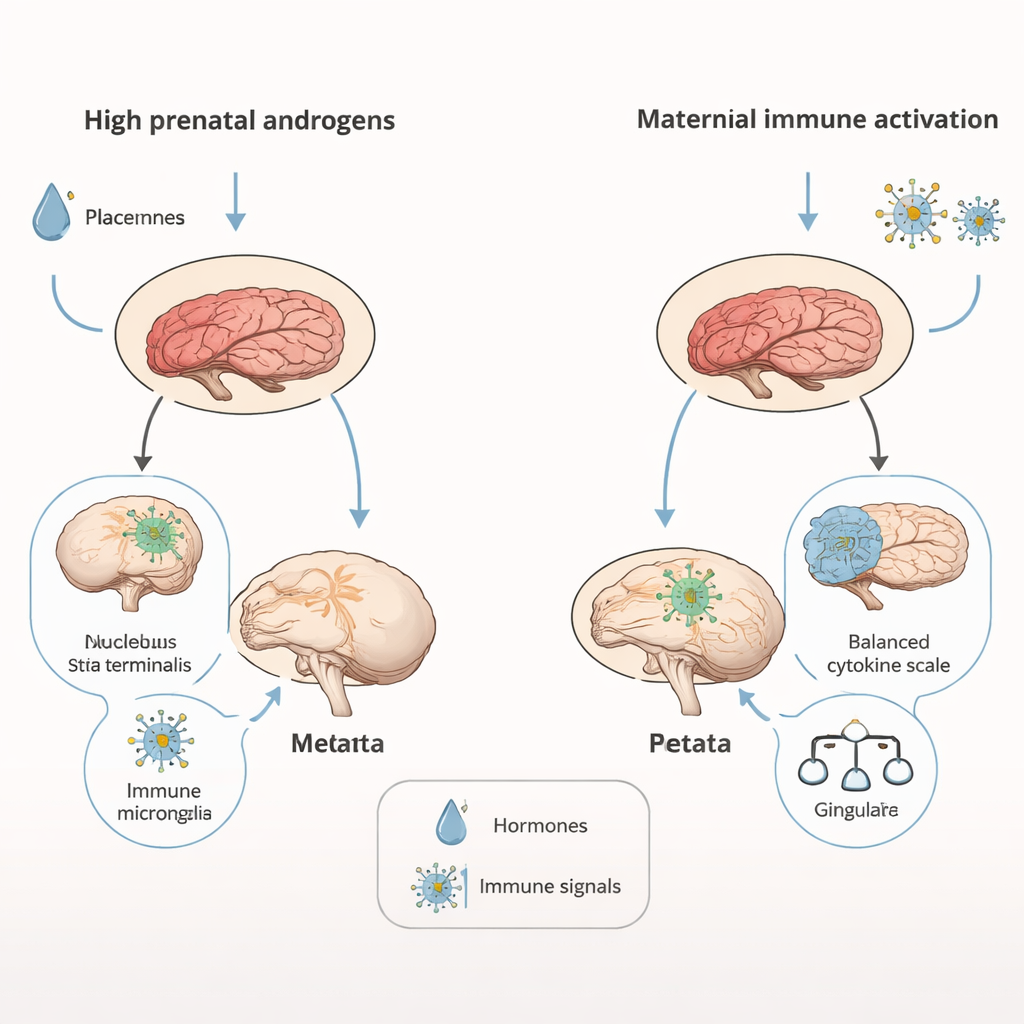
Wegwijzers naar autisme‑subtypen en sekseverschillen
Gezien de gedrags- en biologische bevindingen samen, lijken de twee muismodellen verschillende subtypen autisme bij mensen te weerspiegelen. Androgeenblootstelling verstoorde vooral sociale communicatie, met relatief weinig invloed op repetitief gedrag — vergelijkbaar met personen van wie de sociale moeilijkheden zwaarder wegen dan de repetitieve neigingen. Maternele immuunactivatie leverde het omgekeerde patroon op, met sterkere repetitieve gedragingen en subtielere sociale veranderingen. Omdat mannelijke foetussen van nature hogere androgeneniveaus ervaren dan vrouwelijke, ondersteunt de studie het idee dat zelfs matige toename van deze hormonen — of van hoe de hersenen erop reageren — kan bijdragen aan de hogere autismecijfers bij jongens, vooral voor het subtype dat gedomineerd wordt door sociale‑communicatieproblemen.
Wat dit betekent voor begrip van autisme
Voor niet‑wetenschappers is de kernboodschap dat “autisme” geen enkel pad of één hersenpatroon is. Bij deze muizen duwden extra mannelijke hormonen en sterke maternele immuunreacties de ontwikkeling elk richting autisme‑achtige uitkomsten, maar via verschillende biologische routes en met verschillende gedragsprofielen. Dit helpt verklaren waarom mensen met autisme zo uiteenlopend kunnen zijn. Het suggereert ook dat toekomstige behandelingen of preventiemaatregelen mogelijk moeten worden afgestemd op onderliggende oorzaken — of die nu meer hormoongerelateerd, immuungerelateerd of een mengeling van beide zijn — in plaats van aan te nemen dat alle autisme dezelfde biologie deelt.
Bronvermelding: Burke, F.F., Randell, A.M., Sparkes, K.M. et al. Perinatal hyperandrogenization and immune activation in rodents model subtypes of autism. Transl Psychiatry 16, 97 (2026). https://doi.org/10.1038/s41398-026-03821-0
Trefwoorden: autismesubtypen, prenatale hormonen, maternele immuunactivatie, neuroontwikkeling, knaagdiermodellen