Clear Sky Science · nl
Histamine H3-receptor als doelwit bij alcoholgebruikstoornis: de voorspelbaarheid van diermodellen voor klinische vertaling in geneesmiddelontwikkeling ter discussie
Waarom dit onderzoek van belang is voor het dagelijks leven
Alcoholgebruikstoornis treft miljoenen mensen wereldwijd, maar de beschikbare medicijnen helpen slechts een deel van degenen die ze nodig hebben. Dit artikel volgt de volledige reis van een veelbelovend nieuw kandidaatmedicijn, BP1.3656B, van laboratoriumbank tot menselijke proeven. Het laat zien hoe een idee dat prachtig werkt bij dieren toch kan mislukken bij mensen — en waarom die kloof ertoe doet voor iedereen die hoopt op betere behandelingen voor problematisch drinken.
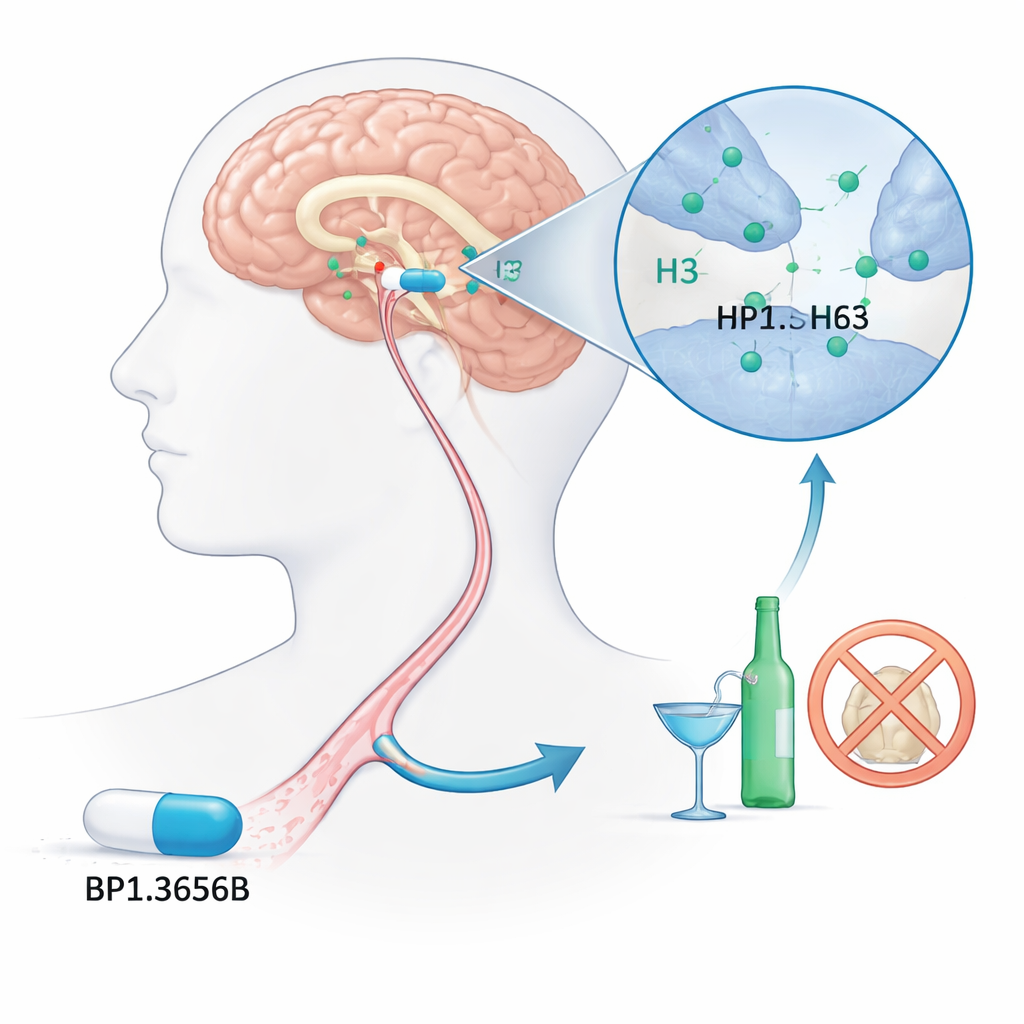
Een nieuw doelwit in de hersenen voor problematisch drinken
De onderzoekers richtten zich op een minder bekende schakel in de hersenen, de histamine H3-receptor. Histamine is vooral bekend om zijn rol bij allergieën, maar in de hersenen reguleert het waakzaamheid en de communicatie tussen zenuwcellen. De H3-receptor werkt als een dimmer en zet de afgifte van histamine en meerdere andere signaalstoffen die betrokken zijn bij beloning en motivatie omlaag. Omdat alcohol sterk met deze hersensystemen samenwerkt, vermoeden wetenschappers al lang dat het blokkeren van H3-receptoren de drang om te drinken zou kunnen verminderen. BP1.3656B werd ontworpen als een krachtige remmer van H3, in de hoop dat het de aantrekkingskracht van alcohol op de beloningscircuits van de hersenen zou kunnen verzwakken.
Van chemie naar succesverhalen in dierstudies
In vroege testen toonde BP1.3656B het profiel waar geneesmiddelontwikkelaars van dromen. Het bindde zeer sterk en selectief aan de H3-receptor, drong goed de hersenen binnen en leek veilig in standaard laboratoriumtests. Bij muizen verminderde het middel de uitbarsting van activiteit die normaal volgt op een alcoholinjectie en sneed het binge-achtig drinken in de “drinking in the dark”-test licht terug. Bij ratten die geleerd waren op een hendel te drukken voor alcohol, verminderde BP1.3656B scherp de hoeveelheid die ze dronken en hoe hard ze bereid waren te werken om alcohol te krijgen, zowel bij dieren die simpelweg veel dronken als bij dieren die lichamelijk afhankelijk waren gemaakt. Het dempte ook relapse-achtig drinken en verlichtte angst gerelateerd aan alcoholonttrekking. Al met al suggereerden deze resultaten dat het middel de motivatie voor alcohol kon verlagen en kon helpen een terugval naar zwaar gebruik te voorkomen.
Vroege tests bij mensen: bereikt het middel zijn doel?
Vervolgens volgden fase I-studies bij gezonde vrijwilligers. Enkele en herhaalde doseringen tot 90 microgram werden over het algemeen goed verdragen, met voornamelijk milde slaapgerelateerde bijwerkingen die passen bij het waakzaamheidsbevorderende karakter van H3-remmers. Bloedmetingen lieten een duidelijk, voorspelbaar patroon zien van hoe het middel werd opgenomen en afgevoerd. Om zeker te weten dat het zijn beoogde doel in het levende menselijk brein raakte, gebruikte het team positronemissietomografie, een type hersenscan dat kan laten zien hoeveel receptoren door een middel bezet zijn. Zelfs relatief lage doses BP1.3656B blokkeerden de meeste H3-receptoren in meerdere hersengebieden die belangrijk zijn voor motivatie en beloning, wat bevestigde dat het middel, althans biologisch gezien, deed wat het ontworpen was te doen.
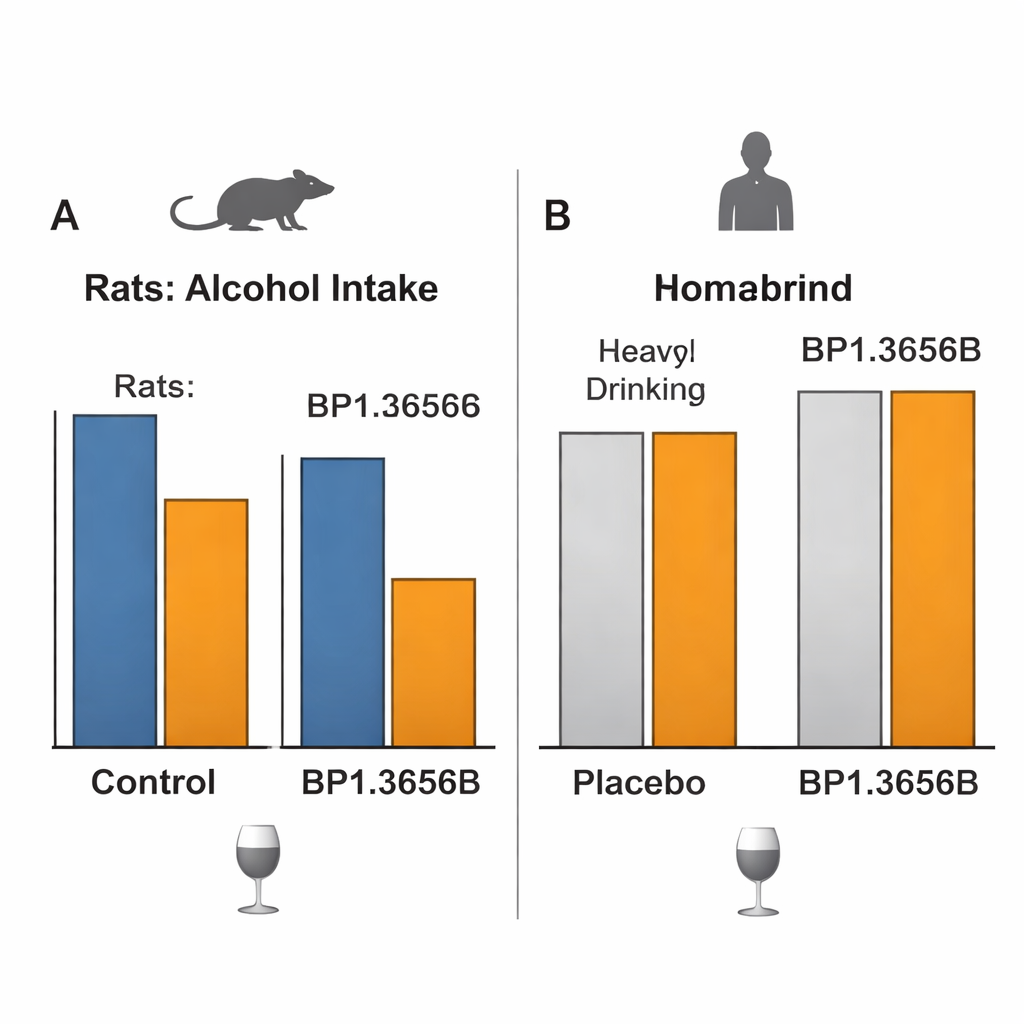
Wanneer veelbelovende dierresultaten niet vertalen naar mensen
De cruciale vraag was of dit alles zou vertalen in betekenisvolle veranderingen in drinkgedrag bij mensen met een alcoholgebruikstoornis. In een zorgvuldig gecontroleerde laboratoriumstudie kregen volwassenen met alcoholproblemen die geen behandeling zochten BP1.3656B of placebo en voltooiden ze sessies waarin ze intraveneuze alcohol zelf konden toedienen door op een knop te drukken, onder condities die zowel plezier als motivatie moesten meten. Het middel had geen waarneembaar effect op hoeveel alcohol ze kozen te ontvangen. Een grotere, 12 weken durende, multicenter klinische studie bij patiënten die behandeling zochten testte vervolgens drie dagelijkse doseringen BP1.3656B versus placebo. Alle groepen, inclusief placebo, verminderden in de loop van de tijd het aantal zware drinkdagen en de totale alcoholinname aanzienlijk, maar het middel presteerde niet beter dan placebo op enige belangrijke maat van drinken of verlangen, ondanks een goede veiligheid en duidelijke targetbezetting.
Wat dit betekent voor toekomstige behandelingen
Voor een niet-specialistische lezer is de conclusie nuchter maar belangrijk: een middel dat uitstekend leek in cellen, muizen en ratten — en duidelijk zijn doel in het menselijk brein bereikte — mislukte toch in het helpen van mensen om minder te drinken. Dat betekent niet dat de wetenschap een fout was, maar het benadrukt hoe onzeker het is om menselijke uitkomsten alleen op basis van diermodellen te voorspellen. De auteurs pleiten ervoor dat kleinere, vroege humane laboratoriumstudies die rechtstreeks de impact van een middel op alcoholgebruik testen, vaker gebruikt worden om de ontwikkeling te “ont-risken” voordat er grote, dure proeven worden opgezet. Met andere woorden, dit werk laat zien dat we niet alleen nieuwe medicijnideeën nodig hebben, maar ook betere manieren om te beslissen welke van die ideeën echt een kans hebben om mensen met een alcoholgebruikstoornis te helpen.
Bronvermelding: Le Foll, B., Naassila, M., Jeanblanc, J. et al. Histamine H3 Receptor as a target for alcohol use disorder: challenging the predictability of animal models for clinical translation in drug development. Transl Psychiatry 16, 55 (2026). https://doi.org/10.1038/s41398-026-03807-y
Trefwoorden: alcoholgebruikstoornis, histamine H3-receptor, BP1.3656B, verslavingsbehandeling, translational research