Clear Sky Science · nl
Spi-1 proto-oncogen reguleert mRNA-hypertranscriptie en kwaadaardige progressie bij hoofd- en halskanker
Waarom deze kankerstudie ertoe doet
Hoofd- en halskankers komen vaak voor en zijn regelmatig dodelijk, deels omdat veel tumoren blijven groeien, uitzaaien en terugkeren ondanks agressieve behandeling. Deze studie behandelt een schijnbaar eenvoudige vraag met grote implicaties: wat gebeurt er wanneer kankercellen het volume van al hun genactiviteit tegelijk opvoeren en ongewoon grote hoeveelheden boodschapper-RNA (mRNA) produceren, de moleculen die de eiwitproductie aansturen? Door één enkele regelaar te identificeren die deze overactieve toestand voedt, ontdekken de auteurs een mogelijke kwetsbaarheid in sommige van de gevaarlijkste hoofd- en hals tumoren.
Cellen die in versneld afspelen leven
Ieder cel heeft mRNA nodig om eiwitten op te bouwen, maar kankercellen gedragen zich vaak als fabrieken die vastzitten in overdrive. De onderzoekers richtten zich op “mRNA-hypertranscriptie”, een toestand waarbij cellen wereldwijd de productie van eiwitcoderende berichten opvoeren in plaats van slechts een paar kankerlijnen. Met enkelcelsequencing van meer dan 100.000 cellen van 12 patiënten telden ze mRNA-moleculen cel voor cel. Tumorcellen met de hoogste totale mRNA-uitvoer waren minder geëvolueerd, flexibeler in hun identiteit en vol actieve routes die groei, stressbestendigheid en beweeglijkheid ondersteunen. Toen ze de analyse uitbreidden naar een grote openbare kanker-database, bleken patiënten wiens tumoren deze hoge-uitvoer toestand toonden een aanzienlijk slechtere overleving te hebben, zelfs nadat factoren zoals tumorstadium en infectie met humaan papillomavirus werden meegewogen. 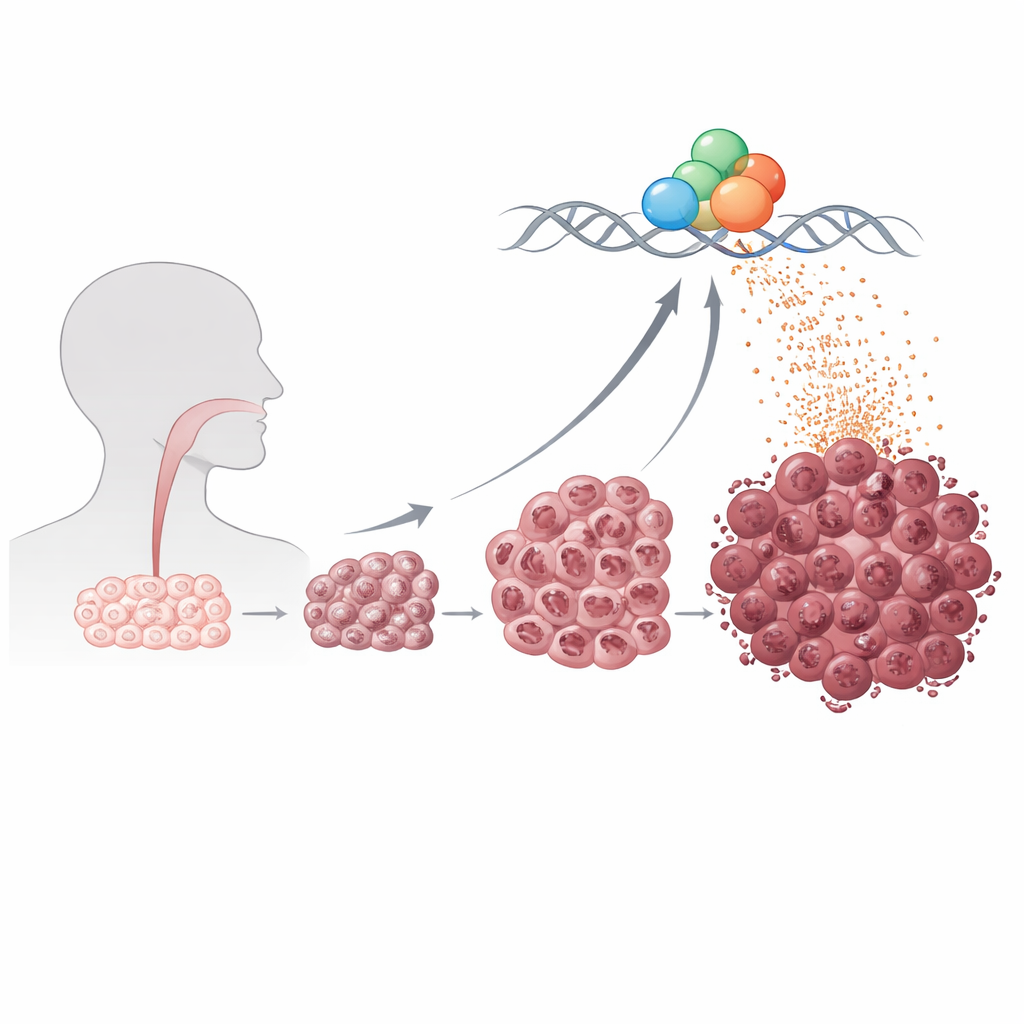
Een hoofdschakel genaamd SPI1
Om te begrijpen wat deze hyperactieve berichtgeving aandrijft, zocht het team naar transcriptiefactoren — eiwitten die op DNA zitten en bepalen welke genen worden aangezet — die bijzonder actief waren in tumorcellen met hoge output. Eén factor sprong eruit: SPI1, ook bekend als PU.1, eerder vooral in verband gebracht met bloedkankers. In hoofd- en hals tumoren nam SPI1-activiteit gelijktijdig toe met het totale mRNA-niveau, zowel in patiëntmonsters als in kankercellijnen. Tumoren met meer SPI1-activiteit waren rijker aan kankerverwekkende routes en waren gekoppeld aan slechtere uitkomsten voor patiënten. Binnen individuele tumoren waren dezelfde cellen die sterke SPI1-signalen vertoonden ook degene met de meest intense mRNA-productie, wat wijst op een directe verbinding tussen deze factor en de overbelaste toestand.
SPI1 in het lab omhoog en omlaag draaien
De auteurs vroegen vervolgens of SPI1 louter een begeleider is van agressieve ziekte of er daadwerkelijk aan bijdraagt. In gekweekte hoofd- en hals kankercellen die van nature veel SPI1 maken, gebruikten ze genetische middelen om het eiwit terug te schakelen. Deze cellen vertraagden in groei, vormden minder kolonies, migreerden en infiltreerden minder, en vertoonden meer tekenen van geprogrammeerde celdood. Wanneer deze verzwakte cellen in muizen werden ingebracht, waren de resulterende tumoren kleiner, groeiden ze langzamer en bevatten ze minder delende cellen en meer stervende cellen. Het omgekeerde experiment bevestigde het beeld: het verhogen van SPI1 in laag-expressieve kankercellen versnelde groei en invasie in kweek en produceerde grotere, sneller groeiende tumoren in dieren.
Hoe SPI1 de genoutput overstroomt
Om de impact van SPI1 op genactiviteit zelf te meten, volgde het team nieuwgemaakt RNA met een chemisch label en kwantificeerde direct gezuiverd mRNA per cel. Het verlagen van SPI1-niveaus verminderde zowel de nieuwe RNA-synthese als het totale mRNA, terwijl het dwingen van cellen om meer SPI1 te maken deze verhoogde. Met systemen die SPI1 snel konden inschakelen, toonden ze aan dat de mRNA-productie binnen uren stijgt, wat wijst op een tijdsafhankelijke boost. Genoomwijde bindingsexperimenten lieten zien dat SPI1 zich bij duizenden genen in de buurt van de startplaatsen vestigt en fungeert als een brede activator, vooral van routes die verband houden met energiegebruik, celbeweging en stressresponsen. Gezamenlijk schetsen deze bevindingen SPI1 als een hoofdregelaar die kankercellen in een hypertranscriptietoestand duwt in plaats van slechts een paar geïsoleerde genen bij te stellen. 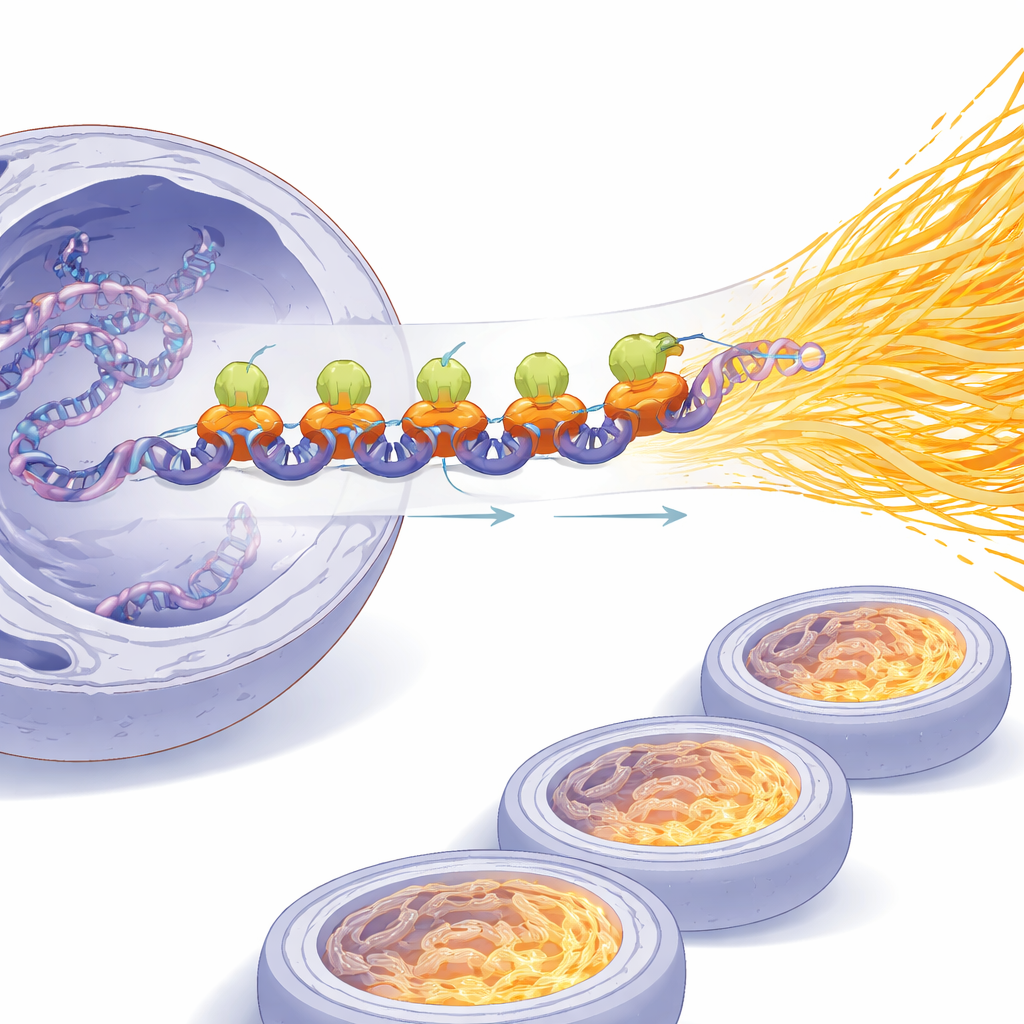
Wat dit voor patiënten betekent
Tot slot onderzochten de onderzoekers tumorstalen van twee onafhankelijke patiëntengroepen die in één ziekenhuis werden behandeld. Zowel bij strottenhoofd- als hypofarynxkankers waren SPI1-eiwitniveaus duidelijk hoger in tumorweefsel dan in nabijgelegen gezond weefsel. Patiënten van wie de tumoren meer SPI1 bevatten hadden een kortere totale overleving, en deze associatie bleef bestaan zelfs na correctie voor standaard klinische kenmerken zoals stadium. Hoewel er momenteel geen medicijnen zijn die SPI1 direct remmen, suggereert dit werk dat het verstoren van zijn activiteit — of van het achterliggende transcriptieapparaat waarop het vertrouwt — de hoge-risico hoofd- en halskankers zou kunnen vertragen of beteugelen. Eenvoudig gezegd laat de studie zien dat sommige tumoren bijzonder gevaarlijk worden door het globale "gaspedaal" voor genactiviteit in te trappen, en dat SPI1 een van de belangrijke voeten is die dat pedaal naar beneden drukt.
Bronvermelding: Liu, Z., Qin, Z., Li, H. et al. Spi-1 proto-oncogene regulates mRNA hypertranscription and malignant progression in head and neck cancer. Sig Transduct Target Ther 11, 102 (2026). https://doi.org/10.1038/s41392-026-02669-6
Trefwoorden: hoofd- en halskanker, mRNA-hypertranscriptie, SPI1 transcriptiefactor, tumorprogressie, kankerbiomarkers