Clear Sky Science · nl
Cyclisch guanosine-monofosfaat–proteïnekinase G-signaal remt verkalking van de aortaklep via ULK1-gemedieerde autofagie
Waarom „roest” van de hartklep ertoe doet
Met het ouder worden kan de aortaklep—de belangrijkste uitgang van het hart—geleidelijk stug worden en bedekt raken met calcium; dit wordt verkalkende aortaklepaandoening genoemd. Deze „verharding” dwingt het hart harder te pompen en kan leiden tot pijn op de borst, flauwvallen, hartfalen of de noodzaak van klepvervangende chirurgie. Er is momenteel geen geneesmiddel dat dit proces betrouwbaar vertraagt; artsen kunnen alleen wachten tot de klep ernstig beschadigd is en dan opereren. Deze studie verkent een ingebouwd cellulair pad dat de klep tegen verkalking lijkt te beschermen, en test een modern hartfalengeneesmiddel als mogelijke manier om die bescherming weer aan te zetten.
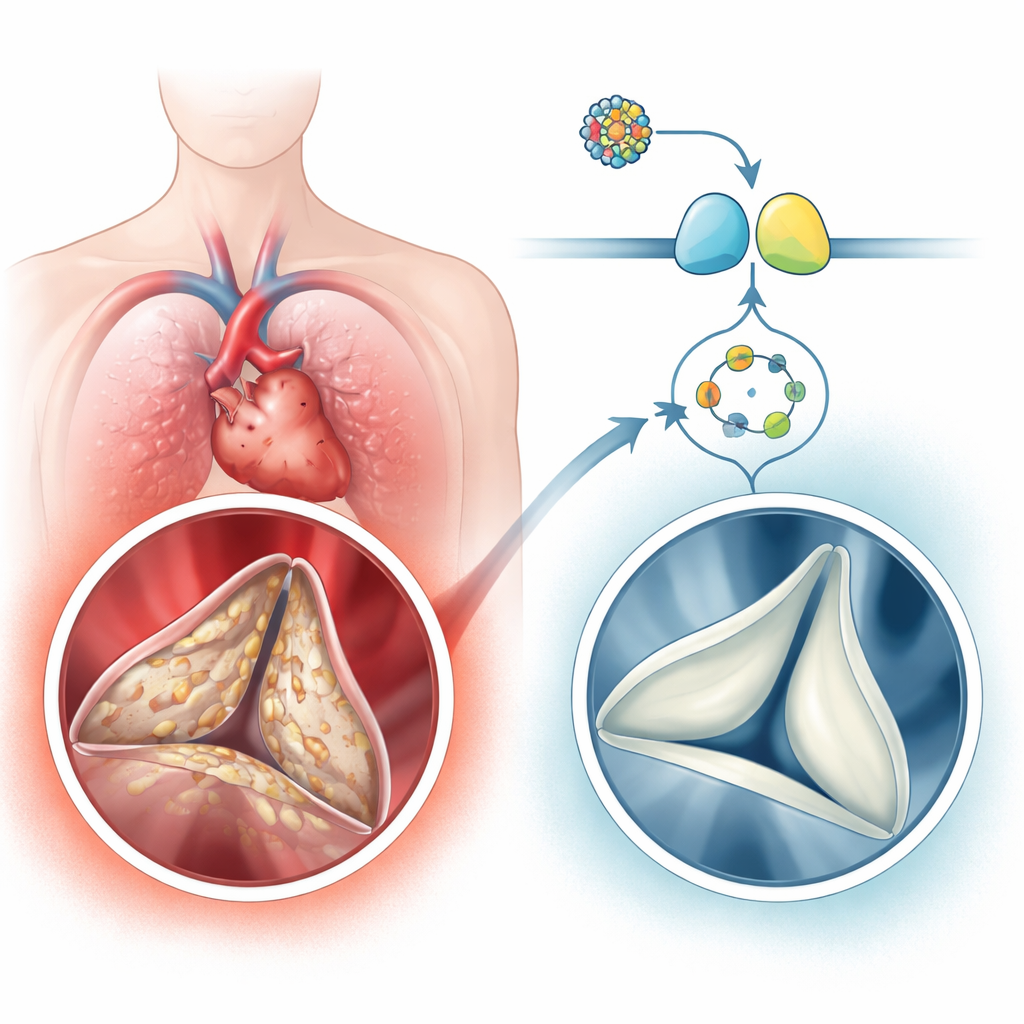
Een veelvoorkomend maar onderbelicht hartprobleem
Verkalkende aortaklepaandoening komt verrassend vaak voor bij oudere volwassenen, en treft enkele procenten van de mensen boven 65 en tot één op de tien boven 75. De ziekte is niet slechts passieve „slijtage.” In plaats daarvan schakelen de zachte bindweefselcellen in de klep, bekend als valvulaire interstitiële cellen, over naar wondherstellende en botachtige toestanden. Ze leggen extra collageen neer en zetten vervolgens calcium af, waardoor de ooit flexibele klepbladen veranderen in stijve, steenachtige flappen. De auteurs analyseerden menselijk klepweefsel en grote genexpressiedatasets en vonden dat een signaalroute rond het kleine molecuul cGMP en het partnerenzym proteïnekinase G (PKG) consequent omlaag was gereguleerd in verkalkte kleppen, terwijl genen en eiwitten die met botvorming geassocieerd zijn omhoog stonden. Mensen met ernstige klepverkalking hadden ook lagere cGMP-niveaus in hun bloed, wat samenhing met hoe vernauwd en geblokkeerd hun kleppen waren.
Een beschermend signaal dat verdwijnt
Om oorzaak en gevolg te onderzoeken, gebruikte het team muizen en gekweekte humane klepcellen. Muizen die zodanig waren aangepast dat ze minder PKG maakten, ontwikkelden dikkere, zwaarder verkalkte klepbladen na een gecontroleerde beschadiging van de aortaklep, en hun kleppen vertoonden hogere niveaus van een sleuteleiwit voor botvorming. In humane klepcellen gekweekt in een schaaltje onder omstandigheden die calciumafzetting bevorderen, versnelde het terugschakelen van PKG met genetische middelen deze botachtige transformatie. Deze resultaten suggereren dat cGMP–PKG-signaal normaal gesproken fungeert als rem op schadelijke celherschikking in de klep—en wanneer deze rem verzwakt, versnelt de verkalking.
Herbestemming van een hartfalengeneesmiddel
De onderzoekers vroegen zich vervolgens af of het verhogen van dit pad verkalking kon vertragen of omkeren. Ze testten drie geneesmiddelen die cGMP op verschillende manieren verhogen, waaronder vericiguat, een goedgekeurd middel voor bepaalde patiënten met hartfalen. In humane klepcellen verminderden alle drie de middelen kalkafzettingen en merkers van botachtige verandering, waarbij vericiguat het sterkste effect liet zien. Vericiguat verminderde ook verkalking in kleine stukken menselijk klepweefsel die buiten het lichaam werden levend gehouden. In twee muismodellen—één aangedreven door een hoog-cholesterol dieet en één door mechanisch letsel aan de klep—leidde dagelijkse behandeling met vericiguat tot dunnere, minder verkalkte klepbladen en betere bloeddoorstroming over de klep, zonder het pompen van het hart te verzwakken. Toen PKG echter genetisch werd gereduceerd, verloor vericiguat grotendeels zijn voordelen, wat aangeeft dat PKG de sleutelspeler stroomafwaarts is.
Cellulaire opruiming, gezondere kleppen
Dieper gravend vonden het team dat vericiguat en PKG de kleine energiecentrales van klepcellen, de mitochondriën, beschermden. Onder verkalkende omstandigheden bouwden cellen schadelijke reactieve zuurstofsoorten op, verloren ze mitochondriale membraanpotentiaal en produceerden minder energie. Vericiguat herstelde de mitochondriale functie en verminderde oxidatieve stress. Grootschalige eiwit- en fosfaat-tagmapping wees hen in de richting van autofagie—het intracellulaire opruim- en recyclingsysteem. In verkalkte menselijke kleppen toonden microscopische beelden en eiwitmerkers verminderde vorming en activiteit van autophagosomen, de „vuilniszakken” van autofagie. In single-cell-analyses lieten meerdere subtypes klepcellen uit zieke kleppen een brede onderdrukking van autofagie-gerelateerde programma’s zien. In gekweekte cellen wist het blokkeren van autofagie het beschermende effect van PKG-activatie uit, wat impliceert dat PKG grotendeels werkt door dit opruimsysteem te herstellen.
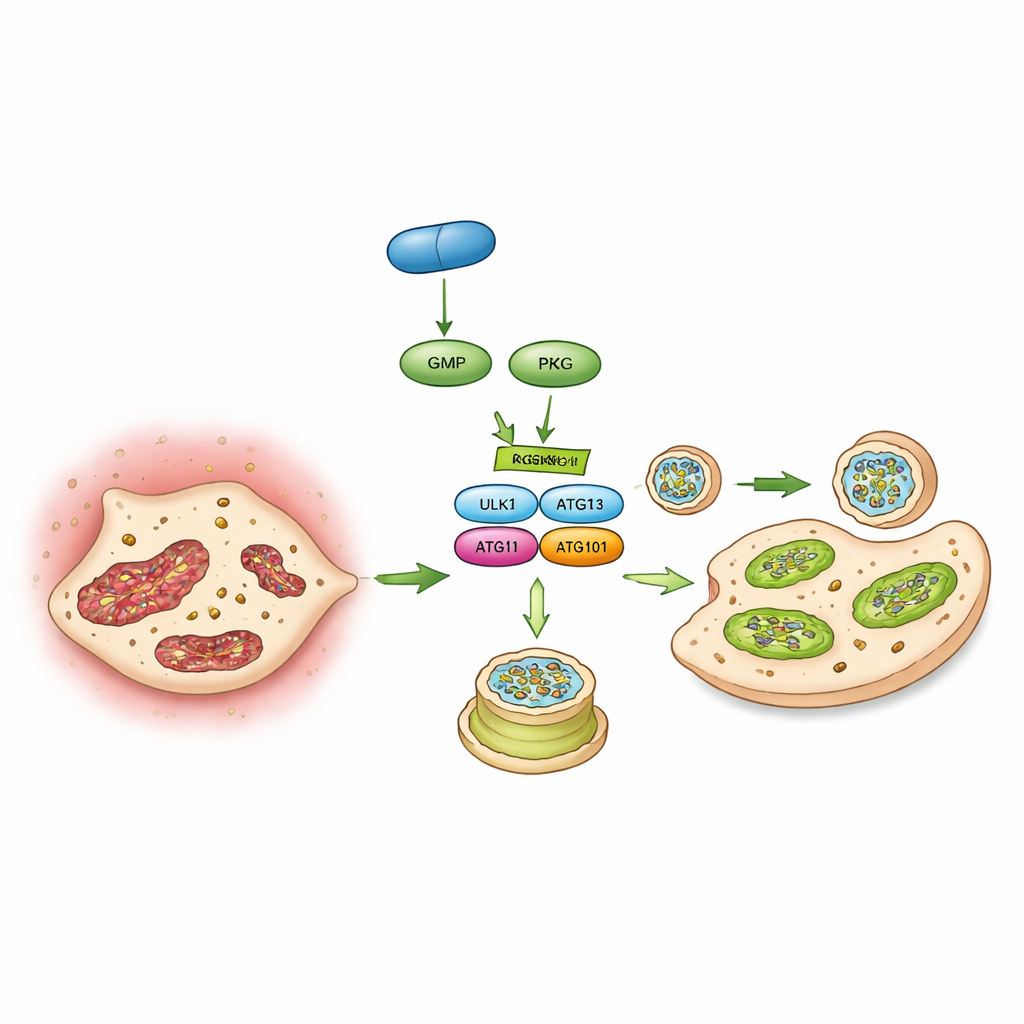
Het omschakelen van een moleculaire schakelaar
Ten slotte identificeerden de auteurs een specifieke moleculaire schakel die PKG verbindt met autofagie: een eiwit genaamd ULK1 dat de vorming van autophagosomen op gang brengt. Met behulp van fosfoproteomics, interactiestudies en kinase-assays in reageerbuis toonden ze aan dat PKG direct een fosfaatgroep aan ULK1 bindt op een specifieke plaats (een aminozuur dat serine 556 wordt genoemd). Wanneer deze plaats werd gemuteerd zodat hij niet langer gemodificeerd kon worden, kon PKG autofagie niet meer stimuleren of verkalking in klepcellen blokkeren. In muizen veegde het tot expressie brengen van dit niet-reagerende ULK1-mutant in klepcellen ook het beschermende vermogen van vericiguat weg. Gezamenlijk schetsen deze bevindingen een keten van gebeurtenissen: vericiguat stimuleert cGMP, wat PKG activeert, dat de ULK1-schakelaar omzet, waardoor autofagie herleeft, mitochondriën behouden blijven en klepcellen niet veranderen in botvormende cellen.
Wat dit voor patiënten zou kunnen betekenen
Dit werk positioneert de cGMP–PKG–ULK1–autofagie-as als een ingebouwd verdedigingssysteem tegen „roesten” van de aortaklep. Bij verkalkende klepaandoening is die verdediging verzwakt, waardoor cellen schade ophopen en afdrijven naar een botachtige identiteit. Door het signaal farmacologisch te herstellen met een geneesmiddel dat al in de hartfalenzorg wordt gebruikt, vertraagden de onderzoekers verkalking in verschillende experimentele modellen. Hoewel klinische studies bij mensen met klepaandoening nodig zullen zijn, biedt de studie een duidelijk, toetsbaar idee: het voorzichtig versterken van dit cellulaire opruimproces kan op een dag mogelijk het uitstel of de vermindering van de noodzaak voor klepvervangende chirurgie bij oudere volwassenen met risico op aortastenose bewerkstelligen.
Bronvermelding: Wang, Y., Xu, F., Song, C. et al. Cyclic guanosine monophosphate-protein kinase G signaling attenuates aortic valve calcification through ULK1-mediated autophagy. Sig Transduct Target Ther 11, 90 (2026). https://doi.org/10.1038/s41392-026-02624-5
Trefwoorden: verkalkende aortaklepaandoening, cGMP PKG-signaal, vericiguat, autofagie, hartklepverkalking