Clear Sky Science · nl
Glucocorticoïden verhogen de gevoeligheid van clear cell niercelcarcinoom voor HIF-2α-remmers door remming van H4K12-lactylering
Waarom deze studie naar nierkanker belangrijk is
Clear cell nierkanker is de meest voorkomende en dodelijkste vorm van nierkanker, en veel patiënten krijgen nog steeds een terugval of reageren niet op de huidige medicijnen. Deze studie onthult een verborgen “verslaving” van deze tumoren aan een specifieke manier van suikerverbranding en het gebruik van het bijproduct lactaat om kankerveroorzakende genen aan te houden. Belangrijker nog, de studie toont aan dat een bekende klasse geneesmiddelen — glucocorticoïden, zoals dexamethason — kunnen worden hergebruikt om deze verslaving te verzwakken en een nieuw gericht geneesmiddel, de HIF-2α-remmer belzutifan, beter te laten werken.
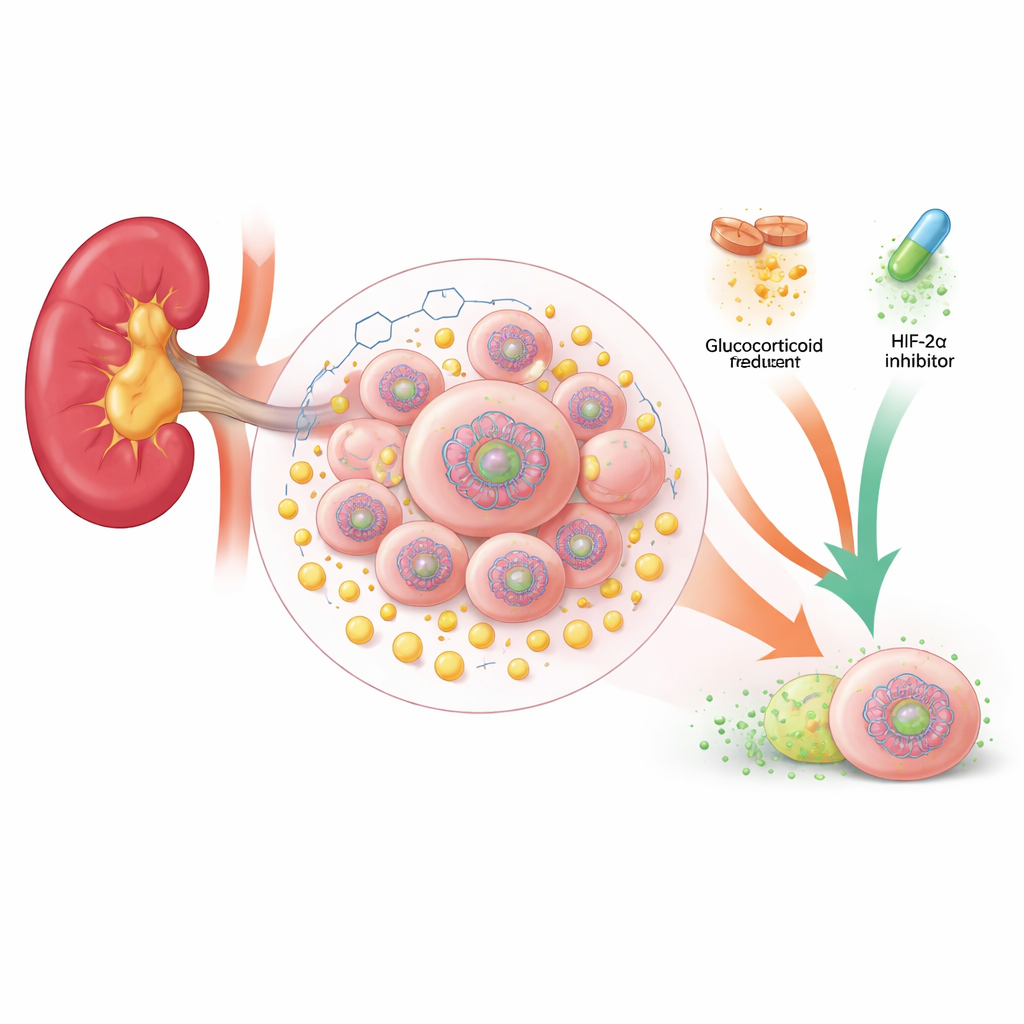
Een suikergestuurde lus binnen niertumoren
Veel clear cell-nierkankers verliezen een sleutelgen dat bescherming biedt, genaamd VHL. Zonder VHL gedragen cellen zich alsof ze zuurstofgebrek hebben, ook als dat niet het geval is. Ze verschuiven hun metabolisme weg van efficiënte energieproductie in mitochondriën naar een snelle maar minder efficiënte route genaamd glycolyse, die energie levert en grote hoeveelheden lactaat produceert. De auteurs ontdekten dat in VHL-deficiënte niertumoren lactaat meer doet dan alleen ophopen als afvalstof: het komt de celkern binnen en labelt chemisch de eiwitten die het DNA verpakken. Vooral een merkteken dat H4K12-lactylering heet, was opvallend verhoogd in patiëntentumoren en werd geassocieerd met grotere, agressievere tumoren en slechtere overleving.
Hoe lactaat helpt dat kankergenen aan blijven staan
Door in kaart te brengen waar dit lactaatgebaseerde merkteken op het DNA zit in kankercellen, ontdekte het team dat het sterk geconcentreerd is bij de "aan"-schakelaars (promoters) van genen die tumorgroei en suikerverbranding stimuleren. Een opvallend gen is PGK1, een enzym dat helpt suiker door de glycolytische route te duwen richting lactaat. In VHL-deficiënte cellen en muismodellen leidde meer PGK1 tot meer lactaat, wat op zijn beurt tot meer H4K12-lactylering op PGK1 en andere groeigenen leidde. Dit creëerde een zichzelf versterkende lus: PGK1 verhoogt lactaat; lactaat voorziet chromatine van het H4K12-merkteken; dat merkteken houdt PGK1 en andere tumorpromoterende genen hoog actief, waardoor de kanker vastgezet wordt in een rigide, hoog-glycolytische toestand.
De lus doorbreken met bestaande medicijnen
De onderzoekers vroegen zich vervolgens af of goedgekeurde medicijnen deze lactaat–chromatine-lus konden dempen. Een screening van 2.468 door de FDA goedgekeurde verbindingen in nierkankercellen bracht een verrassende lijst van hits aan het licht: meerdere glucocorticoïden verminderden het H4K12-merkteken aanzienlijk. Dexamethason bleek het krachtigst en verlaagde H4K12-lactylering zelfs bij lage doses. Deze hormonen werken via de glucocorticoïdreceptor, een eiwit dat naar de kern verhuist en aan DNA bindt wanneer het medicijn aanwezig is. In de kankercellen viel binding van de glucocorticoïdreceptor bij de promoters van glycolysegenen samen met verlies van het H4K12-merkteken en verminderde activiteit van PGK1 en andere suikerverbrandingsgenen. Daardoor produceerden de cellen minder lactaat en verschoof hun metabolisme weer richting meer normaal, zuurstofgebaseerd energiegebruik.
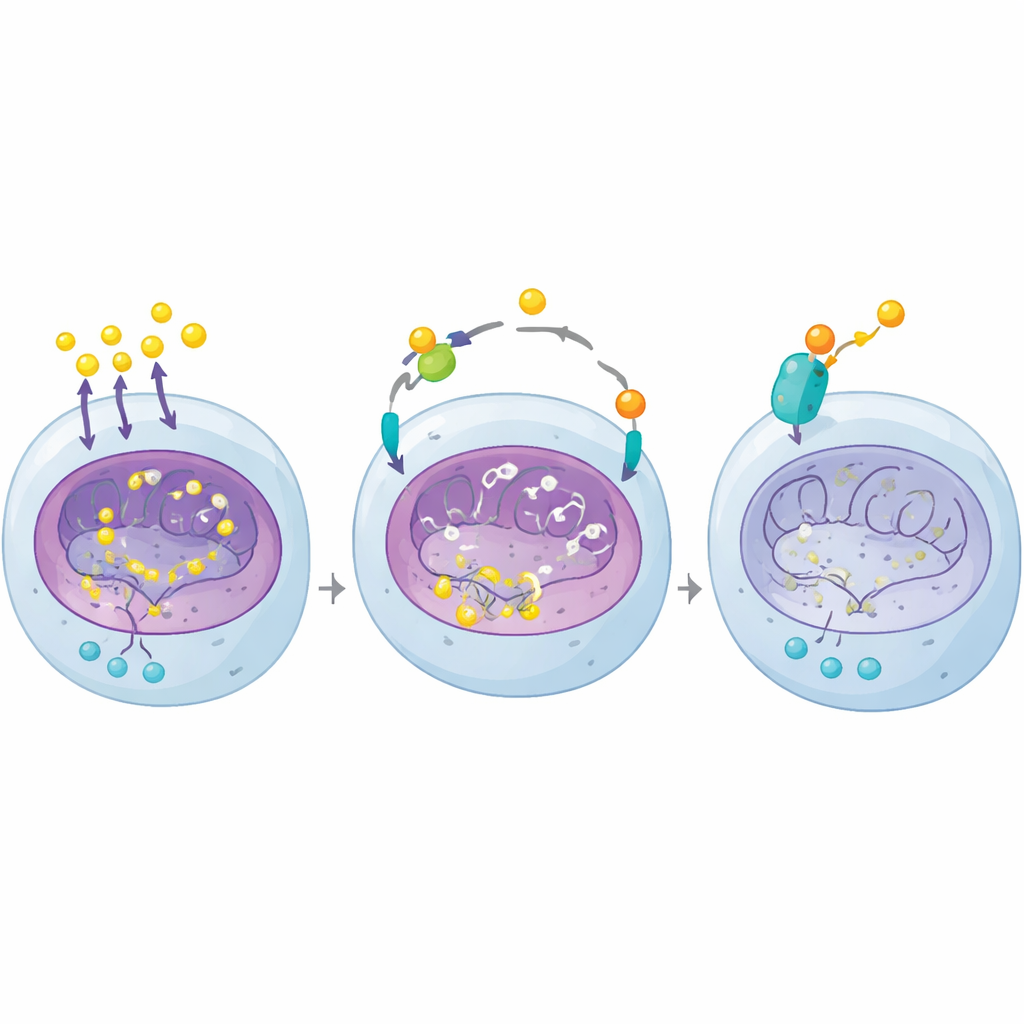
Een gerichte kankergeneesmiddel harder laten werken
Belzutifan, een recent goedgekeurde HIF-2α-remmer, blokkeert rechtstreeks een van de belangrijkste downstream-effectoren van VHL-verlies en heeft voordeel laten zien bij patiënten met gevorderd clear cell niercelcarcinoom. Reacties zijn echter onvolledig en vaak van korte duur. Omdat dexamethason het door lactaat aangedreven chromatineprogramma van de kanker vanuit een andere hoek aanvalt, testten de auteurs de twee geneesmiddelen samen in muismodellen. In tumoren gekweekt uit celijnen en uit patiënweefsel krompen VHL-deficiënte tumoren veel meer bij de combinatie van glucocorticoïden plus belzutifan dan bij een van beide behandelingen alleen. De combinatie verminderde H4K12-lactylering en verlaagde de niveaus van sleutelgenen voor glycolyse en nierlijnage die met tumorgroei geassocieerd zijn, terwijl normaal weefsel in dierstudies gespaard bleef.
Wat dit betekent voor patiënten en toekomstige therapieën
Dit werk laat zien dat veel clear cell-nierkankers gevangen zitten in een vicieuze cirkel: een VHL-defect drijft suikierhongerig metabolisme aan, dat lactaat produceert; dat lactaat modificeert chromatine chemisch om dezelfde groeigenen en metabolismegenen permanent actief te houden. De studie toont aan dat glucocorticoïden, lang gebruikt vanwege hun ontstekingsremmende effecten, ook kunnen optreden als gerichte epigenetische geneesmiddelen die deze lactaatgevoede lus tot rust brengen en tumoren gevoeliger maken voor HIF-2α-blokkade. Hoewel zorgvuldige klinische tests nodig zullen zijn — vooral omdat glucocorticoïden het immuunsysteem kunnen onderdrukken — wijzen de bevindingen op een praktische, op het mechanisme gebaseerde combinatiestrategie die bestaande gerichte therapieën effectiever zou kunnen maken voor mensen met deze moeilijk te behandelen nierkanker.
Bronvermelding: Zhang, K., He, L., Wang, Y. et al. Glucocorticoids elevate clear cell renal cell carcinoma sensitivity to HIF-2α inhibitors by suppressing H4K12 lactylation. Sig Transduct Target Ther 11, 117 (2026). https://doi.org/10.1038/s41392-026-02622-7
Trefwoorden: clear cell niercelcarcinoom, tumormetabolisme, histonlactylering, glucocorticoïden, HIF-2α-remmer belzutifan