Clear Sky Science · nl
Effectiviteit en immunomodulerend effect van Claudin18.2-specifieke IL-7/XCL1 gewapende CAR-T-cellen bij kanker van het spijsverteringskanaal: preklinische en klinische analyse
Het immuunsysteem tegen spijsverteringskankers keren
Maag- en alvleesklierkanker behoren tot de dodelijkste tumoren, deels omdat ze vaak resistent zijn tegen chirurgie, chemotherapie en bestraling. Deze studie verkent een nieuwe manier om deze kankers te bestrijden door de eigen immuuncellen van het lichaam te versterken zodat ze solide tumoren kunnen binnendringen, daar overleven en versterking kunnen oproepen. Door kankervragende T‑cellen zo te herontwerpen dat ze behulpzame immuursignalen afgeven, beogen de onderzoekers niet alleen tumoren direct aan te vallen maar ook de rest van het immuunsysteem binnen de vijandige omgeving van de kanker wakker te maken.
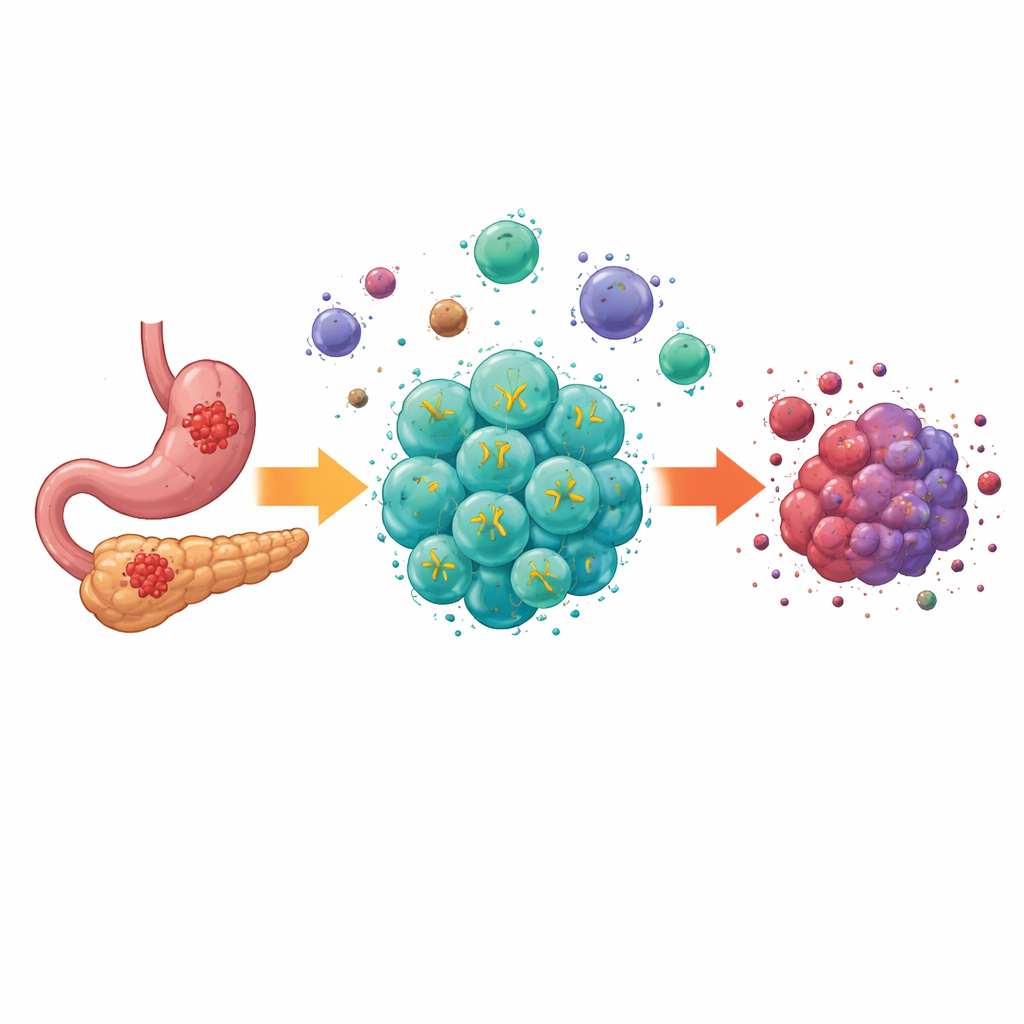
Waarom solide tumoren moeilijk te behandelen zijn
Moderne celtherapieën, CAR-T‑cellen genoemd, hebben spectaculaire resultaten opgeleverd bij bloedkankers en sommige patiënten genezen die geen andere opties meer hadden. Maar solide tumoren zoals die in het spijsverteringskanaal vormen extra obstakels. Hun cellen variëren van plaats tot plaats, het tumorerium is uitgeput van voedingsstoffen en zuurstof, en een mix van onderdrukkende cellen en signalerende moleculen dempt immuunaanvallen. Vroege generaties CAR-T‑cellen konden wel doelmoleculen op spijsverteringskankercellen herkennen, maar faalden vaak in expansie, persistentie en functie binnen deze harde omgeving, wat hun effect in de praktijk beperkte.
Een slimmer ontwerp voor gemodificeerde T‑cellen
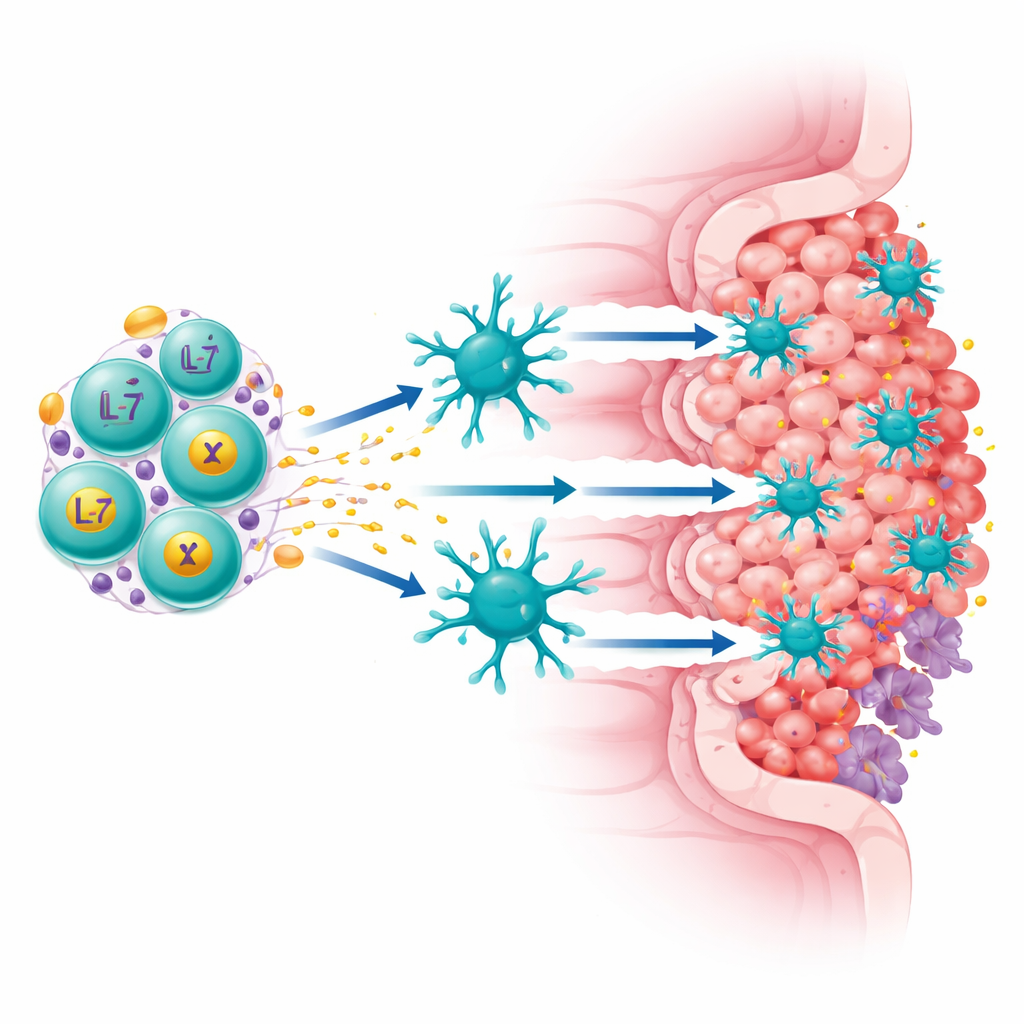
Het team richtte zich op een eiwit genaamd Claudin18.2, dat op veel maag- en alvleesklierkankercellen sterk tot expressie komt maar grotendeels afwezig is in normaal weefsel. Ze ontwikkelden een “vierde-generatie” CAR-T‑cel die twee taken tegelijk uitvoert: ze herkent Claudin18.2 op tumorcellen en scheidt continu twee immuunstimulerende factoren uit, IL‑7 en XCL1. IL‑7 helpt T‑cellen te overleven en een langlevende, stamachtige toestand te behouden, terwijl XCL1 fungeert als een baken om een zeldzaam maar krachtig type immuuncel aan te trekken, de cDC1, die bijzonder goed is in het activeren van cytotoxische T‑cellen. Deze verbeterde cellen, ExCAR-T of RD07 genoemd, zijn ontworpen om niet alleen te doden wat ze zien, maar ook het immuunlandschap van de tumor te hervormen.
Krachtige tumorgroeicontrole in preklinische modellen
In muismodellen van spijsverteringskankers presteerden ExCAR-T‑cellen beter dan conventionele CAR-T‑cellen die geen IL‑7 en XCL1 bevatten. In petrischaaltjes doodden de gemodificeerde cellen meer kankercellen en bevatten ze meer langlevende, geheugenachtige T‑cellen. In dieren met Claudin18.2‑positieve tumoren veroorzaakte ExCAR-T‑behandeling diepere tumorregressie en verlengde overleving vergeleken met standaard CAR-T. De verbeterde cellen breidden zich beter uit in het bloed en veroorzaakten bredere immuunactiviteit, inclusief signalen die extra immuuncellen rekruteren en factoren verminderen die aan tumorspreiding gelinkt zijn. Opvallend was dat muizen die met ExCAR-T waren genezen een tweede uitdaging met kankercellen zonder Claudin18.2‑doel afwezen, wat erop wijst dat de therapie duurzame, tumorbrede immuunherinnering opwekte in plaats van een smalle, eenmalige doelaanpak.
Vroege klinische proefresultaten bij patiënten
Gesterkt door deze gegevens startten de onderzoekers een eerste‑in‑mens onderzoek met RD07 bij 12 personen met gevorderde maag-, gastro‑oesofageale overgangs‑ of alvleesklierkanker die al gefaald hadden in standaardbehandelingen. Bijwerkingen waren over het algemeen beheersbaar: de meeste ernstige problemen waren dalingen in bloedcellen door de voorinfusie chemotherapie, en slechts milde cytokine‑afgifte reacties werden gezien; er traden geen ernstige hersengerelateerde toxiciteiten op. Van de 10 beoordeelbare patiënten lieten er 7 meetbare tumorkrimping zien en 2 behaalden partiële responsen. Patiënten waarvan de tumoren matig tot hoog Claudin18.2‑niveau toonden, deden het bijzonder goed: elke patiënt in die groep behaalde ten minste ziekte‑stabilisatie en sommigen leefden vele maanden langer dan verwacht. Bij deze responders breidden de gemodificeerde T‑cellen zich sterker uit in het bloed en stegen de bloedspiegels van IL‑7 en XCL1, overeenkomstig het ontwerp van de therapie.
Inzichten in de immuunbuurt van de tumor
Om te begrijpen hoe RD07 in mensen werkt, onderzocht het team tumormonsters op single‑cell resolutie voor en na behandeling. Ze zagen dat het aandeel Claudin18.2‑positieve kankercellen afnam bij reagerende patiënten, wat bevestigt dat de therapie haar beoogde target trof. Tegelijkertijd werd een toename gezien in diverse T‑celklonen, inclusief actieve killers en weefsel‑resident geheugen‑cellen, wat suggereert dat het lichaam een bredere immuunaanval uitvoerde. Gespecialiseerde dendritische cellen toonden tekenen van verhoogde activiteit en sterkere interacties met prolifererende T‑cellen, in lijn met het aantrekken van deze cellen door XCL1. Beeldvorming van een tumorpreparaat van één patiënt toonde na behandeling minder tumor- en onderdrukkende myeloïde cellen, met meer T‑ en B‑cellen en een herorganisering van het weefsel in immuunrijke zones — kenmerken van een ‘heetere’, sterker ontstoken micro‑omgeving.
Wat dit kan betekenen voor toekomstige kankerzorg
Samengevat suggereren de preklinische en vroege klinische bevindingen dat RD07 meer doet dan simpelweg een nieuw gerichte geneesmiddeloptie toevoegen. Door tumorerkenning te combineren met ingebouwde immuunondersteuning kunnen deze gemodificeerde T‑cellen langer overleven, belangrijke partnercellen rekruteren en het eigen immuunsysteem van de patiënt trainen om kanker onder controle te houden, zelfs wanneer het oorspronkelijke target verloren gaat. Hoewel de studie klein was en werd uitgevoerd bij zwaar voorbehandelde patiënten, zijn de consistente tumorkrimping, acceptabele veiligheid en diepgaande immuunherschikking veelbelovend. Als dit wordt bevestigd in grotere onderzoeken, kan deze benadering een nieuw hoofdstuk openen in de behandeling van kankers van het spijsverteringskanaal, waarbij het versterken van het immuune‑ecosysteem in de tumor even belangrijk wordt als de initiële klap tegen kankercellen zelf.
Bronvermelding: Zhao, X., Liu, J., Zhang, Z. et al. Efficacy and immunomodulatory effect of Claudin18.2-specific IL-7/XCL1 armored CAR-T cells in digestive tract cancer: preclinical and clinical analysis. Sig Transduct Target Ther 11, 87 (2026). https://doi.org/10.1038/s41392-026-02621-8
Trefwoorden: CAR-T-celtherapie, kanker van het spijsverteringskanaal, tumormicro-omgeving, Claudin18.2, immunotherapie