Clear Sky Science · nl
M6A-gemodificeerde circArhgap26 vermindert ischemie‑reperfusie‑schade aan het hart door remming van plakophiline‑1‑palmitoylatie
Waarom het beschermen van het hart na een hartaanval van belang is
Wanneer iemand een hartaanval krijgt, proberen artsen snel de geblokkeerde slagader te heropenen en de bloedtoevoer te herstellen. Deze reddingsmaatregel redt levens, maar heeft ook een keerzijde: de plotselinge terugkeer van bloed kan het hart verder beschadigen, een probleem dat bekendstaat als ischemie–reperfusie‑letsel. De hier samengevatte studie onderzoekt een onverwachte natuurlijke beschermer in hartcellen — een circulair RNA‑stukje genaamd circArhgap26 — dat helpt het hartspierweefsel te beschermen tegen deze secundaire schade. Begrijpen hoe dit kleine molecuul werkt kan wijzen op nieuwe behandelingen en bloedtesten voor mensen met hartziekte.
Een verborgen cirkel in het genetische script van het hart
De meesten van ons zien genen als rechte strengen DNA en RNA, maar cellen produceren ook ringvormige RNA‑moleculen, zogenaamde circulaire RNA’s, die ongewoon stabiel zijn en veel cellulaire processen fijnstemmen. De onderzoekers zochten in muizenharten naar circulaire RNA’s die veranderen tijdens hartletsel en concentreerden zich op één, circArhgap26, waarvan de niveaus scherp daalden wanneer de bloedstroom werd onderbroken en vervolgens hersteld. Ze bevestigden dat dit circulaire RNA een gesloten lus vormt, voornamelijk in het cytoplasma voorkomt en niet dient als sjabloon voor eiwitsynthese. In plaats daarvan lijkt het te werken als een regulator die met andere moleculen interageert en zo beïnvloedt of een hartcel na stress overleeft of sterft. 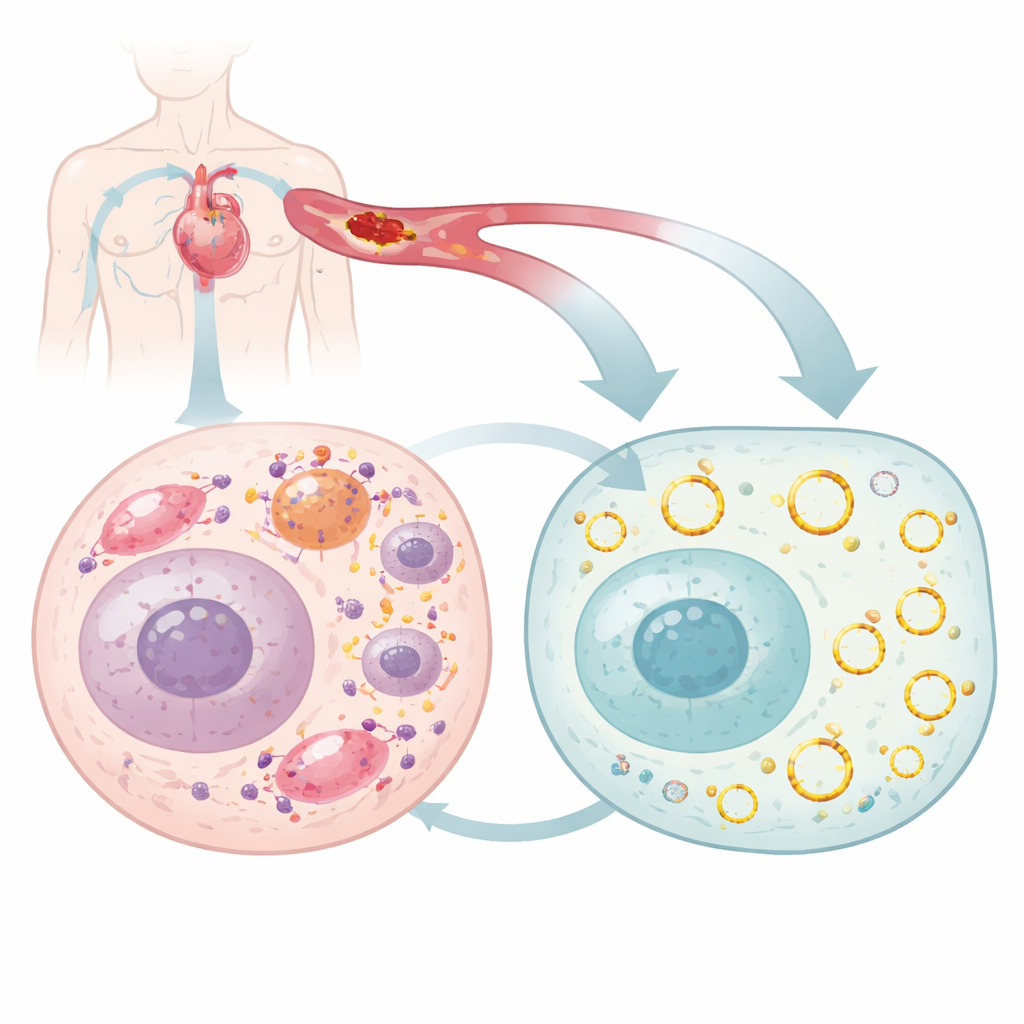
Bewijs dat het circulaire RNA het hart beschermt
Om te zien wat circArhgap26 daadwerkelijk doet, verhoogde of verlaagde het team de niveaus in muizenharten. Wanneer ze een virus gebruikten om circArhgap26 specifiek in hartspiercellen te verhogen, hadden dieren die werden blootgesteld aan een tijdelijke afsluiting van een kransslagader gevolgd door herstel van de bloedstroom een betere hartpompfunctie, kleinere beschadigde gebieden en minder stervende cellen. Klassieke markers van schade in bloed en hartweefsel waren ook lager. Het tegenovergestelde trad op wanneer het circulaire RNA werd stilgelegd: zelfs zonder een geïnduceerde hartaanval verslechterde de hartfunctie en nam celdood toe, en deze problemen werden ernstiger bij toevoeging van ischemie–reperfusie. Vergelijkbare beschermende effecten verschenen in humane hartachtige cellen in het laboratorium, wat suggereert dat het mechanisme tussen muizen en mensen behouden is.
Een schadelijke partner‑eiwit onder controle gehouden
Dieper gravend vroegen de onderzoekers hoe circArhgap26 deze bescherming uitoefent. Met biochemische 'hengel'-technieken ontdekten ze dat het direct bindt aan een structureel eiwit genaamd plakophiline‑1 (PKP1), dat kan beïnvloeden hoe sterk cellen aan elkaar hechten en hoe geneigd ze zijn tot geprogrammeerde celdood. In beschadigde harten en gestreste hartcellen stegen PKP1‑niveaus en werden die gekoppeld aan ernstigere schade. Het stilleggen van PKP1 verlichtte hartletsel en celdood, terwijl geforceerde productie de uitkomst verslechterde. Toen circArhgap26 werd verhoogd, daalde de hoeveelheid PKP1‑eiwit ondanks onveranderde genactiviteit, wat wijst op regulatie na het maken van het RNA‑bericht. Experimenten toonden aan dat circArhgap26 de afbraak van PKP1‑eiwit versnelt door in te grijpen in een vetzuurmodificatieproces dat palmitoylatie heet en dat PKP1 normaal stabiliseert.
Een moleculair touwtrekken om signalen voor celdood
Palmitoylatie wordt uitgevoerd door een familie van enzymen; één in het bijzonder, ZDHHC1, bleek vetgroepen aan PKP1 te hechten en het langer te laten voortbestaan. CircArhgap26 bindt PKP1 op hetzelfde gebied dat ZDHHC1 gebruikt, waardoor een moleculair touwtrekken ontstaat. Wanneer het circulaire RNA wint, krijgt PKP1 minder vetlabels, wordt het minder stabiel en wordt het sneller afgebroken. Dit heeft een kettingreactie tot gevolg: PKP1 stimuleert normaal de aanmaak van een ander eiwit, APAF1, door te interageren met een controlesegment van diens RNA. APAF1 is een sleutelfactor in het apparaat dat de caspase‑9 en caspase‑3 enzymen activeert, centrale uitvoerders van celdood. Met minder stabiel PKP1 daalt de productie van APAF1‑eiwit, wordt de doodssignaleringscascade afgezwakt en overleven hartcellen de stress van herstelde bloedstroom vaker. 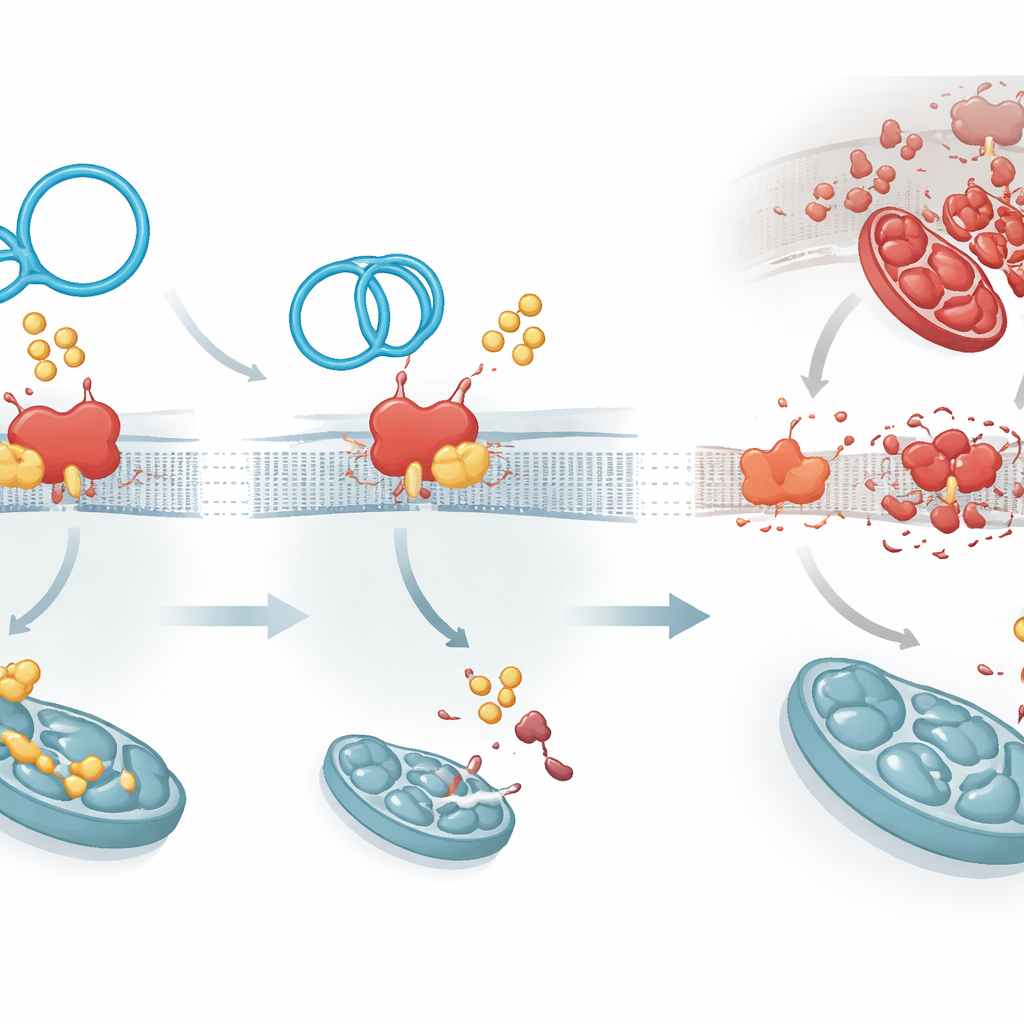
Het fijnafstemmen van de cirkel en de belofte voor patiënten
De studie laat ook zien hoe circArhgap26 zelf omlaag wordt bij letsel. Een veelvoorkomende chemische markering op RNA, m6A genaamd, hoopt zich op op dit circulaire RNA in gestreste harten. Een reader‑eiwit, YTHDF2, herkent deze markering en bevordert de afbraak van circArhgap26, waardoor de natuurlijke hartverdediging wordt verzwakt juist wanneer die het meest nodig is. Belangrijk is dat de menselijke versie van dit circulaire RNA sterk lijkt op die van de muis en duidelijk lager is in het bloed van patiënten die arterie‑heropeningsprocedures ondergaan vergeleken met gezonde vrijwilligers. Gezamenlijk wijzen deze bevindingen erop dat het herstellen of nabootsen van circArhgap26 zowel kan dienen als een bloedgebaseerde risicomarker als een nieuwe therapie. Simpel gezegd onthult het werk een klein circulair molecuul dat fungeert als beschermer tegen reperfusieschade door een dodelijke kettingreactie in hartcellen onschadelijk te maken.
Bronvermelding: Zhang, My., Ji, Dn., Qi, Wy. et al. M6A-modified circArhgap26 attenuates cardiac ischemia‒reperfusion injury by suppressing plakophilin-1 palmitoylation. Sig Transduct Target Ther 11, 99 (2026). https://doi.org/10.1038/s41392-026-02609-4
Trefwoorden: ischemie reperfusie‑letsel, circulair RNA, hartaanval, cardiomyocyt apoptose, RNA‑gebaseerde therapie