Clear Sky Science · nl
Chemo‑fotothermische synergie ontketent antitumorimmuniteit via ferroptose
Het lichaam van warmte en licht tot kankerkrijger maken
Chemotherapie kan tumoren laten krimpen, maar gaat vaak gepaard met sterke bijwerkingen en voorkomt niet altijd dat de kanker terugkeert. Deze studie onderzoekt een nieuwe manier om een bestaand middel, docetaxel, efficiënter en slimmer te laten werken door het in kleine, warmte‑gevoelige deeltjes te verpakken en deze met nabij‑infrarood licht te activeren. Het doel is niet alleen om tumorcellen preciezer te doden, maar ook het immuunsysteem te wekken zodat het kankercellen in het hele lichaam herkent, opspoort en toekomstige terugvallen voorkomt. 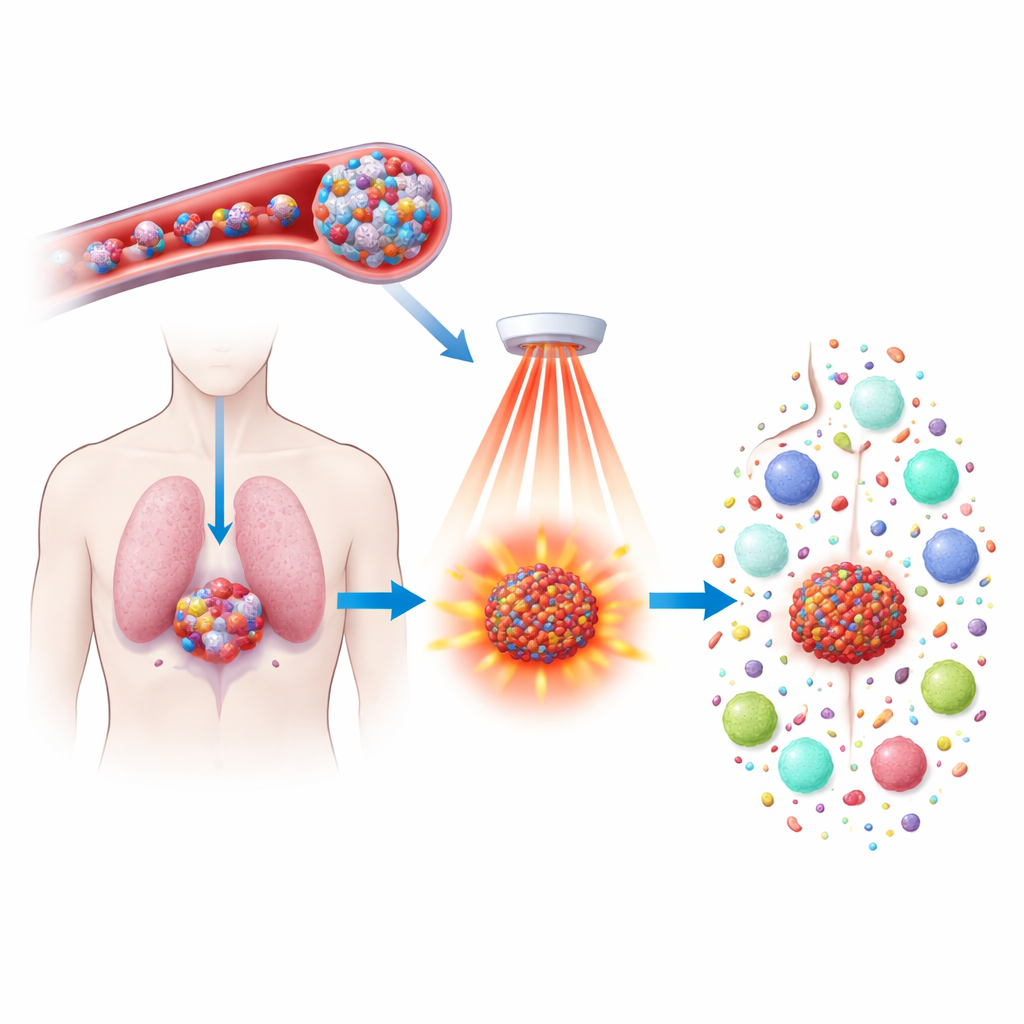
Kleine koeriers die weten waar ze heen moeten
De onderzoekers ontwikkelden een nieuw type nanopartikel uit een polymeer dat ferrocene bevat, een ijzerhoudende molecule die sterk reageert met waterstofperoxide—een oxidant die in hogere concentraties in tumoren voorkomt dan in gezond weefsel. Deze polymeren assembleren zichzelf tot watervriendelijke bolletjes die zowel docetaxel als een lichtabsorberende kleurstof, IR808, kunnen vervoeren. Eenmaal in de bloedbaan zijn de deeltjes klein en stabiel genoeg om te circuleren en in tumoren te lekken, waar de lekke bloedvaten en hoge waterstofperoxidewaarden de deeltjes beginnen te verzwakken en hun lading langzaam vrijgeven. Dit ontwerp concentreert de behandeling in tumoren en beperkt schade aan gezonde organen.
Met licht locale schade versterken
Nabij‑infrarood licht, dat veilig door weefsel kan dringen, wordt vervolgens op het tumorgebied gericht. De IR808 in de nanopartikels absorbeert dit licht en zet het om in warmte, terwijl het ook chemisch reactieve zuurstofsoorten genereert. De combinatie van tumor‑productie van waterstofperoxide en lichtgedreven oxidanten doet de deeltjes sneller uiteenvallen en hun geneesmiddel juist daar vrijgeven waar het nodig is. Tegelijkertijd helpt het ijzer in het ferrocene‑segment deze oxidanten omzetten in bijzonder agressieve vormen die de vetcomponenten van celmembranen aanvallen. Deze gerichte chemische en thermische aanval verhoogt het dodend vermogen aanzienlijk vergeleken met alleen docetaxel of alleen lichtbehandeling. 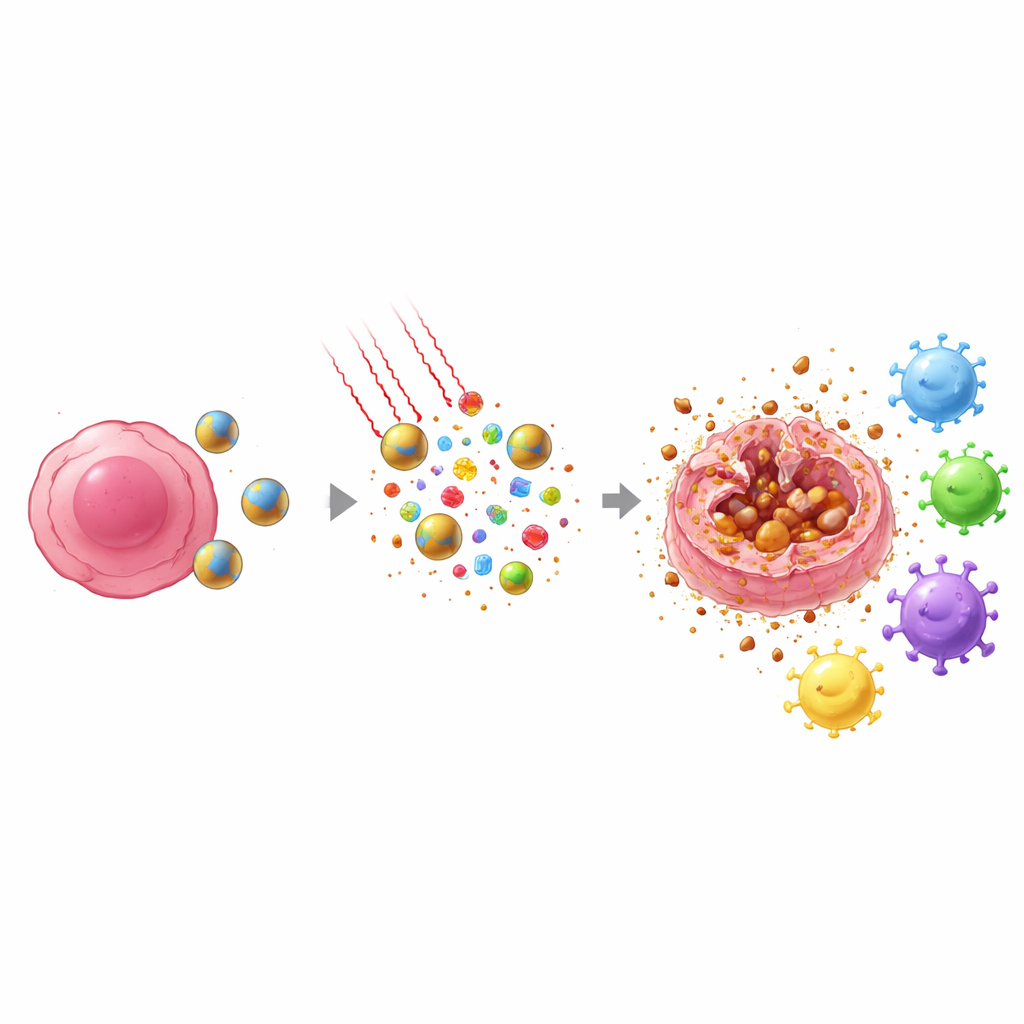
Een gecontroleerde verbranding die het immuunsysteem signaleert
Belangrijk is dat de manier waarop tumorcellen onder deze behandeling sterven verschilt van gewone chemotherapie. In plaats van stilletjes uiteen te vallen in nette fragmenten, ondergaan veel cellen een proces dat ferroptose wordt genoemd, een vorm van door ijzer aangedreven, lipidederende celdood waarbij het buitenste membraan scheurt. Wanneer dat gebeurt, morsen de cellen interne alarmsignalen en tumor‑specifieke fragmenten in hun omgeving. Tegelijkertijd duwt docetaxel een belangrijke kernprotein, HMGB1, naar de rand van de cel, waardoor het klaar is voor vrijgave. Samen creëren warmte, oxidanten en de werking van het geneesmiddel een uitbarsting van gevaar‑ en antigeensignalen die nabijgelegen immuunwachters—dendritische cellen—kunnen detecteren en naar de lymfeklieren vervoeren.
Van lokale aanval naar afweer in het hele lichaam
In muismodellen met tumoren kromp deze gecombineerde chemo‑fotothermale behandeling niet alleen de direct verhitte tumoren effectiever dan een enkel onderdeel, ze veranderde ook het immuunsysteem in de tumoromgeving. Tumoren toonden meer rijpe dendritische cellen en grotere aantallen killer‑T‑cellen, zowel in de tumor zelf als in de afvoerende lymfeklieren. In sommige immuunsysteembekwaamde muizen verdwenen de primaire tumoren na slechts twee behandelingscycli. Toen de wetenschappers later nieuwe tumoren op afstandelijke plaatsen of aan de tegenovergestelde flank implanteren, werden deze secundaire gezwellen vertraagd of onderdrukt, wat aangeeft dat de dieren een vorm van kankerspecifiek immuungeheugen hadden ontwikkeld. Het toevoegen van een checkpointremmend antilichaam dat T‑celuitputting voorkomt verminderde longmetastasen verder en verlengde de overleving, wat suggereert dat deze lokale behandeling kan worden gecombineerd met moderne immunotherapieën.
Waarom dit belangrijk is voor toekomstige kankerzorg
Voor niet‑specialisten is de belangrijkste conclusie dat deze aanpak van docetaxel een grof systeemgif verandert in onderdeel van een slimme, meerstaps anti‑kankerstrategie. Door het geneesmiddel in licht‑geactiveerde, ijzerhoudende nanopartikels te verpakken die reageren op de eigen chemie van de tumor, bezorgt de therapie meer schade binnen tumoren terwijl gezond weefsel wordt gespaard. Het specifieke patroon van celdood dat het veroorzaakt werkt als een vaccin vanuit de tumor zelf en leert het immuunsysteem de kanker te herkennen en te onthouden. Als deze bevindingen op mensen toepasbaar zijn, zouden dergelijke chemo‑fotothermale systemen resistente “koude” tumoren kunnen omzetten in “hete” tumoren die veel beter reageren op immuun‑gebaseerde behandelingen, mogelijk met minder terugkeer en betere lange termijncontrole.
Bronvermelding: Lin, J., Yang, H., Zou, Z. et al. Chemo-photothermal synergy ignites antitumor immunity via ferroptosis. Sig Transduct Target Ther 11, 98 (2026). https://doi.org/10.1038/s41392-026-02608-5
Trefwoorden: kankernanogeneesmiddelen, fotothermale therapie, ferroptose, kankerimmunotherapie, docetaxelafgifte