Clear Sky Science · nl
Geleidend coördinatie-nanozyme-prodrug triggert nauwkeurig pyroptose, cuproptose en ferroptose voor in situ-kankervaccinatie
Tumoren in hun eigen vaccins veranderen
Kankerbehandeling is meestal gericht op het direct doden van tumorcellen, maar wat als een tumor in een vaccin tegen zichzelf kan worden veranderd? Deze studie beschrijft een slimme nanodeeltje-"prodrug" die veilig door het lichaam reist, alleen binnen tumoren wordt geactiveerd en daar kankercellen dwingt te sterven op een manier die het immuunsysteem krachtig alarmeert. Het resultaat is niet alleen krimping van primaire tumoren, maar ook het trainen van het lichaam om naar afgelegen tumoren en uitzaaiingen te zoeken.
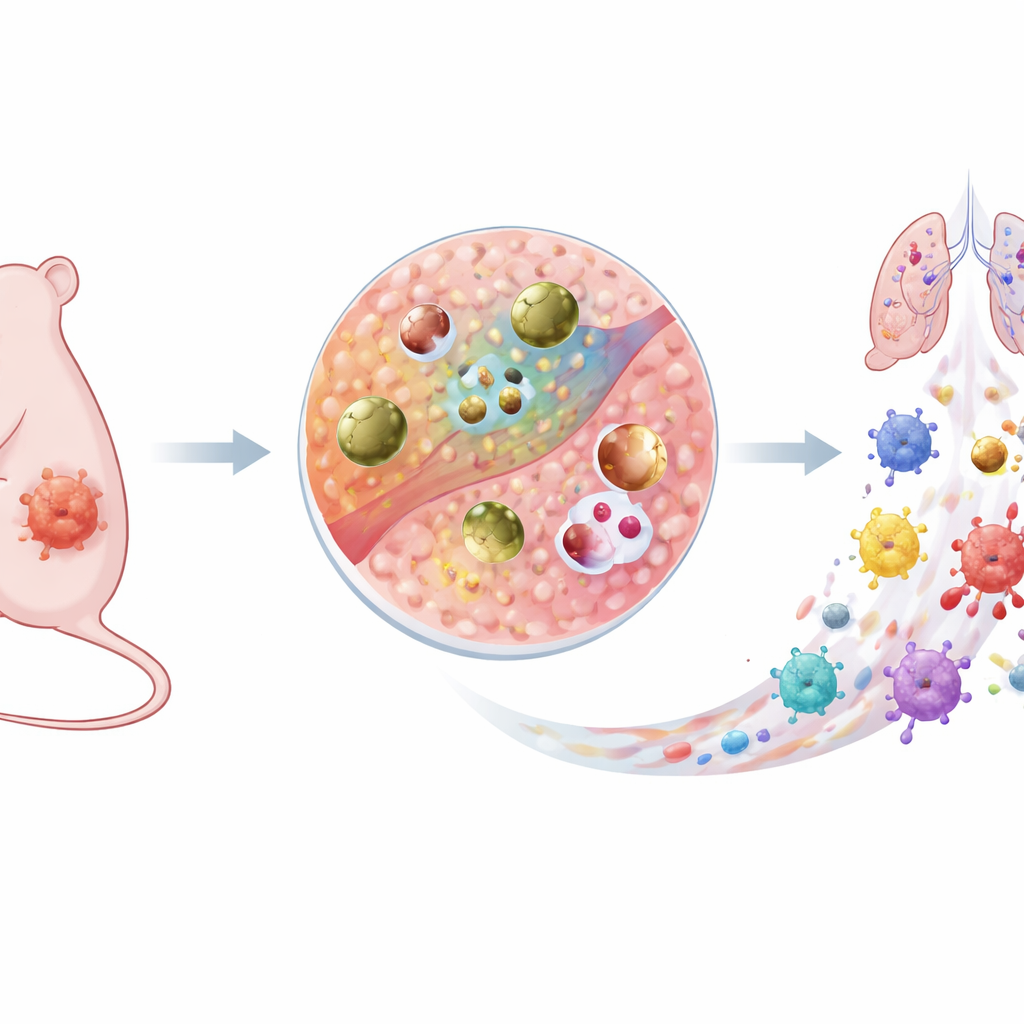
Een nieuw soort slim kankerwapen
De onderzoekers bouwden een klein koperen deeltje genaamd Cu–DHN dat zich tijdens circulatie als een sluimerend medicijn gedraagt en als agressieve kankerbestrijder optreedt zodra het een tumor bereikt. Het is samengesteld uit koperionen, een onschadelijk voorloper-molecuul (1,5-dihydroxynaftaleen, of DHN) en het aminozuur cysteïne. Samen vormen ze een geleidend coördinatienetwerk, wat betekent dat elektronen gemakkelijk door het deeltje kunnen bewegen. Deze interne "elektronensnelweg" laat het hele nanopartikel, niet alleen het oppervlak, deelnemen aan chemische reacties. Cruciaal is dat Cu–DHN is ontworpen om alleen te reageren op de ongebruikelijke chemie van het tumormicro-omgeving, waar antioxidant glutathion en waterstofperoxide beide abnormaal hoog zijn.
Hoe tumorchemie de aan-knop omzet
Binnen tumoren functioneert Cu–DHN als een kunstmatig enzym. In aanwezigheid van zowel glutathion als waterstofperoxide gebruikt het eerst glutathion om zijn koperionen terug te zetten in een zeer reactieve toestand en vervolgens waterstofperoxide om een continue uitbarsting van zeer agressieve oxidanten (hydroxylradicalen) te genereren. Deze oxidanten vervullen een dubbele taak: ze beschadigen cellulaire componenten en zetten het onschadelijke DHN dat in het deeltje opgesloten zit om in juglone, een krachtig anti-kankermolecuul. Juglone onderdrukt op zijn beurt de antioxidatieve verdedigingen van de tumor en verhoogt verder de waterstofperoxide-spiegel, waardoor een zelfversterkende lus van oxidatieve stress ontstaat die beperkt blijft tot de tumor, omdat alleen tumoren de juiste chemische inputs leveren om de cyclus te starten.
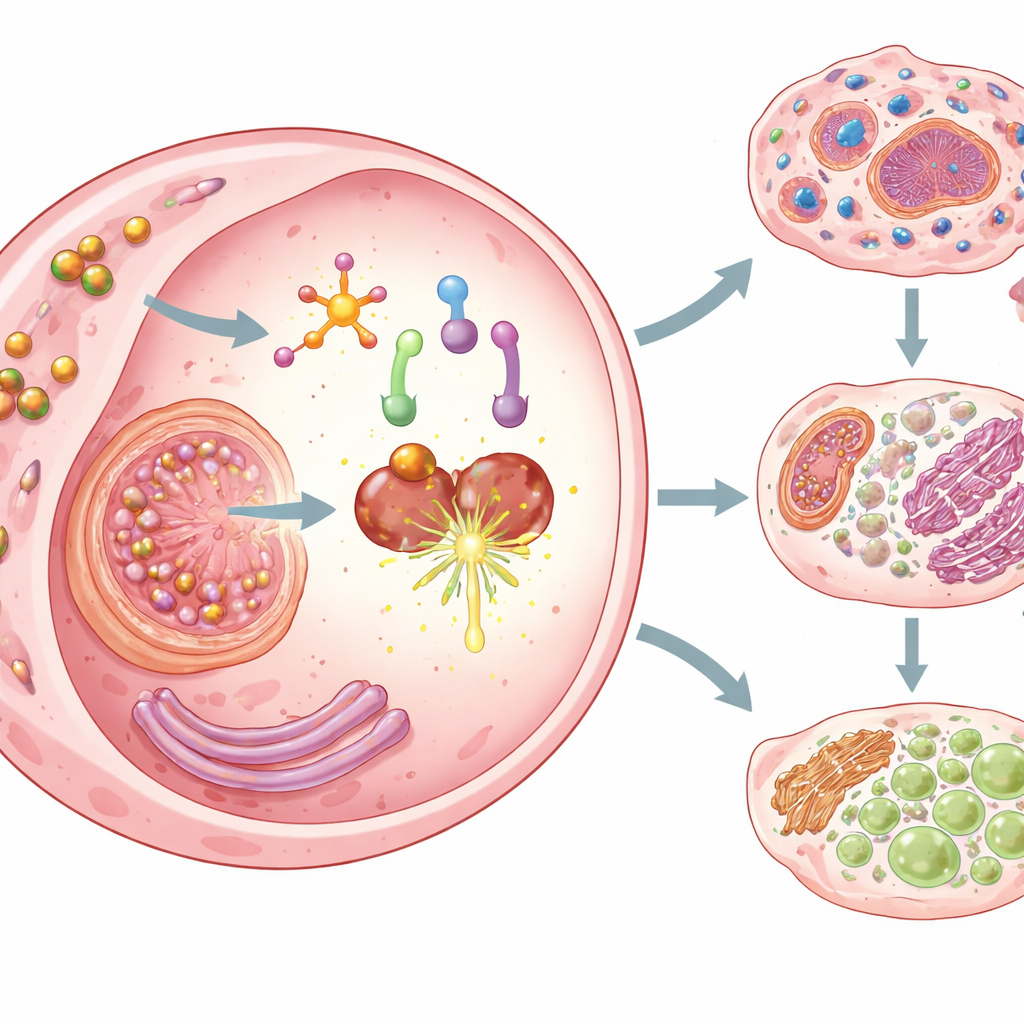
Drie vormen van kankerceldood activeren
Eens geactiveerd doet Cu–DHN meer dan alleen kankercellen vergiftigen. Het veroorzaakt drie gereguleerde vormen van celdood die bijzonder zichtbaar zijn voor het immuunsysteem. Ten eerste keert juglone epigenetische stilte van een porievormend eiwit genaamd gasdermine D om en activeert een inflammatoir sensorscomplex, waardoor cellen pyroptose ondergaan—een dramatische, blaarachtige vorm van dood die het membraan doet barsten en inwendige inhoud doet lekken. Ten tweede veroorzaakt het koper dat door de nanodeeltjes wordt geleverd, en efficiënt door kankercellen wordt opgenomen, cuproptose, een doodsmechanisme gerelateerd aan toxische ophoping van koper in essentiële metabole machinerie. Ten derde bevordert Cu–DHN door uitputting van glutathion en het uitschakelen van een beschermend enzym (GPX4) ferroptose, een door lipidenperoxidatie gedreven celdood. Samen zorgen deze modes ervoor dat kankercellen niet alleen efficiënt worden gedood, maar op een bijzonder immunogeen manier sterven.
Van lokale aanval naar verdediging in het hele lichaam
Pyroptose en de bijbehorende oxidatieve schade zorgen ervoor dat tumorcellen een vloed van alarmtekens vrijgeven: tumorgeassocieerde antigenen, gevarensignalen zoals ATP en HMGB1, en stressmarkers op hun oppervlak. In muismodellen van agressieve borstkanker leidde een enkele injectie van Cu–DHN in primaire tumoren tot sterke activatie van dendritische cellen in nabijgelegen lymfeklieren en een golf van tumorbestrijdende CD8-T-cellen. Deze immuuncellen reisden vervolgens naar onbehandelde tumoren aan de andere kant van het lichaam en naar de longen, waar ze de groei van nieuwe tumoren en metastatische knobbels vertraagden of bijna voorkwamen. Het blokkeren van CD8-T-cellen nam deze bescherming grotendeels weg, wat bevestigt dat Cu–DHN de primaire tumor in een in situ-vaccin verandert dat het immuunsysteem leert kanker elders te herkennen en te vernietigen.
Krachtige effecten met een veiliger profiel
Een belangrijke zorg bij pyroptose-gebaseerde therapieën is het risico normale weefsels te schaden, die dezelfde porievormende eiwitten dragen. Wanneer juglone direct in zijn actieve vorm wordt toegediend, ondervinden muizen aanzienlijke lever-, nier- en bloedtoxiciteit. Daarentegen blijft Cu–DHN inert in gezonde weefsels, omdat deze niet de combinatie van chemische triggers hebben die nodig zijn om het deeltje te activeren. Bij muizen evenaarde Cu–DHN de tumordodende en anti-metastatische kracht van actieve juglone terwijl orgaanschade, bloedafwijkingen en gewichtsverlies werden vermeden. In eenvoudige bewoordingen laat dit werk zien hoe een slim, elektrisch geleidend nanopartikel stil kan blijven in het lichaam, alleen binnen tumoren wakker wordt, kankercellen dwingt immuunstimulerend te sterven en aldus fungeert als een precies, zelfvoorzienend platform voor kankervaccinatie.
Bronvermelding: Wang, Y., Zhao, H., Sun, K. et al. Conductive coordination nanozyme prodrugs precisely trigger pyroptosis, cuproptosis and ferroptosis for in situ cancer vaccination. Sig Transduct Target Ther 11, 96 (2026). https://doi.org/10.1038/s41392-026-02607-6
Trefwoorden: kankerimmunotherapie, nanogeneeskunde, pyroptose, kankervaccins, tumormicro-omgeving