Clear Sky Science · nl
Door de natuur geïnspireerde geconfinieerde cascade-enzymnanoreactoren voor gerichte therapie van atherosclerose
Arteriële verstoppingen bestrijden met slimme kleine helpers
Atherosclerose — verstopte, ontstoken slagaders — is een belangrijke oorzaak van hartaanvallen en beroertes. Veel mensen gebruiken al cholesterolverlagende medicijnen, maar gevaarlijke plaque kan toch blijven ophopen en ontstoken blijven. Deze studie beschrijft een door de natuur geïnspireerde “nanoreactor”, een klein ontworpen deeltje dat de antioxiderende verdediging van het lichaam nabootst om ontstoken plaques te kalmeren, schadelijke moleculen op te ruimen en de veroudering van de bloedvaten in diermodellen te vertragen. 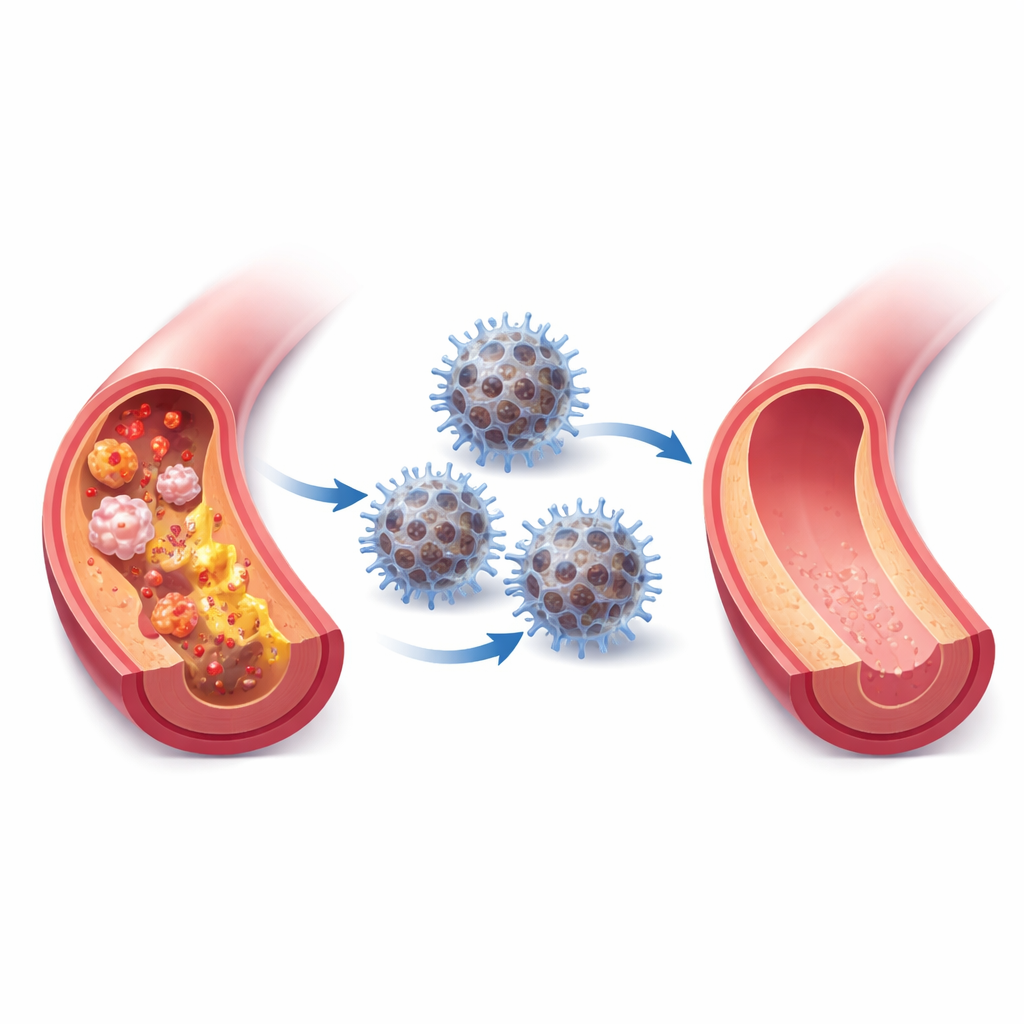
Waarom plaques meer zijn dan alleen vet
Artsen dachten vroeger dat arteriële plaques vooral te maken hadden met cholesterolophoping. We weten nu dat ze ook worden aangedreven door oxiderende stress en chronische ontsteking. In zieke slagaders beschadigen onstabiele moleculen, zogenaamde reactieve zuurstofsoorten, vetten, waardoor normale cholesterol verandert in een schadelijkere vorm die wordt opgenomen door immuuncellen, waardoor “foamcellen” en instabiele plaques ontstaan. Veroudering en gestreste endotheelcellen (de cellen die de vaatwand bekleden) voeren de vlam aan door meer ontstekingssignalen vrij te geven. In gezond weefsel houden natuurlijke enzymen deze reactieve moleculen normaal gesproken onder controle, maar in plaques is die balans verloren, en het enkel toedienen van afzonderlijke antioxidanten heeft bij patiënten niet goed gewerkt.
Strategieën lenen van de enzymfabrieken van de natuur
In levende cellen werken beschermende enzymen die reactieve zuurstofsoorten neutraliseren vaak zij aan zij in dicht opeengepakte teams, waarbij schadelijke tussenvormen snel van het ene naar het andere enzym worden doorgegeven in een cascade. De onderzoekers wilden deze strategie nabootsen met kunstmatige materialen. Ze bouwden een “geconfinieerde cascade” nanoreactor door ultrasmalle Pruisisch blauw-deeltjes — die zich gedragen als meerdere antioxiderende enzymen — in te pakken binnen een dendritische, sponsachtige silica bol die is gedopeerd met selenium, een sleutelcomponent van een ander natuurlijk antioxiderend enzym. Deze poreuze structuur concentreert zowel de katalysatoren als hun doelwitten, waardoor stapsgewijze ontgifting van reactieve zuurstofsoorten efficiënter verloopt dan wanneer elk component los in de bloedbaan zou rondzweven. 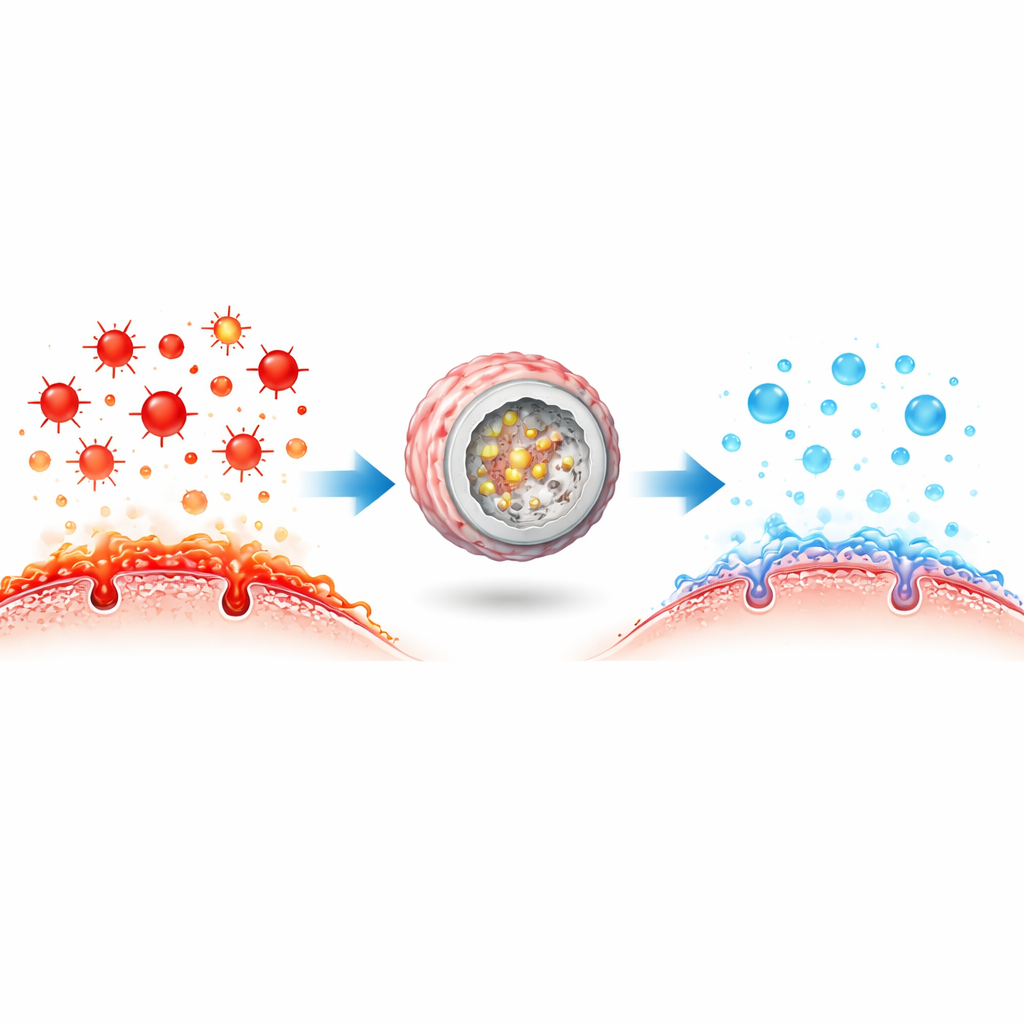
Nanoreactoren een neutrofiel‑vermomming geven
Een medicijn op de juiste plek krijgen is een grote uitdaging. Het team omhulde hun nanoreactoren met membranen afkomstig van neutrofielen, een type witte bloedcel dat van nature naar ontstoken plekken wordt aangetrokken. Deze camouflage helpt de deeltjes langer circuleren, voorkomt snelle verwijdering en leidt ze naar plaques, waar zieke vaatcellen en immuuncellen bijpassende hechtingsmarkers tonen. In celexperimenten werden deze gecoate nanoreactoren makkelijker opgenomen door ontstoken endotheelcellen en macrofagen dan niet‑gemonteerde controles, wat aantoont dat de biologische “schil” actief richting de probleemgebieden stuurt.
Ontsteking, foamcellen en cellulaire veroudering kalmeren
In petrischaalstudies konden de nanoreactoren meerdere enzymfuncties tegelijk nabootsen, verschillende typen reactieve zuurstofsoorten afbreken en onschadelijke producten genereren. Wanneer ze werden toegevoegd aan ontstoken immuuncellen en endotheelcellen, verlaagden ze sterk de oxiderende stress, verminderden ze de afgifte van belangrijke ontstekingsboodschappers en duwden ze macrofagen van een schadebevorderende naar een herstellende toestand. Ze verminderten ook de vetophoping in macrofagen, waardoor de vorming van foamcellen werd beperkt, en beschermden endotheelcellen tegen DNA‑schade en verouderingsmarkeringen. Deze effecten waren sterker dan die van de afzonderlijke componenten alleen, wat het belang van het geconfinieerde, meerstapsontwerp onderstreept.
Slagaders beschermen in een muismodel
Het team testte vervolgens de neutrofiel‑gelaagde nanoreactoren in muizen die genetisch vatbaar zijn voor atherosclerose en een vetrijk dieet kregen. De deeltjes circuleerden urenlang in het bloed, stapelden zich op in plaques en lieten beperkte ophoping in gezonde organen zien. Na meerdere weken behandeling hadden muizen die de volledige nanoreactor kregen kleinere plaque‑gebieden, minder ontstekingscellen, meer stabiliserend collageen en lagere niveaus van enzymen die samenhangen met plaque‑ruptuur vergeleken met controles of dieren die eenvoudigere formuleringen kregen. Weefselkleuring toonde gereduceerde oxiderende stress en minder verouderde cellen in de vaatwand, allemaal zonder duidelijke tekenen van toxiciteit of gewichtsverlies.
Wat dit kan betekenen voor toekomstige hartbehandelingen
Voor een leek suggereert dit werk een nieuwe manier om vaatziekte aan te pakken: in plaats van alleen cholesterol te verlagen of een enkele ontstekingstrigger te blokkeren, gebruiken deze kleine, door de natuur geïnspireerde machines om schadelijke moleculen stilletjes op te ruimen, ontsteking te koelen en cellulaire veroudering direct in plaques te vertragen. Hoewel nog ver verwijderd van gebruik bij mensen, laten deze geconfinieerde cascade‑nanoreactoren zien dat het combineren van slimme materialen met biologische camouflage een krachtige, meer gerichte benadering kan bieden om verstopte slagaders te stabiliseren en mogelijk op termijn het risico op hartaanvallen en beroertes te verminderen.
Bronvermelding: Wu, Y., Xia, H., Ding, H. et al. Nature-inspired confined cascade enzyme nanoreactors for targeted atherosclerosis therapy. Sig Transduct Target Ther 11, 84 (2026). https://doi.org/10.1038/s41392-026-02598-4
Trefwoorden: atherosclerose, nanomedicine, oxiderende stress, ontsteking, nanozyme