Clear Sky Science · nl
DUSP6-verwijdering herstelt CAR T-celconditie die door tumorverlies van CD58 verslechterde via versterking van AP-1-signaal
Waarom het versterken van kankergenezende cellen ertoe doet
Gecodeerde immuuncellen, bekend als CAR T-cellen, hebben de behandeling van bepaalde bloedkankers veranderd, maar veel patiënten krijgen toch een terugval omdat hun tumoren leren te ontkomen aan de aanval. Deze studie onthult een verborgen kwetsbaarheid in sommige tumoren die CAR T-cellen van binnenuit stilletjes uitschakelt—en toont hoe een precieze genetische aanpassing de uithoudingskracht, energievoorziening en dodelijkheid van deze cellen kan herstellen. Voor lezers is het een inkijkje in hoe de volgende generatie celtherapieën duurzamer en effectiever voor meer mensen kan worden.
Een ontbrekende greep aan tumorcellen
CAR T-cellen hebben een stevige handdruk met hun doelwit nodig om goed te werken. Veel tumorcellen dragen een oppervlakte-eiwit genaamd CD58 dat fungeert als een “greep” voor immuuncellen, waardoor ze zich kunnen vastklampen en een nauwe contactzone kunnen vormen. Eerder werk toonde aan dat wanneer kankers CD58 verliezen, CAR T-cellen moeite hebben dat contact te vormen en minder effectief worden. In deze studie stelden de onderzoekers een diepere vraag: voorbij dat mechanische handdrukprobleem, hoe herschikt het verlies van CD58 de interne biologie van CAR T-cellen zodat hun prestaties in de loop van de tijd verzwakken?
Verkorte bedrading binnen CAR T-cellen
Door CAR T-cellen die aan normale tumoren waren blootgesteld te vergelijken met cellen die geconfronteerd werden met CD58-deficiënte tumoren, vonden het team dat een belangrijke controlehub binnen de T-cellen—AP-1 genaamd—selectief verzwakt was, terwijl andere belangrijke signaalroutes grotendeels intact bleven. AP-1 is een groep eiwitten die genen inschakelen die betrokken zijn bij activatie en overleving. Wanneer de AP-1-activiteit inzakte, toonden CAR T-cellen kenmerkende tekenen van een interne energiecrisis: minder en kleinere mitochondriën (hun energiecentrales), een verminderde capaciteit om zuurstof te verbruiken en suiker te benutten, en verlies van het elektrische spanningsverschil over mitochondriale membranen. Tegelijk bouwden schadelijke reactieve zuurstofmoleculen zich op. Gezamenlijk duwden deze veranderingen CAR T-cellen naar een zelfvernietigingsprogramma gebaseerd op schade binnen hun eigen mitochondriën, zelfs zonder externe doodssignalen.
Een interne rem uitschakelen
Om te begrijpen waarom AP-1 zo gedempt was, zochten de onderzoekers stroomopwaarts naar moleculaire “remsystemen” die overactief zouden kunnen zijn. Ze ontdekten dat CAR T-cellen die geconfronteerd werden met CD58-negatieve tumoren meerdere fosfatases opvoerden—enzymen die signaalroutes uitschakelen—met name één genaamd DUSP6. Met behulp van farmacologische middelen en vervolgens precieze genbewerking om deze enzymen te blokkeren, ontdekten ze dat het verwijderen van DUSP6 het sterkst de AP-1-activiteit heractiveerde. DUSP6-bewerkte CAR T-cellen expandeerden beter, vormden meer mitochondriën, verbrandden brandstof efficiënter, produceerden meer kanker-dodende moleculen en waren minder vatbaar voor apoptose, vooral wanneer ze herhaaldelijk werden uitgedaagd door CD58-deficiënte tumorcellen.
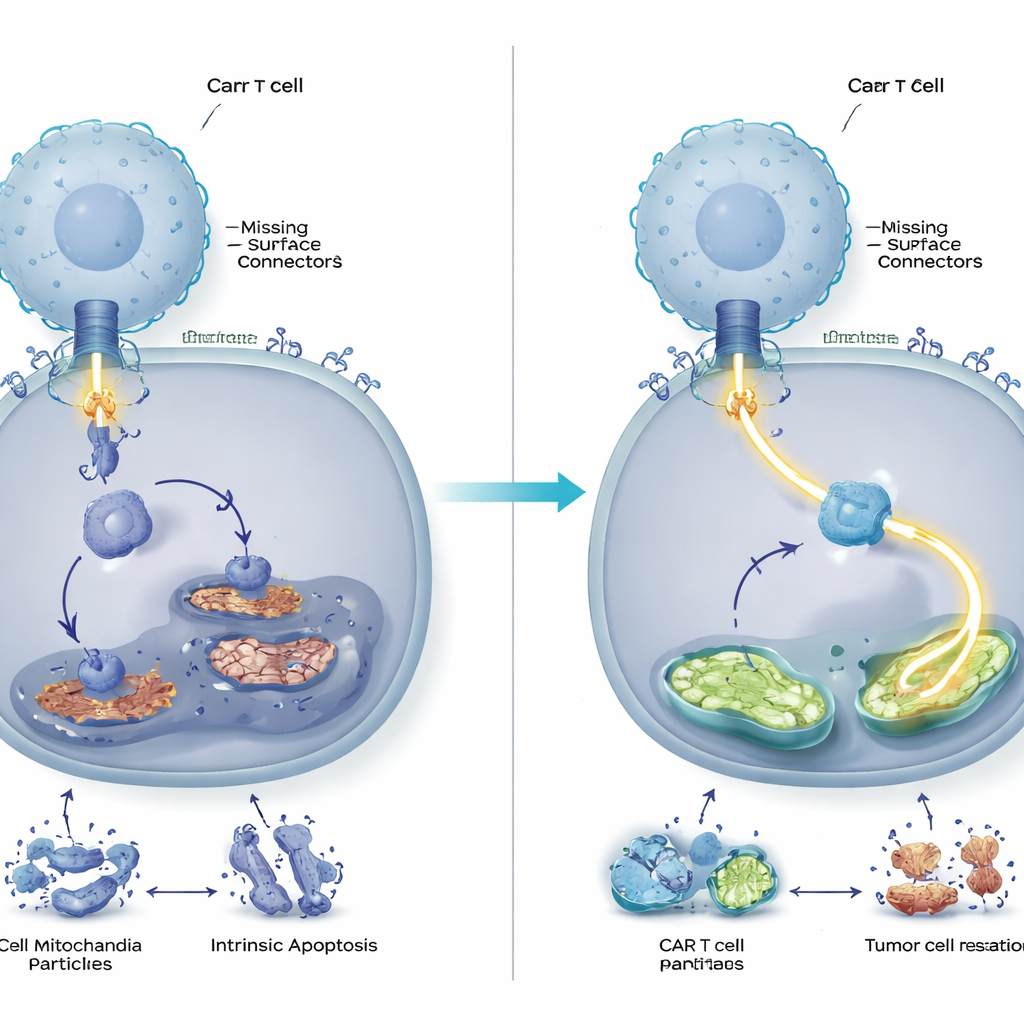
Sterkere, langdurigere tumorgroeicontrole in dieren
Het team testte vervolgens of deze moleculaire afstemming in levende systemen uitmaakte. In muizen met menselijke bloedkankercellen die ofwel CD58 hadden of het misten, wisten DUSP6-deficiënte CAR T-cellen tumoren effectiever te wissen en hielden ze die langer onder controle dan conventionele CAR T-cellen. De gemodificeerde cellen vermenigvuldigden zich robuuster, vertoonden minder uitputtingsmarkers en scheidden hogere niveaus van belangrijke immuurboodschappers af. Opmerkelijk was dat de voordelen van het verwijderen van DUSP6 niet alleen zichtbaar waren wanneer tumoren CD58 misten, maar ook wanneer ze CD58 behielden, wat suggereert dat deze aanpassing CAR T-celtherapieën algemeen kan versterken in plaats van slechts een beperkte oplossing te zijn voor een zeldzaam tumortype.
Hints uit patiëngegevens
Om de relevantie bij mensen te onderzoeken, bekeken de onderzoekers genexpressiegegevens van personen behandeld met CAR T-cellen of met immuunremmende (checkpoint) geneesmiddelen. Bij patiënten met diffuus groot B-cellymfoom die een dubbelgericht CAR T-middel ontvingen, waren lagere DUSP6-niveaus in CD8-T-cellen vóór of kort na infusie geassocieerd met hogere volledige-responscijfers. In een aparte cohort met huidkanker behandeld met anti–PD-1-antistoffen, neigden uitgerookte (exhausted) CD8-T-cellen van non-responders meer DUSP6 tot expressie te brengen dan die van responders. Samen suggereren deze observaties dat DUSP6 fungeert als een negatief merkteken van T-celconditie over verschillende immunotherapieën heen en dat het terugdraaien ervan de uitkomsten zou kunnen verbeteren.
Wat dit betekent voor toekomstige kankertherapieën
Voor een lezer zonder specialistische achtergrond is de kernboodschap dat sommige tumoren aan CAR T-celaanval ontsnappen niet alleen door zich te verbergen voor herkenning, maar door de interne motoren van de cellen te saboteren. Het verliezen van de CD58-“greep” op tumorcellen verlaagt stilletjes het AP-1-signaal in CAR T-cellen, uitgeput de mitochondriën, verhoogt toxische bijproducten en duwt ze richting vroegtijdige celdood. Door de DUSP6-rem te verwijderen, kunnen wetenschappers dit verloren signaal herstellen, de mitochondriale gezondheid repareren en CAR T-cellen meer uithoudingsvermogen en dodelijke kracht geven, zelfs tegen resistente tumoren. Hoewel meer veiligheids- en klinische testen nodig zijn, komt DUSP6-verwijdering naar voren als een veelbelovende engineeringstrategie om levende kankertherapieën krachtiger, duurzamer en mogelijk effectiever voor een breder scala aan patiënten te maken.
Bronvermelding: Ma, X., Zhang, Y., Wang, Y. et al. DUSP6 ablation restores CAR T-cell fitness impaired by tumor CD58 loss through invigoration of AP-1 signaling. Sig Transduct Target Ther 11, 100 (2026). https://doi.org/10.1038/s41392-026-02597-5
Trefwoorden: CAR T-cellen, CD58, DUSP6, kankerimmunotherapie, T-celmetabolisme