Clear Sky Science · nl
Het potentieel ontketenen van bimetaal nanobom-gemedieerde STING-route om bispecifieke T-cel engager te versterken tegen fototherapie-immunotherapie van colorectale kanker
Het immuunsysteem weer tegen darmkanker keren
Darm- en endeldarmkankers zijn veelvoorkomend en vaak dodelijk, deels omdat tumoren leren zich te verbergen voor het immuunsysteem. Deze studie onderzoekt een nieuwe strategie die meerdere kankebestrijdende eigenschappen samenbrengt in één kleine "nanobom" om de afweer van het lichaam te wekken, immuuncellen te helpen de tumor te vinden en te voorkomen dat de kanker terugkomt of uitzaait.
Waarom de huidige immuunmiddelen een upgrade nodig hebben
Een veelbelovende klasse kankertherapieën, bispecifieke T-cel engagers, werkt als biologische koppelaars: het ene uiteinde pakt een T-cel (een belangrijke immuunvechter) en het andere hecht zich aan een marker op een tumorcel, waardoor ze samenkomen zodat de T-cel kan doden. Hoewel krachtig bij bloedkankers, hebben deze middelen moeite met solide tumoren zoals colorectale kanker. Ze worden snel uit het lichaam verwijderd, kunnen gezonde weefsels aanvallen die dezelfde marker delen, en stuiten vaak op "koude" tumoren die niet genoeg immuuncellen bevatten om de behandeling effectief te maken. Artsen en wetenschappers zoeken daarom naar manieren om deze middelen veiliger af te leveren en koude tumoren om te zetten in "hete" tumoren die vol zitten met geactiveerde immuuncellen.
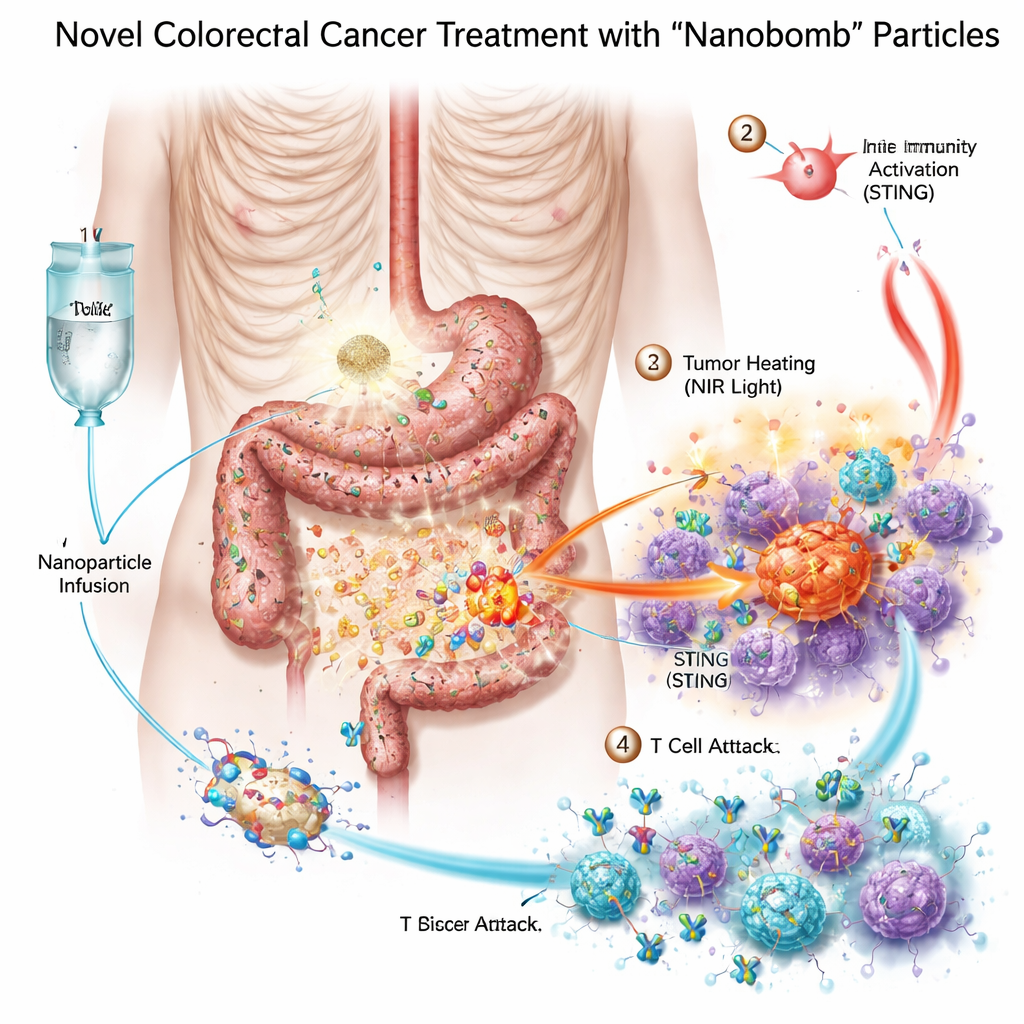
Drie wapens samengepakt in één kleine "nanobom"
De onderzoekers ontwierpen een bimetaal nanobom—wetenschappelijk aangeduid als MnO2/Co‑DA@BiTE/HPT—die drie behandelmodi in één deeltje combineert. Ten eerste bevat de kern mangaan en kobalt, metalen die een cellulair alarmsysteem genaamd de STING-route kunnen activeren, wat het lichaam helpt gevaar te signaleren en immuuncellen te mobiliseren. Ten tweede is het oppervlak van het deeltje bekleed met een bispecifieke T-cel engager die T-cellen met kankercellen verbindt. Ten derde absorbeert het materiaal nabij-infrarood licht, waardoor artsen de tumor van buitenaf kunnen verhitten in een vorm van fotothermische therapie. Om ervoor te zorgen dat de nanobommen zich richten op colorectale kankercellen, voegde het team een kort stukje DNA toe, een aptameer, dat PD‑L1 herkent, een molecuul dat vaak rijkelijk op deze tumoren voorkomt. Zodra deze deeltjes de tumor bereiken, helpen natuurlijke enzymen in het tumortweefsel ze af te breken en hun lading precies daar vrij te geven waar die nodig is.
Verwarmen, alarmeren en het immuunleger rekruteren
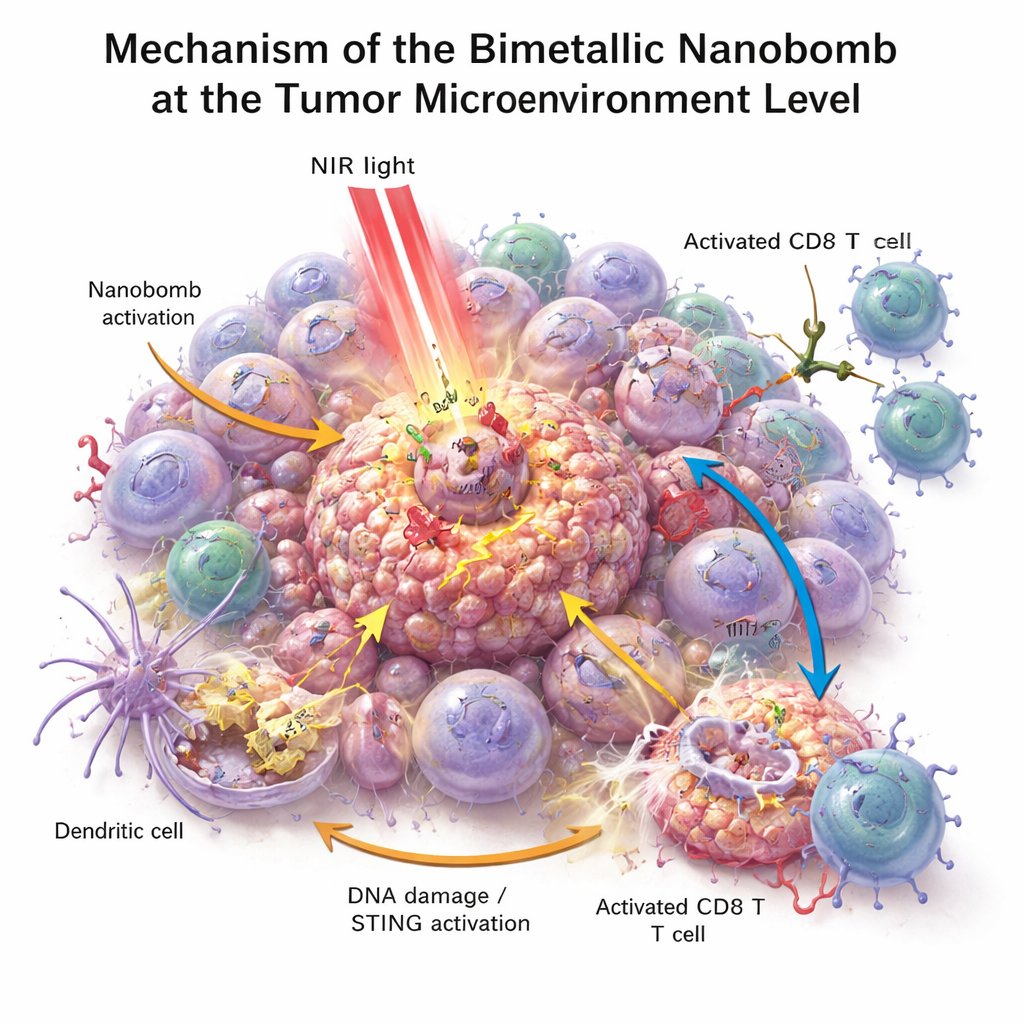
In laboratoriumschalen doodden de nanobommen colorectale kankercellen effectiever dan welk afzonderlijk component dan ook. Bij belichting met nabij-infrarood licht verwarmden de deeltjes, veroorzaakten stress en schade aan de kankercellen en hielpen ze reactieve zuurstofsoorten te genereren—hoogreactieve moleculen die tumorcellen verder beschadigen. Deze stress beschadigde het DNA van de cellen en duwde ze richting een bijzonder zichtbare vorm van celdood die "gevaar"-signalen uitzendt. Nabijgelegen immuuncellen, vooral dendritische cellen, namen het stervende tumormateriaal op en schakelden de STING-route in met behulp van het vrijgekomen mangaan en kobalt. Ze produceerden vervolgens interferonen en andere ontstekingsboodschappers die T-cellen rijpen en aantrekken. Tegelijkertijd verbond de bispecifieke engager op de nanobom T-cellen fysiek met PD‑L1‑positieve tumorcellen, wat de T-celactivering en tumorvernietiging verbeterde, zelfs in eerder koude tumoren.
Van tumorkrimp naar blijvend immuungeheugen
In meerdere muismodellen—waaronder subcutane colorectale tumoren, tumoren aan beide zijden van het lichaam, longmetastasen en een model van recidief na operatie—remden de nanobommen in combinatie met licht de tumorgroei sterk of stopten die bijna helemaal. Behandelde tumoren bevatten veel meer CD8 T-cellen die kanker doden en minder regulerende T-cellen die normaal immuunreacties onderdrukken. Dendritische cellen in de tumoren en in lymfeklieren vertoonden tekenen van rijping en bloedonderzoek toonde verhoogde niveaus van immuunstimulerende cytokinen. Belangrijk is dat muizen die hun tumoren hadden geruimd na nanobombehandeling beter beschermd waren toen de kanker opnieuw werd ingebracht, en ze ontwikkelden minder longmetastasen, wat aantoont dat de therapie hielp bij het opbouwen van langetermijn immuungeheugen in plaats van alleen een eenmalige tumorkrimp te veroorzaken.
Wat dit zou kunnen betekenen voor toekomstige kankerzorg
Dit werk introduceert een "drievoudig treffende" nanogeneesmiddel dat tumoren verwarmt, een intern gevaaralarm activeert en T-cellen direct naar kankercellen leidt, allemaal binnen één gericht deeltje. Bij muizen transformeerde deze benadering niet alleen koude colorectale tumoren tot hete, ontstoken tumoren, maar hielp ook recidief en uitzaaiing te voorkomen. Hoewel de technologie nog ver verwijderd is van klinisch gebruik—opschaling, langetermijnveiligheid en tests in mensen blijven grote uitdagingen—biedt het een blauwdruk voor toekomstige behandelingen die slimme materialen combineren met immuunmedicijnen om patiënten een sterkere, duurzamere antikankerrespons te geven.
Bronvermelding: Mu, M., Li, H., Chen, B. et al. Unleashing the potential of bimetallic nanobomb-mediated STING pathway to enhance bispecific T-cell engager against colorectal cancer photo-immunotherapy. Sig Transduct Target Ther 11, 80 (2026). https://doi.org/10.1038/s41392-026-02596-6
Trefwoorden: colorectale kanker, immunotherapie, nanodeeltjes, STING-route, bispecifieke T-cel engager