Clear Sky Science · nl
Gepersonaliseerde farmacokinetisch–farmacodynamisch geleide therapie via een pluripotente-stamcel-afgeleid multi-organoïde platform bij NF1-gemuteerde borstkanker
Waarom dit onderzoek belangrijk is voor patiënten
Veel mensen met kanker krijgen medicijnen die in sommige patiënten goed werken maar in anderen niet, en die vaak heftige bijwerkingen veroorzaken. Deze studie beschrijft een nieuwe manier om kankerbehandelingen buiten het lichaam te testen met in het laboratorium gekweekte mini-organen die zijn gemaakt van de eigen cellen van een patiënt. Het werk richt zich op een moeilijk te behandelen vorm van borstkanker die wordt aangedreven door wijzigingen in een gen genaamd NF1 en laat zien hoe het combineren van een gen-herstellende aanpak met een gerichte medicatie kan leiden tot veiliger, effectiever en werkelijk gepersonaliseerde therapie.
Een miniatuurversie van het lichaam van de patiënt opbouwen
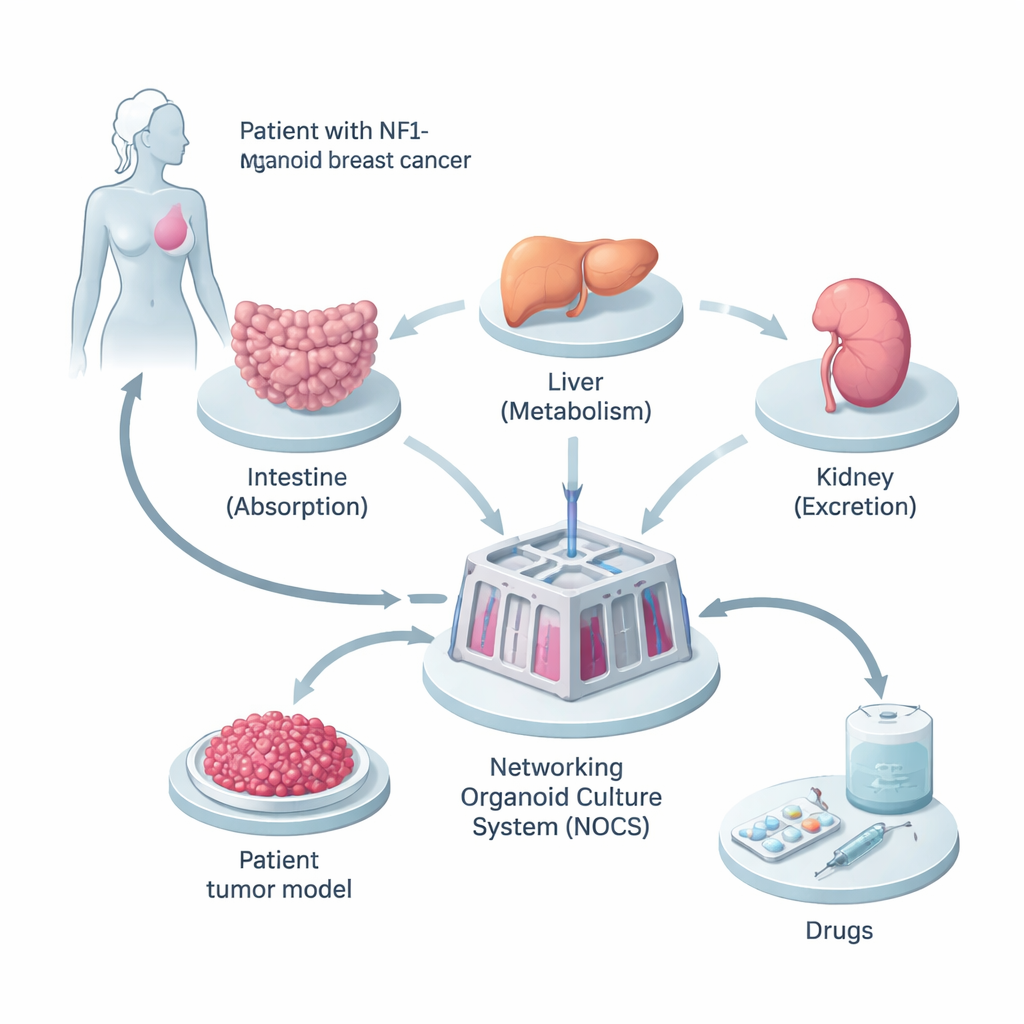
De onderzoekers begonnen met weefsel van een vrouw wiens borstkanker een erfelijke mutatie in het NF1-gen droeg. Ze programmeerden haar normale huidachtige cellen om tot geïnduceerde pluripotente stamcellen, die bijna elk celtype in het lichaam kunnen worden. Hiervan lieten ze drie soorten mini-organen groeien—dunne darm, lever en nier—omdat dit de belangrijkste plaatsen zijn waar geneesmiddelen worden opgenomen, verwerkt en verwijderd. Parallel daaraan maakten ze 3D-tumorspheroïden van haar kankercellen, waarbij de mengeling van celtypen en de genetische veranderingen uit de oorspronkelijke tumor bewaard bleef.
Een levende circuit voor medicijntesten
Om deze mini-organen meer als een echt lichaam te laten functioneren, koppelde het team ze samen in een met vloeistof gevuld apparaat dat het Networking Organoid Culture System (NOCS) wordt genoemd. In deze opstelling stroomt medium tussen de darm-, lever-, nier- en tumorcompartimenten en bootst zo de bloedcirculatie na. Medicijnen kunnen worden toegediend op een manier die lijkt op het innemen van een pil of het krijgen van een injectie, en sensoren en pompen regelen hoe snel het "bloed" beweegt en hoe vaak het wordt ververst. Dit stelde de wetenschappers in staat om bij te houden hoeveel geneesmiddel wordt opgenomen, hoe snel het wordt afgebroken en hoe sterk het op de tumor werkt—alles in een patiëntspecifiek, menselijk model.
Een defect gen herstellen met exon skipping
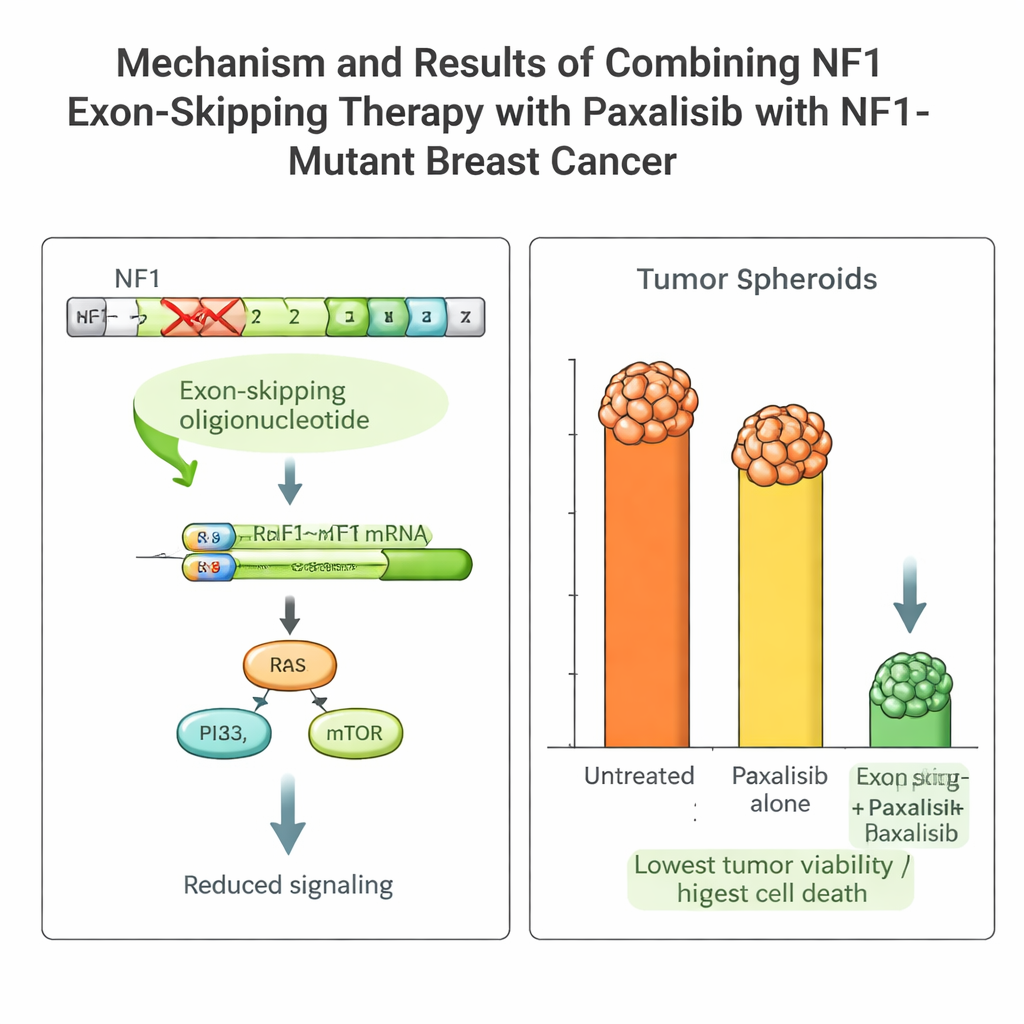
De tumor van de patiënt droeg een schadelijke NF1-mutatie die groeipaden continu aanzet en veel standaardmiddelen minder effectief maakt. Het team ontwierp korte stukjes genetisch materiaal, antisense oligonucleotiden genoemd, om het RNA-verwerkingssysteem van de cel te laten springen over het foutieve stukje (exon 2) van het NF1-gen. Met een viraal afleveringssysteem dat dagenlang actief blijft, veroorzaakten ze stabiele "exon skipping" in de kankercellen van de patiënt. Dit leverde een korter maar functioneel NF1-eiwit op, dempte de overactieve groeisignalen en maakte de tumorcellen gevoeliger voor behandeling.
De juiste gerichte medicatie kiezen met PK/PD-advies
Met dit platform vergeleek het team verschillende geavanceerde middelen die het PI3K–mTOR-pad blokkeren, een route die stroomafwaarts van NF1 ligt. Ze maten farmacokinetiek (hoe het lichaam met het geneesmiddel omgaat) en farmacodynamiek (hoe het geneesmiddel op de tumor werkt) zowel in muizen als in het NOCS. Eén middel, Paxalisib, stak er bovenuit: het werd goed opgenomen in de darm, bleef in het systeem op nuttige concentraties aanwezig en gedroeg zich vergelijkbaar in dieren en in het organoïdeapparaat. In combinatie met NF1-exon skipping nam Paxalisib’s effectiviteit tegen de tumoren van de patiënt dramatisch toe, met sterke verminderingen in groei en duidelijke tekenen van geprogrammeerde celdood, zowel in het NOCS als in muismodellen met de patiëntentumor.
Voor- en nadelen over organen heen afwegen
Omdat de modellen van darm, lever en nier deel uitmaakten van hetzelfde circuit, konden de onderzoekers ook vroegtijdige tekenen van orgaanschade volgen. Paxalisib veroorzaakte stressreacties en subtiele verzwakking van barrières in de darm- en niermodellen en aanwijzingen voor belasting in de lever, maar zonder groot verlies van celviabiliteit bij de geteste dosis. Deze vorm van totaalbeeld, met menselijk weefsel, biedt een manier om behandelingsopties niet alleen te vergelijken op tumorkrimp, maar ook op mogelijke effecten op gezonde organen voordat een geneesmiddel bij een patiënt wordt gebruikt.
Wat dit kan betekenen voor de toekomstige kankerzorg
In eenvoudige bewoordingen laat deze studie zien dat het nu mogelijk is om een vereenvoudigd, patiëntspecifiek "mini-lichaam op een chip" te kweken dat kan testen hoe verschillende medicijnen—en zelfs gen-corrigerende benaderingen—zich gedragen en op elkaar inwerken. Voor deze NF1-gemuteerde borstkankerpatiënt bleek de optimale strategie een combinatie van NF1-exon-skippingtherapie en het orale middel Paxalisib, die samen de tumorontwikkeling veel sterker vertraagden dan elk middel afzonderlijk. Als zulke platforms verder worden ontwikkeld en bij meer patiënten worden getest, zouden ze artsen kunnen helpen bij het kiezen van behandelplannen die zijn afgestemd op iemands genen en biologie, waardoor de kans op succes toeneemt en onnodige toxiciteit vermindert.
Bronvermelding: Lim, J.H., Mun, S.J., Kang, H.M. et al. Personalized pharmacokinetic–pharmacodynamic guided therapy via an induced pluripotent stem cell–derived multi-organoid platform in NF1-mutant breast cancer. Sig Transduct Target Ther 11, 79 (2026). https://doi.org/10.1038/s41392-026-02595-7
Trefwoorden: gepersonaliseerde oncologie, borstkanker, organoïden, NF1-mutatie, gerichte therapie