Clear Sky Science · nl
Benutting van lipiden-gedreven immunometabole routes in omentale metastasen om immunotherapie bij patiënten met eierstokkanker te verbeteren
Waarom het vet rond de buik belangrijk is bij eierstokkanker
Eierstokkanker verspreidt zich vaak naar een vetachtige plooi in de buik die het omentum wordt genoemd. Dit gebied is rijk aan vetcellen en immuuncellen, en het blijkt veel meer te zijn dan een passieve toeschouwer. De hier samengevatte studie laat zien dat de manier waarop immuuncellen vet gebruiken en verwerken in deze omentale afzettingen kan helpen verklaren waarom slechts een klein deel van de patiënten baat heeft bij moderne immunotherapieën. De bevindingen wijzen ook op nieuwe combinaties van geneesmiddelen en op beeldvormingsgebaseerde tests die die behandelingen voor meer mensen effectief zouden kunnen maken.
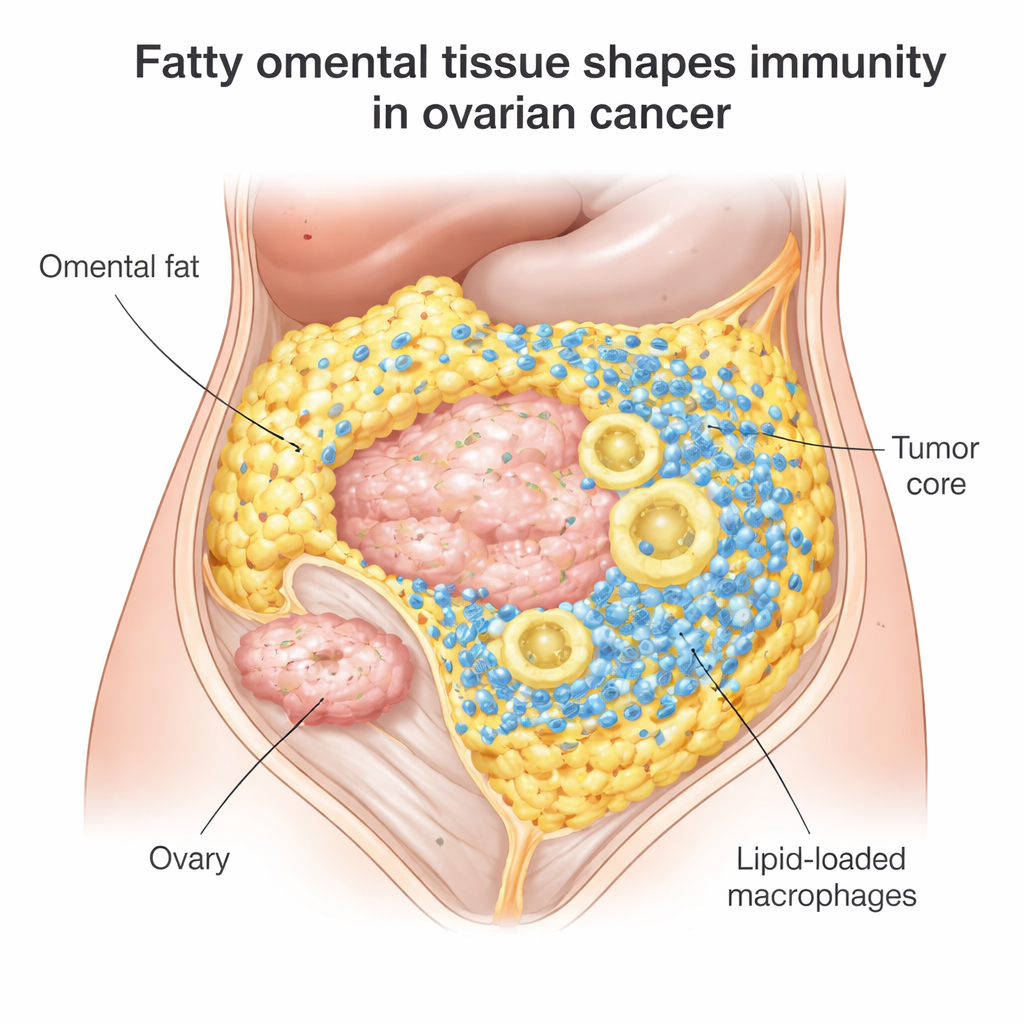
Een verborgen strijdveld in buikvet
De meeste vrouwen met epitheliale eierstokkanker reageren aanvankelijk op chirurgie en chemotherapie, maar bij 70–80% keert de ziekte terug, en immuuncontrolepunten zoals nivolumab of pembrolizumab helpen slechts bij ongeveer 10–15%. De onderzoekers richtten zich op omentale metastasen, een veelvoorkomende plek waar eierstokkanker zich vestigt tussen vetcellen. Bij onderzoek van meer dan 100 tumormonsters vonden ze dat omentale tumoren vol zaten met immuuncellen: cytotoxische T-cellen die kanker kunnen aanvallen en grote opruimcellen die macrofagen worden genoemd. Er was echter een kink in de kabel. Deze T-cellen hadden de neiging zich samen te klonteren bij de grens waar tumor op vet stuit, in plaats van het tumorkerngebied binnen te dringen waar ze het hardst nodig zijn.
Vet dat sommige immuuncellen voedt maar anderen overweldigt
Bij nadere bestudering toonde het team aan dat T-cellen in deze vette tumoren zich aanpassen aan de lokale omgeving door lipiden, oftewel vetten, op te nemen uit nabijgelegen vetcellen. Dit lijkt hen metabolisch “fit” te houden: hun genactiviteit en laboratoriumtests lieten zien dat ze in staat waren de eigen tumorcellen van de patiënt te herkennen en te doden. Tegelijkertijd waren veel tumor-geassocieerde macrofagen in het omentum zwaar geladen met vetdruppels. Deze lipide-gevulde macrofagen vertoonden tekenen van hoge oxidatieve stress—chemische slijtage gekoppeld aan reactieve zuurstofsoorten—en verschooften naar een immuunsuppressieve, tumorondersteunende toestand. Met andere woorden: dezelfde vetrijke omgeving die effectieve T-cellen kan voeden, dwingt macrofagen ook in een schadelijke modus die de algehele immuunaanval verzwakt.
Overgevoede macrofagen herprogrammeren met bestaande geneesmiddelen
De wetenschappers vroegen zich vervolgens af of ze deze gestreste macrofagen weer tot bondgenoten konden maken. Met verse tumorfragmenten die in het laboratorium werden gekweekt, testten ze twee benaderingen. De ene betrof maraviroc, een hiv-medicijn dat CCR5 blokkeert, een receptor voor het immuunsignaal CCL5 dat overvloedig aanwezig is aan de tumor–vetgrens. De andere richtte zich op CD36, een belangrijke “opruimer”-receptor die macrofagen in staat stelt vetzuren op te nemen. Beide behandelingen verminderden de vetbelasting in macrofagen, verlaagden markers van oxidatieve stress en schadelijke lipideperoxidatie, en ontketenden golven van ontstekingssignalen. Cruciaal was dat ze cytotoxische T-cellen lieten vermenigvuldigen en verplaatsen van de vette rand naar het tumorkerngebied, waardoor de lokale immuunactiviteit toenam zonder dat er extra immuuncellen van buitenaf werden toegevoegd.
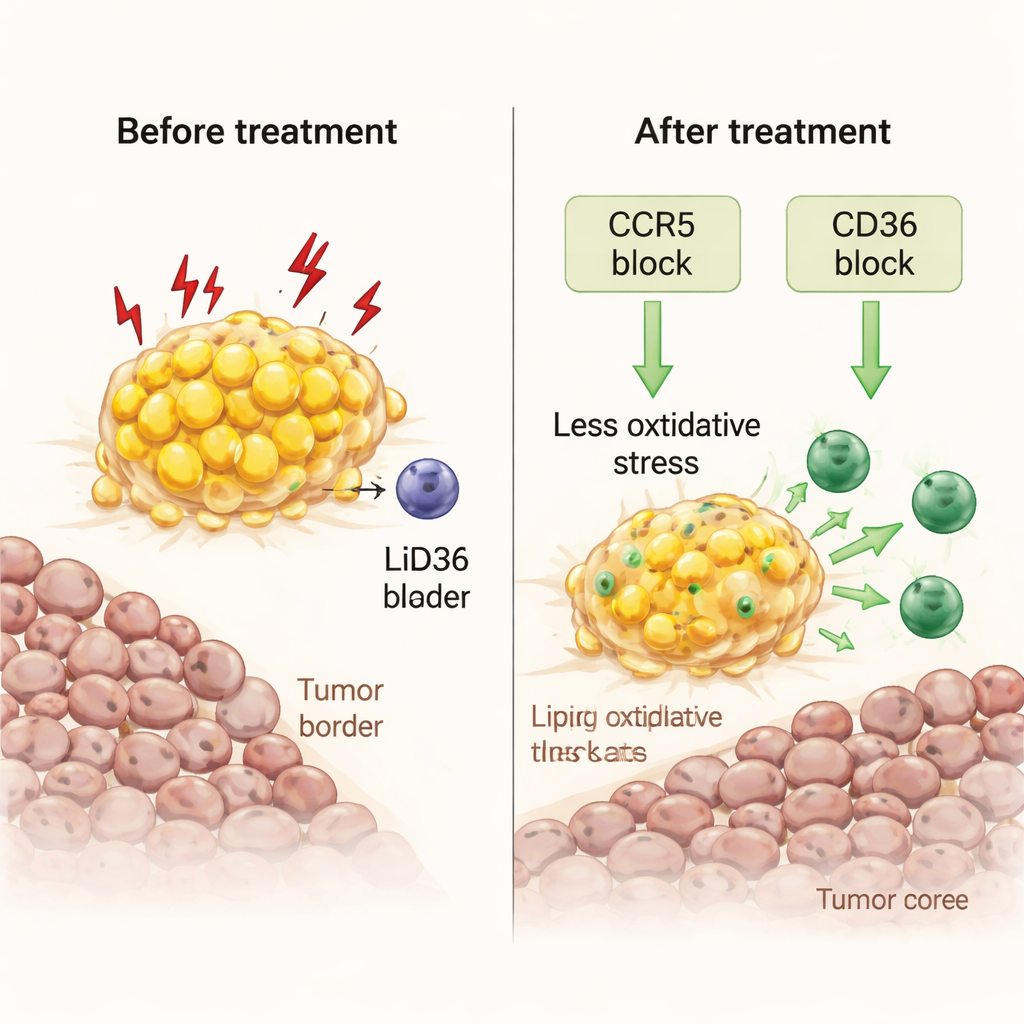
Van celroutes naar realistische modellen en patiënten
Om deze ideeën in een realistischer setting te testen, gebruikte het team gehumaniseerde muizen die een mensachtig immuunsysteem droegen en implanteerden ze humane borstkanker in vetrijke weefsels. Maraviroc-behandeling herprogrammeerde humane macrofagen in deze dieren op manieren die de patiëntafgeleide monsters weerspiegelden: gereduceerde lipide- en stresssignalen, meer cytokineproductie en sterkere ondersteuning van T-celgerelateerde routes. Klinisch heranalyseerden de onderzoekers een Japanse studie met nivolumab voor chemotherapie-resistente eierstokkanker. Iedere patiënt die baat had bij het middel had omentale metastasen zichtbaar in chirurgische monsters. Met CT- of MRI-scans gecombineerd met machine-learninganalyse van de vetverdeling in het lichaam bouwden ze een beslisboom die niet-invasief patiënten kon signaleren waarvan de tumoren waarschijnlijk dicht bij visceraal vet liggen—en in één prospectief geval voorspelde deze methode correct een patiënt die later reageerde op nivolumab.
Wat dit kan betekenen voor toekomstige behandeling
Voor niet-specialisten is de hoofdboodschap dat “waar” eierstokkanker in het lichaam groeit, en hoe nabijgelegen vet immuuncellen hervormt, sterk kan bepalen of immunotherapie werkt. Vetrijke omentale afzettingen lijken krachtige T-cellen te herbergen maar ook overvoede, gestreste macrofagen die de aanval doven. Door de lipidenlast in deze macrofagen te verlichten en hun oxidatieve stress te verminderen—met CCR5-blokkeraars zoals maraviroc, CD36-gerichte middelen of aanverwante strategieën—zou het mogelijk kunnen zijn een gedeeltelijk geblokkeerde immuunrespons om te zetten in een volledige aanval op de tumor. Tegelijkertijd kunnen beeldvormingsgebaseerde maten van omentale betrokkenheid artsen helpen de patiënten te kiezen die het meest waarschijnlijk voordeel hebben van immuuncheckpointmiddelen, wat kan leiden tot een meer gepersonaliseerde en mogelijk effectievere aanpak van de behandeling van eierstokkanker.
Bronvermelding: Suarez-Carmona, M., Hampel, M., Zhang, XW. et al. Harnessing lipid-driven immunometabolic pathways in omental metastases to enhance immunotherapy in patients with ovarian cancer. Sig Transduct Target Ther 11, 78 (2026). https://doi.org/10.1038/s41392-026-02594-8
Trefwoorden: eierstokkanker, omentumvet, immunotherapie, tumor-geassocieerde macrofagen, lipidenmetabolisme