Clear Sky Science · nl
GPR54 reguleert de ontwikkeling van niet-kleincellig longkanker via dopa-decarboxylase
Waarom dit longkankerverhaal ertoe doet
Longkanker blijft een van de dodelijkste vormen van kanker, en de meeste gevallen behoren tot een type dat niet-kleincellig longkanker (NSCLC) heet. Veel patiënten raken uiteindelijk zonder effectieve behandelingsopties omdat tumoren zich aanpassen of resistent worden tegen huidige geneesmiddelen. Deze studie onthult een tot nu toe ondergewaardeerd regelsysteem binnen longkankercellen, gecentreerd rond een receptor genaamd GPR54 en een enzym genaamd dopa-decarboxylase (DDC). Door te begrijpen hoe deze moleculen tumoren helpen groeien en hun brandstof leveren, wijzen onderzoekers op nieuwe manieren om NSCLC te vertragen of zelfs te verkleinen.
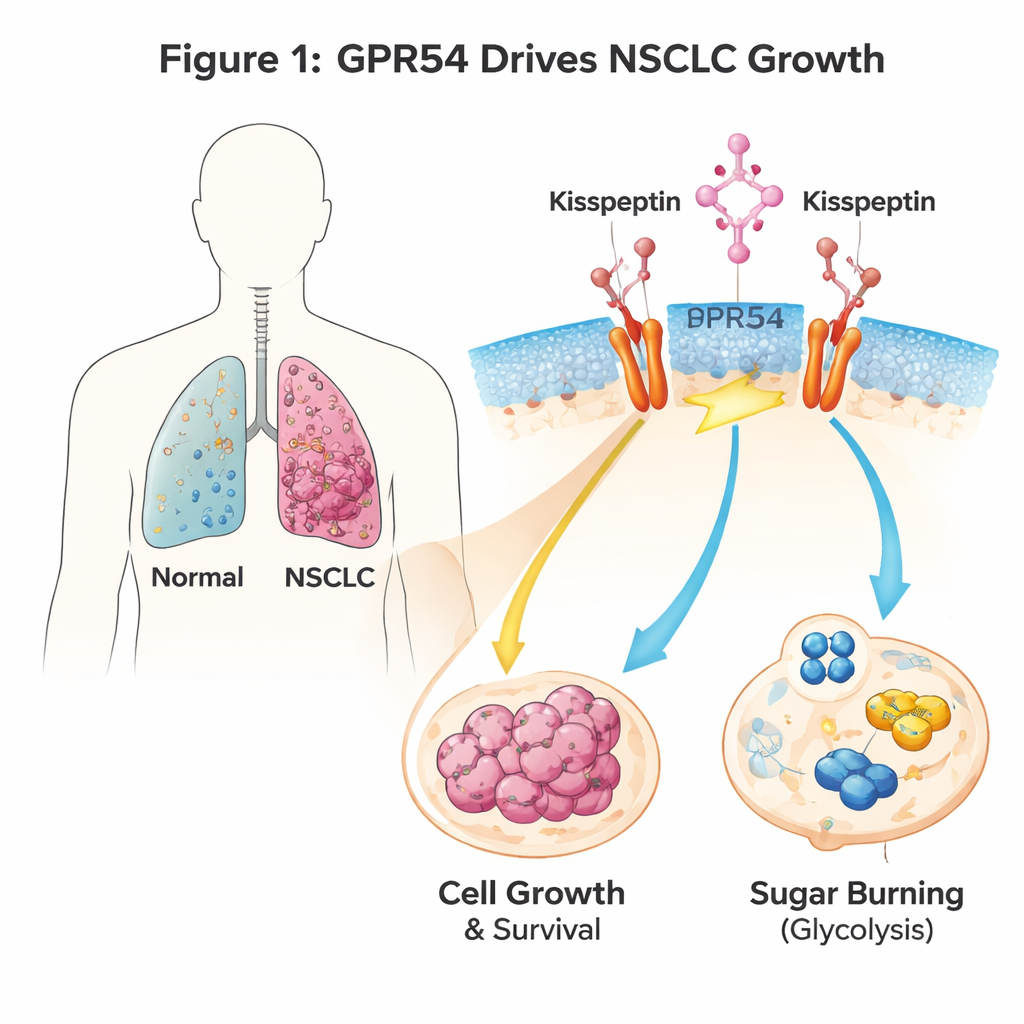
Een signalenschakelaar op longkankercellen
GPR54 is een sensor die aan het celoppervlak zit en reageert op een natuurlijke signaalstof genaamd kisspeptine. Hij is vooral bekend vanwege rollen bij de puberteit en voortplanting, maar komt ook in veel kankers voor. De auteurs gebruikten genetisch gemodificeerde muizen die NSCLC ontwikkelen wanneer een kankerverwekkend gen genaamd Kras in longcellen wordt aangezet. Toen zij het Gpr54-gen in deze muizen verwijderden, leefden de dieren langer, ontwikkelden ze minder en kleinere longtumoren, en lieten hun kankercellen duidelijke tekenen van zelfvernietiging (apoptose) zien. Humane NSCLC-cel lijnen vertelden hetzelfde verhaal: wanneer GPR54-niveaus werden verlaagd, groeiden de tumorcellen langzamer, vormden ze minder kolonies en stierven ze gemakkelijker, ongeacht hun specifieke genetische mutaties.
Hoe GPR54 tumorcellen in leven houdt
Dieper gravend vroegen de onderzoekers welke interne circuits GPR54 gebruikt. Zij vonden dat GPR54 doorgeeft aan twee belangrijke groeipaden binnen de cel, bekend als AKT en ERK. Beiden zijn veelvoorkomende “aansluitpunten” die kankercellen vertellen zich te delen en weerstand te bieden tegen celdood. Wanneer GPR54 werd geblokkeerd of verwijderd, daalde de activiteit van AKT en ERK en werden de cellen gevoeliger voor apoptose. Het herstellen van sterke AKT- of ERK-signalen kon de cellen deels redden, wat bevestigt dat GPR54 NSCLC-cellen helpt overleven door te steunen op deze groeicircuits.
Het herbedraden van hoe kanker suiker gebruikt
Kankercellen herprogrammeren vaak hoe ze voedingsstoffen gebruiken en geven de voorkeur aan snelle suikerafbraak (glycolyse) om groei te ondersteunen. Genexpressieprofilering van muizen tumoren zonder Gpr54 toonde aan dat veel genen die betrokken zijn bij suikerverwerking en energieproductie naar beneden waren bijgesteld. In longkankercellen die met kisspeptine werden behandeld om GPR54 te activeren, lieten metingen van zuurstofgebruik en zuurophoping—proxy’s voor energiemetabolisme—zien dat GPR54 de glycolyse bevordert. Het blokkeren van het GPR54-pad op verschillende stappen (de Gαq/11-schakelaar, PI3K, AKT of mTOR) verminderde glucoseverbruik en lactaatproductie en duwde cellen richting apoptose. In eenvoudige woorden helpt GPR54 NSCLC-cellen suiker sneller en efficiënter te verbranden, waardoor hun snelle groei wordt ondersteund.
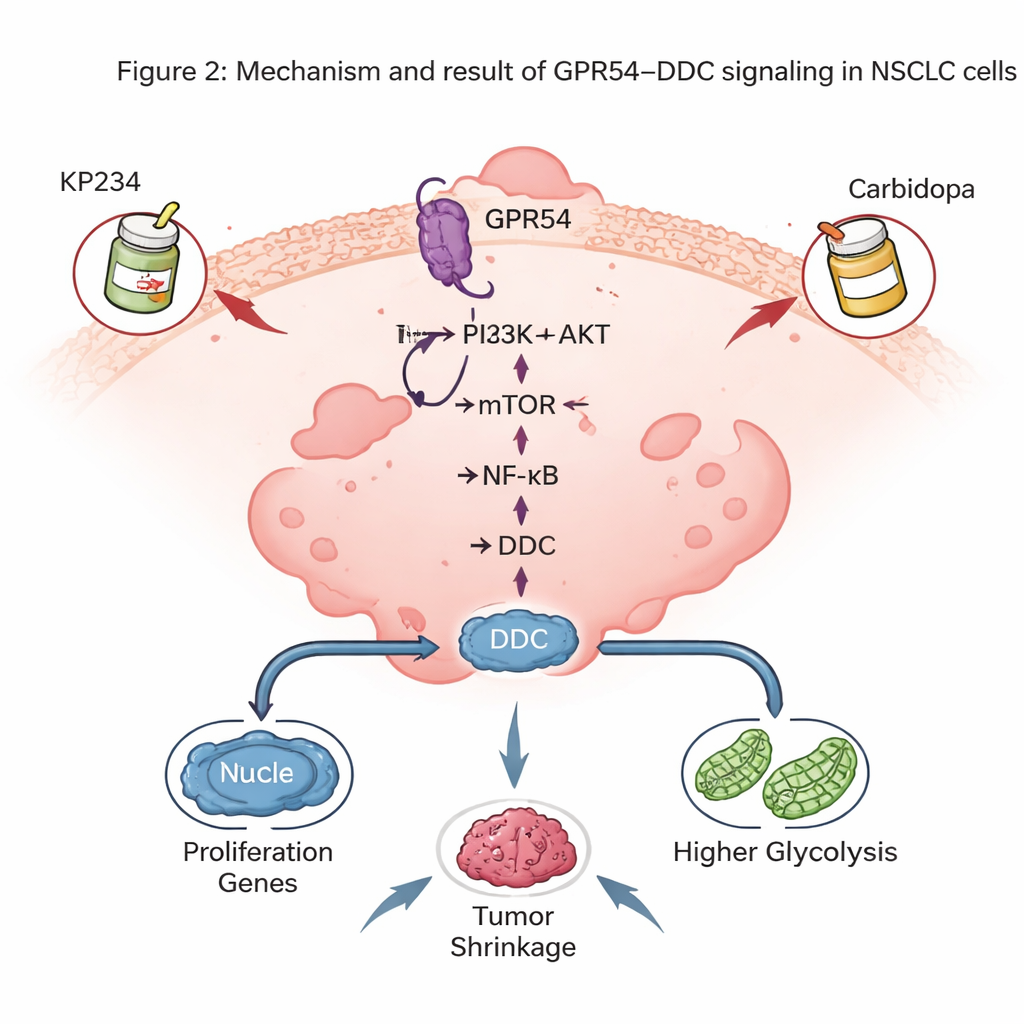
De verrassende rol van een hersengerelateerd enzym
Een van de meest opvallende ontdekkingen was dat GPR54 de niveaus van DDC reguleert, een enzym dat vooral bekend is voor de aanmaak van de hersenchemische stoffen dopamine en serotonine. In muizen tumoren volgden DDC-niveaus nauw de hoeveelheid GPR54: minder GPR54 betekende minder DDC. Humane NSCLC-tumoren en cellijnen toonden ook hogere DDC dan normale longcellen, en patiënten met meer DDC hadden een slechtere overleving. Het terugschakelen van DDC in longkankercellen vertraagde tumor groei in muizen, verminderde celdeling in kweek en veroorzaakte meer apoptose. Op moleculair niveau hielp DDC de activiteit in het NF-κB-pad te behouden, een hoofdregelaar die de overleving van kankercellen en ontsteking bevordert, en ondersteunde het hoge-glycolyse-stadium van tumorcellen.
Het testen van een combinatie-behandelingsstrategie
Aangezien DDC al wordt aangestuurd in de ziekte van Parkinson met een middel genaamd carbidopa, onderzochten de auteurs of het combineren van een GPR54-remmer (KP234) met carbidopa NSCLC van twee kanten kon raken. In celkweek en in muismodellen waarin menselijke NSCLC-cellen in de long werden gekweekt, sneed de dubbele behandeling tumorgroei meer terug dan elk middel afzonderlijk en verhoogde zij de celdood van kankercellen, zonder duidelijke gewichtsafname bij de dieren. Deze combinaties toonden ook veelbelovende resultaten samen met enkele moderne doelgerichte middelen gericht op gemuteerde RAS-genen, wat suggereert dat GPR54–DDC-signaleringsroutes kunnen worden opgeteld bij bestaande precisietherapieën.
Wat dit betekent voor toekomstige longkankerzorg
Voor een leek is de kernboodschap dat NSCLC-cellen vertrouwen op een tot nu toe ondergewaardeerde samenwerking tussen een oppervlakteschakelaar (GPR54) en een metabool enzym (DDC) om in leven te blijven en snel brandstof te verbranden. Het verstoren van deze samenwerking verzwakt tumoren, waardoor ze langzamer groeien en gemakkelijker afsterven in experimentele modellen. Hoewel er veel werk te doen is voordat dergelijke strategieën de kliniek bereiken, plaatst deze studie GPR54 en DDC als potentiële biomarkers om agressieve NSCLC te identificeren en als veelbelovende doelwitten voor nieuwe combinatietherapieën die de uitkomsten kunnen verbeteren voor patiënten van wie de kankers huidige standaardbehandelingen weten te ontlopen.
Bronvermelding: Hwang, HH., Lee, S.Y., Lee, C. et al. GPR54 regulates non-small cell lung cancer development via dopa decarboxylase. Sig Transduct Target Ther 11, 74 (2026). https://doi.org/10.1038/s41392-026-02591-x
Trefwoorden: niet-kleincellig longkanker, GPR54, dopa-decarboxylase, kankermetabolisme, gepaste therapie