Clear Sky Science · nl
Reactieve zuurstofsoorten (ROS) bij kanker: van mechanisme naar therapeutische implicaties
Als nuttige moleculen gevaarlijk worden
In elke cel ontstaan voortdurend kleine chemische vonken, reactieve zuurstofsoorten (ROS), als onderdeel van normaal cellulair leven. In de juiste hoeveelheden helpen ze cellen te groeien, communiceren en zich te verdedigen tegen ziekteverwekkers. Deze review legt echter uit hoe dezelfde moleculen ook DNA kunnen beschadigen, de cellulaire bedrading kunnen ontregelen en kanker kunnen aanzetten tot groei, verspreiding en resistentie tegen behandeling. Inzicht in dit "dubbele leven" van ROS helpt wetenschappers bij het ontwerpen van nieuwe kankertherapieën die óf schadelijke oxidatieve stress dempen, óf die deze stress doelbewust over de rand duwen om tumorcellen te doden.
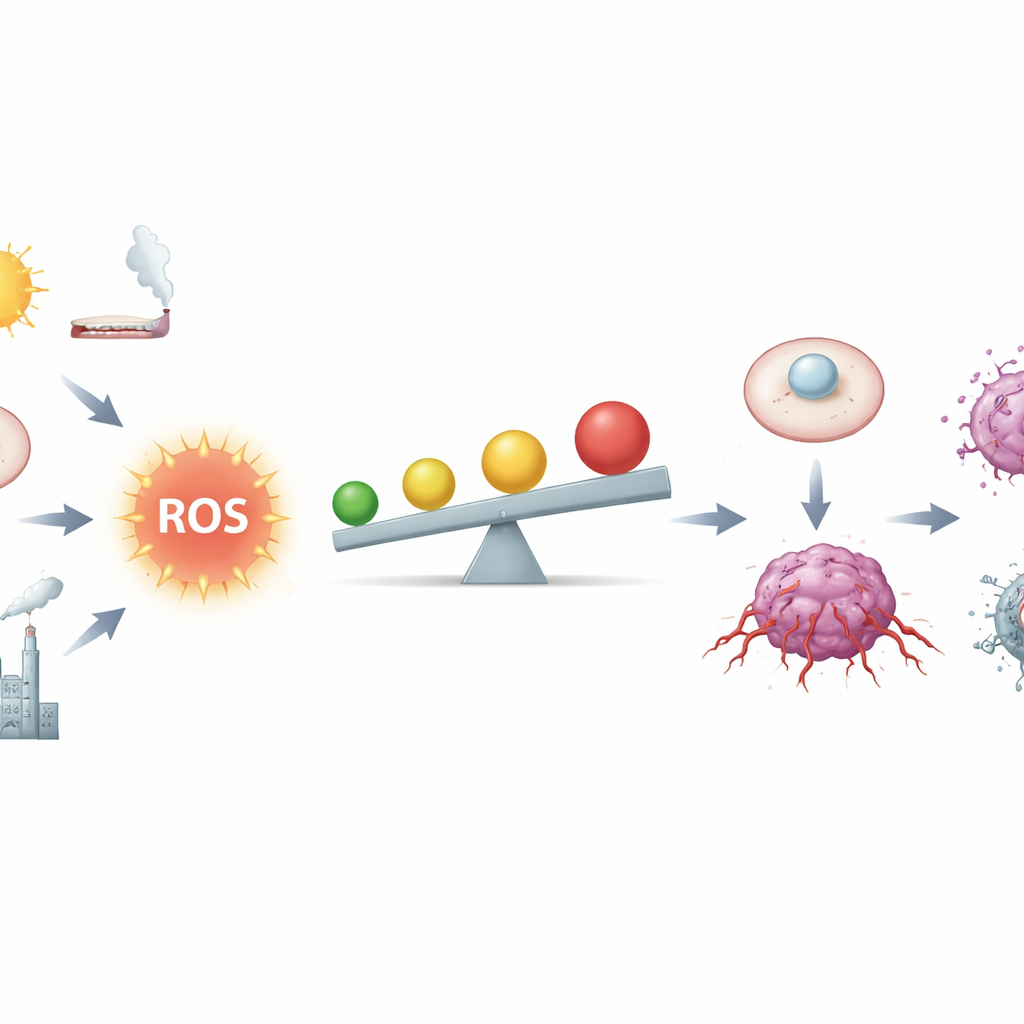
De dunne lijn tussen brandstof en vuur
De auteurs beschrijven ROS als chemische bijproducten van ademhaling en metabolisme, maar ook als krachtige boodschappers. In gezonde weefsels helpen lage niveaus ROS bij de controle van de celcyclus, het herstel van schade en het afstemmen van de immuniteit. Cellen houden deze signalen in toom met een ingewikkeld antioxidantennetwerk, waaronder moleculen zoals glutathion en enzymen die worden geregeld door een meesterregelaar genaamd Nrf2. Kankercellen leven echter dichter bij de gevarenzone: defecte genen, overbelaste mitochondriën, chronische ontsteking, tabaksrook, straling en bepaalde metalen verhogen allemaal ROS. Bij matig hoge niveaus kunnen ROS het DNA aantasten, chromosomen destabiliseren en groei- en overlevingscircuits chronisch inschakelen, waardoor een normale cel gemakkelijker in een kankercel verandert.
Hoe oxidatieve stress het gedrag van tumoren vormgeeft
Zodra een tumor is gevestigd, blijven ROS zijn biologie beïnvloeden. Matige oxidatieve stress activeert vele groeipaden die cellen aanzetten tot delen, het vormen van bloedvaten, het binnendringen van omliggend weefsel en het weerstaan van chemotherapie. ROS kunnen herprogrammeren hoe kankercellen suiker, vetten en aminozuren gebruiken, en brandstof sturen naar routes die extra antioxiderende kracht en bouwstenen voor nieuwe cellen produceren. Ze beïnvloeden ook cellulaire lotbeslissingen: afhankelijk van intensiteit en context kunnen ROS de balans doen doorslaan naar overlevingssignalen of naar verschillende vormen van geprogrammeerde celdood, waaronder klassieke apoptose en nieuwere vormen als ferroptose, necroptose en cuproptose. Dit maakt ROS zowel medeplichtigen in tumorprogressie als potentiële triggers van tumorzelfvernietiging.
Immuniteit en medicijnrespons herbedraden
De review benadrukt dat ROS niet alleen binnen kankercellen werken—ze herschikken ook de omgeving van de tumor. Hoge oxidatieve stress kan kankerbestrijdende T-cellen en natural killer-cellen uitputten of doden, terwijl onderdrukkende cellen die de tumor beschermen worden bevoordeeld. ROS helpen tumoren ook bij het opwaarderen van "dood-me-niet"-signalen zoals checkpoint-eiwitten, waardoor de effecten van immunotherapie worden afgezwakt. Tegelijkertijd kan matige ROS medicijnresistentie aandrijven door drug-effluxpompen en stressreacties te versterken, waardoor kankercellen chemotherapie uitwerpen of de door de therapie veroorzaakte schade herstellen. Onder andere omstandigheden kan het echter overstimuleren van ROS voorbij een kritieke drempel deze verdedigingsmechanismen ontmantelen en tumoren opnieuw gevoelig maken voor behandeling.
Redox-zwakte omzetten in een behandelstrategie
Omdat kankercellen op een slappe koord lopen tussen het benutten van ROS en het vergiftigd worden door hen, zien de auteurs de ROS-balans als een therapeutische hefboom. Een brede strategie is het verlagen van schadelijke ROS of het versterken van antioxidanten, voornamelijk voor preventie of om gezond weefsel tijdens behandeling te beschermen. Een andere aanpak is het tegenovergestelde in tumoren: antioxidantensystemen remmen of ROS-productie verhogen totdat kankercellen een dodelijke drempel overschrijden, vooral in combinatie met straling, gerichte middelen of immunotherapie. Een derde benadering is ROS-niveaus onaangeroerd laten maar de specifieke ROS-gevoelige schakelaars blokkeren—signaaleiwitten, metabole enzymen of doodspaden—waarop tumoren vertrouwen. Door al deze ideeën loopt het thema personalisatie: verschillende kankers hebben verschillende "redox-handtekeningen", dus toekomstige therapieën kunnen bloed- of weefseltesten van oxidatieve schade, antioxidantcapaciteit en ROS-gekoppelde genen vereisen om voor elke patiënt de juiste redox-gerichte behandeling te kiezen.
Wat dit voor patiënten betekent
Simpel gezegd betoogt dit artikel dat ROS noch louter slecht noch louter goed zijn; het zijn krachtige instrumenten die cellen, en kankers, gebruiken. Kankercellen lijken te opereren dichter bij een kantelpunt van oxidatieve stress dan gezonde cellen, wat een therapeutisch venster kan creëren. Omdat antioxidanten en pro-oxidanten echter zowel kunnen helpen als schaden afhankelijk van dosis, timing en tumorsoort, is het gebruik van supplementen of ROS-verhogende middelen zonder onderscheid risicovol. De auteurs concluderen dat de toekomst ligt in zorgvuldig ontworpen therapieën en diagnostiek die de redoxstatus van elke tumor lezen en vervolgens ROS en antioxidantensystemen net genoeg bijsturen—ofwel omlaag om normaal weefsel te beschermen, ofwel omhoog om kankercellen voorbij hun breekpunt te duwen.
Bronvermelding: Akter, S., Madhuvilakku, R., Kar, A.K. et al. Reactive oxygen species (ROS) in cancer: from mechanism to therapeutic implications. Sig Transduct Target Ther 11, 111 (2026). https://doi.org/10.1038/s41392-026-02583-x
Trefwoorden: reactieve zuurstofsoorten, oxiderende stress, kankermetabolisme, redoxtherapie, tumormicro-omgeving