Clear Sky Science · nl
Concordantie-analyse van DNA- en RNA-profileringsgegevens: de IMPACT2-studie van MD Anderson in precisiegeneeskunde voor kanker
Waarom dit onderzoek belangrijk is voor kankerpatiënten
De behandeling van kanker wordt steeds vaker gestuurd door de genetische samenstelling van iemands tumor. Artsen gebruiken al DNA-tests om mutaties te vinden die met specifieke medicijnen gericht kunnen worden, maar deze tests vertellen niet het hele verhaal over hoe een tumor zich gedraagt. Deze studie van het MD Anderson Cancer Center stelt een praktische vraag: als we ook naar RNA kijken—de “bruikbare kopieën” van genen die laten zien welke genen daadwerkelijk aan- of uitgeschakeld zijn—kunnen we dan beter begrijpen welke kanker een patiënt heeft en wat hun overlevingskansen zijn?
Twee informatielagen: DNA en RNA
Elke kankercel draagt veranderingen in zijn DNA, maar DNA is grotendeels een statisch ontwerp. RNA legt daarentegen vast wat de cel op een bepaald moment actief doet. In de IMPACT2-trial ondergingen meer dan 800 patiënten met gevorderde kankers genetische profilering van hun tumoren. Voor 253 van hen waren zowel DNA- als RNA-gegevens beschikbaar. De onderzoekers vergeleken welke genen op DNA-niveau waren gewijzigd (zoals mutaties of extra kopieën) en welke genen ongewoon hoge of lage RNA-niveaus vertoonden; ze onderzochten hoe vaak deze twee lagen hetzelfde verhaal vertelden en of die informatie verband hield met hoe lang patiënten leefden.
Wanneer genveranderingen en activiteit overeenkomen
Het team zocht eerst naar “concordante” gebeurtenissen—gevallen waarin hetzelfde gen afwijkend was op zowel DNA- als RNA-niveau. Van de 253 patiënten hadden er 50 ten minste één dergelijke match, goed voor in totaal 58 gebeurtenissen over 23 genen. De meeste betroffen extra of ontbrekende kopieën van een gen die ook hogere of lagere RNA-niveaus lieten zien, en deze overeenstemming was het sterkst voor bekende kankerdrijvers zoals CDKN2A, AR, ESR1, KRAS, PIK3CA, AKT2, TP53 en CCND1. Deze bevindingen ondersteunen het idee dat structurele DNA-veranderingen bij sommige belangrijke kankergenen inderdaad leiden tot verhoogde of verlaagde genactiviteit, wat hun relevantie als behandeldoelen versterkt.
Verborgen verbanden onthuld door RNA-signalen
Buiten één-op-één-matches testten de onderzoekers meer dan 12.000 genparen om te zien of een DNA-verandering in het ene gen consistent werd gekoppeld aan abnormale RNA-niveaus in een ander gen. Ze vonden 123 significante paren. Veel daarvan clusterden in een belangrijkste groeien overlevingsnetwerk dat bekendstaat als de PI3K/AKT-route, een veelvoorkomend doel van gerichte middelen. Een bijzonder opvallend patroon koppelde veranderingen in het tumorsuppressorgen TP53 aan overactieve RNA-signalen van VEGFA, een gen dat tumoren helpt bij het vormen van nieuwe bloedvaten. Deze relatie kan helpen verklaren waarom sommige patiënten met TP53-afwijkingen in hun tumor reageren op bevacizumab, een medicijn dat de bloedvatvorming remt, en illustreert hoe RNA-gegevens klinisch relevante gen–gen-interacties kunnen blootleggen die DNA alleen mogelijk missen.
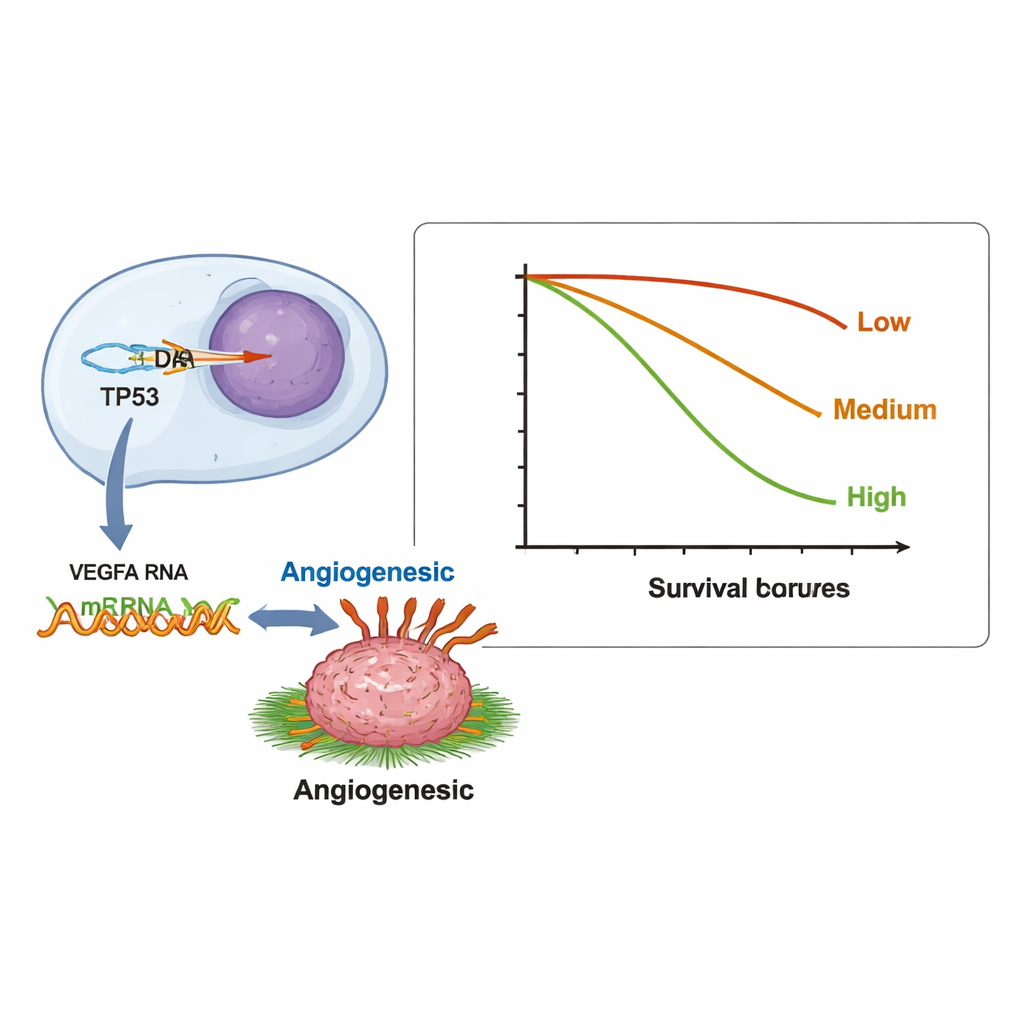
Belasting van genactiviteit en patiëntoverleving
De onderzoekers vroegen ook of de totale hoeveelheid abnormale genactiviteit in een tumor—wat ze tumor transcriptionele belasting of TTB noemen—verband hield met hoe lang patiënten overleefden. Ze telden hoeveel genen bij elke patiënt afwijkende RNA-niveaus vertoonden en groepeerden ze in laag (0–2 genen), intermediair (3–5) en hoog (6 of meer). Patiënten in de hoge groep leefden een mediaan van 6,7 maanden, vergeleken met 9,8 en 11,9 maanden in de lagere groepen. Met andere woorden: tumoren met veel genen die op RNA-niveau niet goed functioneren, leken agressiever te zijn. Tumoren zonder PD-L1, een marker die vaak gebruikt wordt om patiënten voor immunotherapie te selecteren, hadden ook de neiging meer genen met abnormale expressie te hebben, wat wijst op een mogelijk verband tussen brede gendisruptie en een tumoromgeving die immuunaanvallen weerstaat.
Wat dit betekent voor toekomstige kankerzorg
Deze studie laat zien dat RNA-profilering nuttige, aanvullende informatie toevoegt aan DNA-tests bij patiënten met gevorderde kanker in de klinische praktijk. Bij sommige genen komen DNA-veranderingen en RNA-activiteit overeen en versterken ze bekende behandeldoelen; bij andere genen onthullen RNA-patronen nieuwe verbanden die medicijnkeuzes zouden kunnen sturen, zoals de koppeling tussen TP53 en VEGFA. Voor patiënten is het belangrijkste dat een hoge belasting van abnormale genactiviteit geassocieerd was met kortere overleving, wat suggereert dat op RNA gebaseerde maatstaven artsen kunnen helpen inschatten hoe agressief een tumor is en de prognose verfijnen. Hoewel RNA-testen nog niet routinematig worden gebruikt om therapieën te kiezen, ondersteunen deze bevindingen het vooruitzicht dat transcriptomische profilering de volgende stap kan zijn in precisie-oncologie, vooral naarmate grotere studies en betere analysetools transcriptomics naar de dagelijkse kankerzorg brengen.
Bronvermelding: Schmidt, S.T., Baysal, M.A., Fu, S. et al. Concordance analysis of DNA and RNA profiling: The MD Anderson IMPACT2 study in precision oncology. Sig Transduct Target Ther 11, 68 (2026). https://doi.org/10.1038/s41392-026-02580-0
Trefwoorden: precisie-oncologie, RNA-profielering, DNA-sequencing, tumor transcriptionele belasting, kankerbiomarkers