Clear Sky Science · nl
Parathyroïdhormoon–verwant eiwit is een therapeutische target bij idiopathische longfibrose
Waarom littekenvorming in de longen ertoe doet
Idiopathische longfibrose (IPF) is een verwoestende longziekte waarbij fijne luchtzakjes geleidelijk veranderen in stijve littekenweefsels, zodat elke ademhaling zwaar aanvoelt. Huidige geneesmiddelen kunnen deze littekenvorming vertragen maar niet stoppen of terugdraaien. Deze studie onthult een tot nu toe onderschatte dader in dat proces: een klein hormoonachtig eiwit dat door de bekleding van de luchtwegen wordt gemaakt, parathyroïdhormoon-verwant eiwit (PTHrP), en laat zien dat het blokkeren van zijn werking een nieuwe behandelingsmogelijkheid voor IPF zou kunnen bieden.
Een verborgen boodschapper in de luchtwegen
IPF wordt al lang in verband gebracht met overactieve fibroblasten — cellen die normaal weefsel helpen herstellen maar in deze ziekte overmatig collageen aanleggen, het belangrijkste bestanddeel van littekenweefsel. Veel onderzoeken hebben zich gericht op signalen van immuuncellen en de diepste luchtzakechitcellen, maar dit werk kijkt hogerop in de bronchiale boom, naar de buisjes die lucht de longen in voeren. Door grote genetische datasets van mensen met en zonder IPF opnieuw te analyseren, vonden de onderzoekers dat een gen genaamd PTHLH, dat PTHrP codeert, consequent hoger tot expressie kwam in IPF-longen. Microscopische beelden van menselijke longmonsters bevestigden dat het PTHrP-eiwit veel overvloediger aanwezig was bij IPF-patiënten en geconcentreerd zat in de bronchiale epitheelcellen die de luchtwegen bekleden.
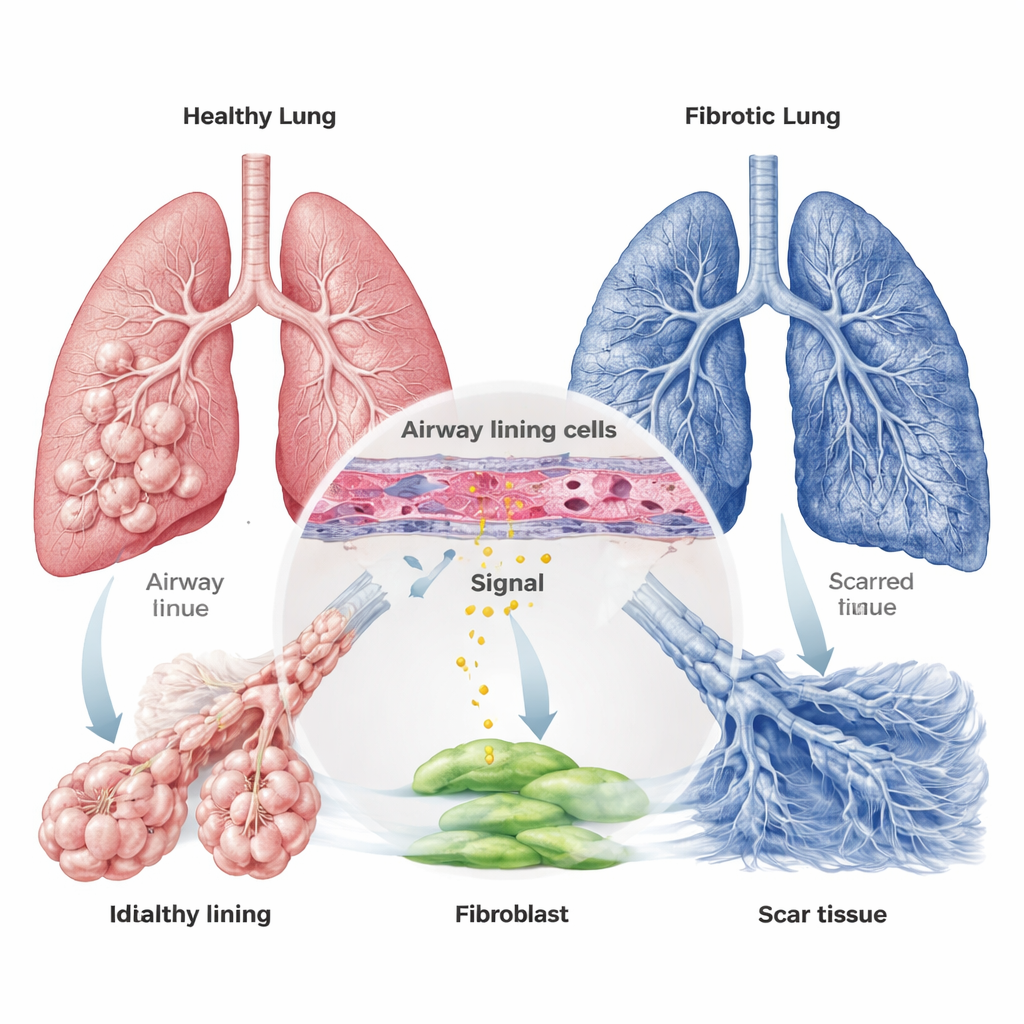
Van luchtwegsignaal naar littekenbouwende cellen
PTHrP wordt geproduceerd als een groter eiwit dat in meerdere kleinere fragmenten kan worden geknipt. Het team richtte zich op één fragment, PTHrP1-34, waarvan bekend is dat het een receptor op bepaalde cellen activeert. Ze toonden aan dat bronchiale epitheelcellen onder stress — zoals lage zuurstof of blootstelling aan het chemotherapie-achtige middel bleomycine, vaak gebruikt om longschade in proefdieren te modelleren — meer PTHrP1-34 in hun omgeving loslaten. Tegelijkertijd vonden ze dat de bijpassende receptor, PTH1R genoemd, voornamelijk niet op de bekledende cellen van de luchtzakjes voorkomt maar op fibroblasten en gladde spiercellen. Dit zet een communicatielijn op: beschadigde luchtwegcellen sturen PTHrP1-34 uit en nabije fibroblasten zijn ingesteld om het te ontvangen.
Hoe het signaal fibroblasten agressief maakt
In laboratoriumschalen maakte het toevoegen van PTHrP1-34 aan menselijke en muislongfibroblasten dat ze een meer agressieve, littekenvormende toestand aannamen. Ze verhoogden de productie van alfa-gladde spieractine (een kenmerk van zogenaamde myofibroblasten) en belangrijke collagegenen, en ze bewogen zich gemakkelijker — kenmerken die geassocieerd worden met progressieve fibrose. Moleculaire testen toonden aan dat dit via een specifieke interne route verloopt: PTHrP1-34 bindt aan PTH1R op het oppervlak van de fibroblasten, verhoogt de boodschapperstof cAMP en activeert een enzym genaamd PKA, dat vervolgens ‘fibrosegenen’ in de celkern aanzet. Het blokkeren van de receptor of het remmen van PKA verminderde deze reactie sterk. Belangrijk is dat luchtweg- en luchtzakepitheelcellen niet op dezelfde manier reageerden, wat benadrukt dat dit hormoonfragment zeer selectief op fibroblasten werkt.
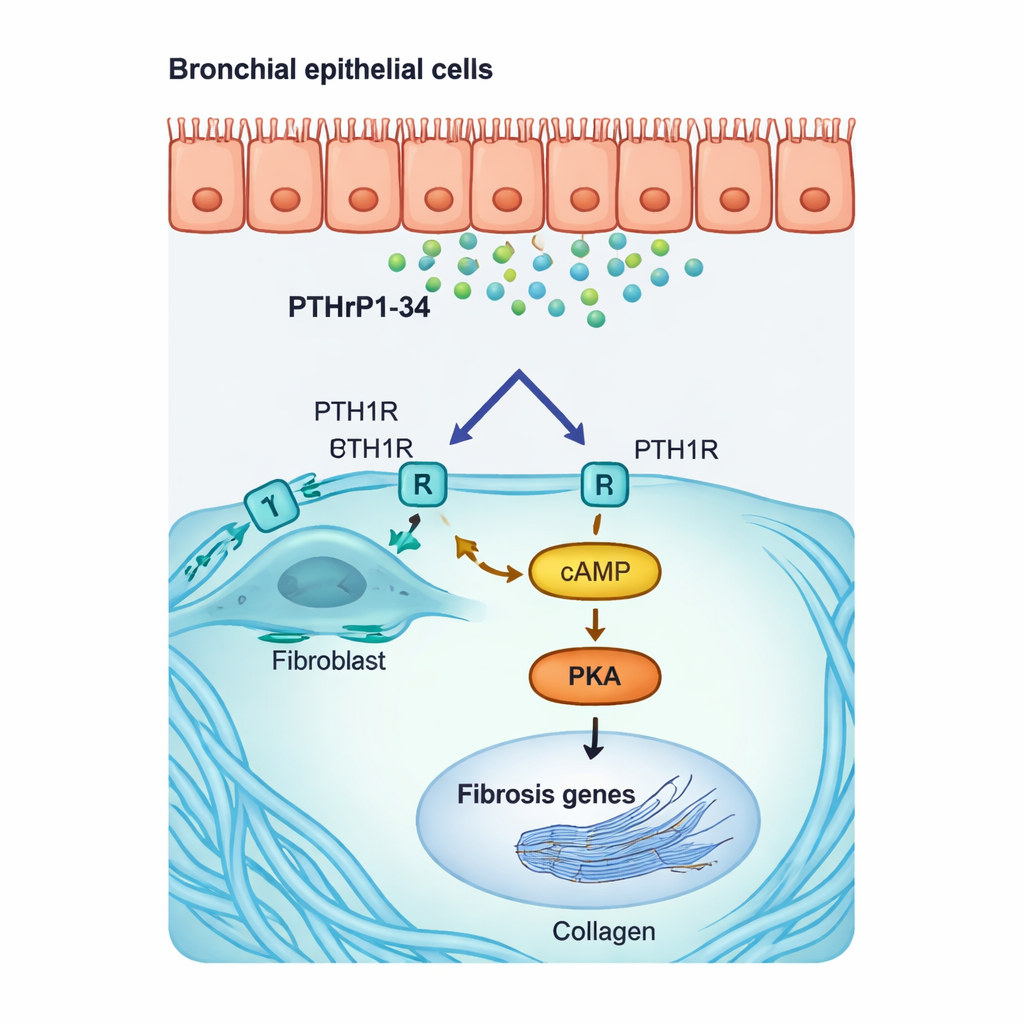
Bewijs in zieke longen en nieuwe behandelrichtingen
Om te zien of deze route er toe doet in volledige longen, gebruikten de onderzoekers muismodellen van longschade veroorzaakt door bleomycine. Terwijl de longen van de dieren vorderden van vroege ontsteking naar dicht littekenweefsel, stegen de PTHrP1-34-niveaus opvallend in de luchtwegen en het longweefsel maar niet in de bloedbaan, wat wijst op een lokale, longspecifieke toename. Direct toedienen van PTHrP1-34 in de luchtwegen zette de longen in de richting van een fibrotische toestand en verergerde, in combinatie met bleomycine, de littekenvorming en collageenopbouw sterk. Het team testte vervolgens drie manieren om dit schadelijke signaal te onderbreken: een neutraliserend antilichaam dat PTHrP1-34 opvangt, een kort peptide dat zijn receptor blokkeert (PTHrP7-34), en een genstilleggende aanpak die de PTHrP-productie in luchtwegcellen verlaagt. In elk geval ontwikkelden de muizen minder longfibrose, hadden ze lagere collageenniveaus en behielden ze beter hun lichaamsgewicht, met effecten die overeenkwamen met of beter waren dan die van nintedanib, een goedgekeurd IPF-middel.
Wat dit betekent voor toekomstige zorg
Voor niet-specialisten is de kernboodschap dat het bronchiale epitheel niet slechts een passieve leiding voor lucht is; het kan actief longfibrose aanjagen door krachtige chemische boodschappen uit te sturen. Deze studie identificeert PTHrP1-34 als één van die boodschappen en toont aan dat het blokkeren van het gesprek tussen dit fragment en fibroblasten fibrose in diermodellen kan vertragen of zelfs omkeren. Hoewel meer werk nodig is om veiligheid en effectiviteit bij mensen te bevestigen, zou het richten op de PTHrP1-34/PTH1R-route een geheel nieuwe klasse behandelingen voor IPF kunnen toevoegen, met als doel niet alleen het vertragen van de ziekte maar het aanpakken van een van haar grondoorzaken.
Bronvermelding: Fang, XQ., Lim, S., Lee, YM. et al. Parathyroid hormone–related protein is a therapeutic target in idiopathic pulmonary fibrosis. Sig Transduct Target Ther 11, 67 (2026). https://doi.org/10.1038/s41392-026-02578-8
Trefwoorden: idiopathische longfibrose, longfibrose, parathyroïdhormoon-verwant eiwit, fibroblastactivatie, bronchiaal epitheel